Болезнь Рефсума
Боле́знь Ре́фсума (БР) — наследственное заболевание из группы пероксисомных заболеваний, относящееся к спектру синдрома Цельвегера. Оно характеризуется дефектами в метаболизме фитановой кислоты из-за недостаточности фермента фитаноил-КоА-гидроксилазы или нарушения его транспорта в пероксисомы, вызванного мутациями в генах PHYH или PEX7. Основные проявления включают неврологические расстройства, снижение зрения, слуха и обоняния, патологическое ороговение кожи, а также сердечные проявления. Заболевание может дебютировать в любом возрасте — от раннего детства до 50 лет[3].
Общие сведения
История
В 1946 году норвежский невролог Сигвальд Бернхард Рефсум впервые описал это заболевание, наблюдая за членами одной семьи. Изначально он назвал патологию наследственная атаксия с полиневритом, но впоследствии за ней закрепилось более краткое название — болезнь Рефсума, а первоначальный термин почти вышел из употребления. В 1960-х годах учёные раскрыли биохимическую основу болезни, обнаружив нарушение метаболизма фитановой кислоты, и уже к концу десятилетия разработали для пациентов специальную диету с ограничением этого вещества. К 1970-м годам применение плазмафереза позволило ослабить строгие пищевые ограничения и улучшить жизнь больных. В конце 1990-х годов были идентифицированы гены PHYH (10-я хромосома) и PEX7 (6-я хромосома), мутации в которых приводят к развитию БР[3].
Этиология
БР — это наследственное заболевание с аутосомно-рецессивным типом наследования. В большинстве случаев оно вызвано мутациями в гене PHYH, расположенном на хромосоме 10p13. Этот ген кодирует фермент ФКАГ, участвующий в метаболизме фитановой кислоты. При мутациях фермент становится неактивным, что приводит к накоплению фитановой кислоты в организме. В редких случаях БР развивается из-за дефектов в гене PEX7 (хромосома 6q21-q22.2), который кодирует рецептор PTS2. Этот рецептор необходим для транспорта определённых белков, включая ФКАГ, в пероксисомы[4].
Патогенез
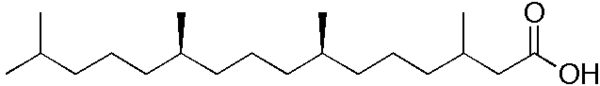
БР возникает из-за изолированного нарушения метаболизма фитановой кислоты (3,7,11,15-тетраметилгексадекановой кислоты) — разветвлённой жирной кислоты, что приводит к её накоплению в тканях. Фитановая кислота не синтезируется в организме человека и поступает исключительно с пищей, в основном с молочными продуктами, мясом и животными жирами. Из-за наличия 3-метильной группы фитановая кислота не может расщепляться путём бета-окисления. Вместо этого она транспортируется в пероксисомы, где подвергается альфа-окислению — процессу, укорачивающему молекулу на один атом углерода с образованием пристановой и муравьиной кислот. Первый этап альфа-окисления катализируется пероксисомальным ферментом ФКАГ. Именно мутации, снижающие активность этого фермента, нарушают расщепление фитановой кислоты. Избыточное накопление фитановой кислоты в организме приводит к её включению в клеточные мембраны различных тканей, включая фоторецепторы сетчатки, миелиновые оболочки нервных волокон, кератиноциты кожи и кардиомиоциты. Это патологическое встраивание вызывает повреждение сетчатки, множественное поражение периферических нервов, нарушения кератинизации кожи и различные формы сердечной аритмии[3][4].
При гистологическом исследовании кожи выявляются характерные признаки вульгарного ихтиоза: умеренный гиперкератоз, акантоз с истончением зернистого слоя. В базальных и супрабазальных кератиноцитах обнаруживаются вакуоли различных размеров. При проведении липидного окрашивания на срезах, полученных методом криостатной резки, подтверждается накопление липидов в этих вакуолях. Гистологическое исследование нервной ткани выявляет типичную картину демиелинизации с выраженной пролиферацией шванновских клеток и формированием «луковичных» структур (концентрическое разрастание клеток вокруг повреждённых нервных волокон)[5].
Эпидемиология
Из-за крайней редкости заболевания точные данные о его распространённости ограничены: она оценивается в менее чем 1 случай на 1 000 000 человек. Возраст начала клинических проявлений варьирует в широких пределах — от 7 месяцев до 50 лет, однако в большинстве случаев первые симптомы появляются до 20-летнего возраста[4].
Диагностика
БР обычно проявляется медленно прогрессирующей периферической нейропатией с выраженной мышечной слабостью и атрофией, особенно в нижних конечностях. Типичная клиническая картина также включает[6]:
- офтальмологические проявления: наиболее характерным и постоянным симптомом заболевания является пигментный ретинит, который наблюдается у всех пациентов. Первыми клиническими проявлениями болезни обычно становятся нарушения сумеречного зрения, постепенное концентрическое сужение полей зрения и снижение остроты зрения. По мере прогрессирования заболевания развиваются катаракта, атрофия зрительного нерва, помутнения стекловидного тела, нистагм, а также миоз со слабой реакцией зрачков на свет. Эти изменения в совокупности приводят к значительному ухудшению зрительной функции у пациентов с БР;
- мозжечковую симптоматику: у пациентов может отмечаться неустойчивость походки, умеренные нарушения координации движений и другие признаки мозжечковой дисфункции. Мозжечковая симптоматика при болезни Рефсума прогрессирует относительно медленно и редко бывает первым проявлением заболевания;
- сенсорную и моторную полинейропатию: у пациентов с БР развивается хроническая прогрессирующая полинейропатия смешанного (моторно-сенсорного) типа с симметричным поражением, которое первоначально затрагивает дистальные отделы нижних конечностей. Характерными проявлениями являются мышечная атрофия, слабость и сенсорные нарушения. Нейропатия может носить эпизодический характер на ранних стадиях, предшествуя зрительным и слуховым нарушениям на несколько лет. По мере прогрессирования заболевания мышечная слабость становится более распространённой и инвалидизирующей, затрагивая не только конечности, но и мышцы туловища. Сенсорные нарушения включают преимущественно снижение глубокой чувствительности, особенно вибрационной и проприоцептивной, в дистальных отделах ног. Осмотр выявляет утрату глубоких рефлексов, а также отсутствие или ослабление подошвенных рефлексов.
Помимо основных симптомов, у пациентов могут наблюдаться другие характерные нарушения[6]:
- аносмия;
- нарушения слуха — обычно проявляются нейросенсорной тугоухостью при сохранной функции вестибулярного аппарата;
- сердечные проявления включают кардиомиопатию, нарушения проводимости. Описаны случаи внезапной смерти, связанной с острой сердечной недостаточностью;
- скелетные аномалии: укорочение или удлинение плюсневых костей (чаще III и IV), синдактилия, укороченные и расширенные фаланги или пястные кости, молоткообразные пальцы стоп;
- кожные изменения — варьируют от лёгкой сухости кожи (особенно на туловище) до выраженного ихтиоза, хотя у некоторых пациентов кожные проявления могут полностью отсутствовать.
Офтальмоскопия: характерными проявлениями являются тонкозернистые пигментные отложения, создающие картину «соли с перцем», а также частое отсутствие классических «костных спикул», типичных для обычных форм пигментного ретинита. При детальном осмотре выявляются значительные структурные изменения сетчатки: выраженное истончение внутреннего ядерного слоя и заметное уменьшение количества ганглиозных клеток[6].
Электроретинография выявляет снижение или отсутствие ответов палочек и колбочек, отражающее прогрессирующую дегенерацию фоторецепторов[6].
Электронейромиография: характерно снижение скорости проведения по чувствительным нервам, при этом замедление проведения носит неравномерный характер[6].
Магнитно-резонансная томография: могут обнаруживаться характерные симметричные изменения сигнала в кортикоспинальных трактах, зубчатых ядрах мозжечка и мозолистом теле[5].
Биохимический анализ крови: характерно повышение концентрации фитановой кислоты в плазме крови (>200 мкмоль/л)[4].
Молекулярно-генетический анализ: характерно выявление мутаций в генах PHYH и PEX7 методом секвенирования[4].
Дифференциальная диагностика
Дифференциальная диагностика БР проводится со следующими состояниями[4]:
- синдром Ашера;
- синдром Барде — Бидля;
- синдром Альстрёма;
- синдром Кернса — Сейра;
- дефицит альфа-метил-ацил-КоА-рацемазы;
- спектр болезней Цельвегера;
- ризомелическая точечная хондродисплазия;
- синдром Шегрена — Ларссона.
Лечение
Основной метод лечения — диета со строгим ограничением продуктов, содержащих фитановую кислоту[4]:
- мясо и жиры жвачных животных (баранина, говядина);
- некоторые виды рыбы;
- хлебобулочные изделия с животными жирами;
- молочные продукты (сливочное масло, сыр).
Цель диеты — снизить ежедневное потребление фитановой кислоты до менее чем 10 мг. Важно избегать резкой потери веса и длительного голодания, так как эти состояния вызывают липолиз и высвобождение фитановой кислоты из печени и жировой ткани[4].
Плазмаферез применяется для экстренного выведения фитановой кислоты из крови, особенно при острых состояниях с критически высокими уровнями (>1500 мкмоль/л). В качестве поддерживающей терапии при хорошо контролируемом уровне фитановой кислоты диетой плазмаферез не применяется[4].
Прогноз
Прогноз заболевания вариабелен и зависит от нескольких факторов: возраста начала симптомов, скорости прогрессирования, тяжести течения и, что наиболее важно, от строгости соблюдения терапии — в первую очередь, диеты с ограничением фитановой кислоты. При отсутствии лечения прогноз в целом неблагоприятный: в тяжёлых или поздно диагностированных случаях заболевание может представлять угрозу для жизни. Основными причинами летального исхода являются жизнеугрожающие аритмии и сердечная недостаточность. Своевременная диагностика и строгое соблюдение рекомендаций по диете значительно улучшают перспективы пациентов[4][7].
Диспансерное наблюдение
Не разработано.
Профилактика
Не разработана.
Примечания
Литература
- Мамедов И. С., Смолина Ю. А., Сухоруков В. С., Новиков П. В. Диагностика пероксисомных болезней у детей // Клиническая лабораторная диагностика. — 2012. — № 3.
- Полякова С. И., Засурцев Г. В., Паршина П. В., Кобринский Б. А. Перспективы диагностики и лечения дефицита плазмалогенов // Российский вестник перинатологии и педиатрии. — 2021. — № 4.