UBTF
UBTF (англ. upstream binding transcription factor, RNA polymerase I, другие названия UBF; UBF1; UBF2; UBF-1; NOR-90) — ядрышковый транскрипционный фактор, регулирующий транскрипцию генов рРНК РНК-полимеразой I и ряд других процессов. У человека кодируется геном UBTF, расположенным на 17-й хромосоме[5]. UBTF представлен единственной полипептидной цепью, причём за связывание с ДНК отвечает особый домен HGM-бокс. Белок локализуется в ядрышке, точнее, в фибриллярных центрах и плотном фибриллярном компоненте. Нарушения работы UBTF приводят к различным заболеваниям, в том числе раковым.
Что важно знать
Классификация
Ген и изоформы
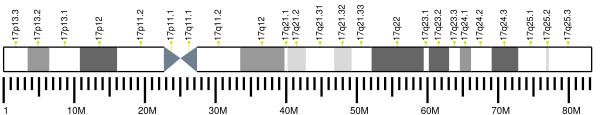
Ген UBTF у человека находится на 17-й хромосоме в локусе 17q21.31 и содержит 25 экзонов. У млекопитающих известны 2 изоформы белка UBTF, которые образуются из-за альтернативного сплайсинга первичных транскриптов гена UBTF: UBTF1 и UBTF2[9]. Псевдогены этого гена располагаются на коротких плечах хромосом 3, 11 и Х, а также длинном плече хромосомы 11[5][10].
Структура
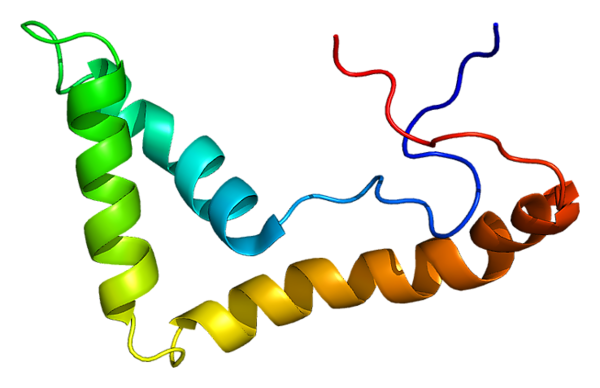
Белок UBTF представлен единственной цепью из 764 аминокислотных остатков. Во вторичной структуре имеются альфа-спирали, бета-слои и бета-поворот. Связывание с ДНК обеспечивается шестью мотивами HGM-бокс. Белок также характеризуется наличием N-концевого домена димеризации и С-концевого кислого хвоста. У изоформы UBTF2 отсутствуют 37 аминокислот из второго HGM-бокса[9].
В растворе UBTF формирует димеры, димеризация осуществляется за счёт N-концевого домена длиной более 80 аминокислотных остатков. Этот домен чрезвычайно консервативен, поэтому, возможно, участвует также в регуляции транскрипции и/или связывании UBTF с функциональными ядрышковыми организаторами. Среди HGM-боксов UBTF для связывания с ДНК совершенно необходим только первый, а другие HGM-боксы усиливают это взаимодействие. HGM-боксы UBTF имеют характерную изогнутую L-образную форму и состоят из трёх альфа-спиралей, которые могут вносить конформационные изменения в ДНК. В условиях in vitro димер UBTF лягушки Xenopus может изгибать в петлю свободную от нуклеосом рДНК длиной до 180 пар оснований. Кроме того, UBTF может одновременно связываться с двумя молекулами ДНК[9].
C-концевой домен UBTF состоит из 57 остатков кислых аминокислот (глутаминовой и аспарагиновой кислоты), а также 23 остатков серина. Кислый домен играет ключевую роль в участии UBTF в активации транскрипции. Именно этот отрицательно заряженный домен обусловливает окрашивание активных ядрышковых организаторов солями серебра[9].
UBTF может подвергаться таким посттрансляционным модификациям, как ацетилирование и фосфорилирование (по остатку треонина Thr201 и 12 остаткам серина)[10]. О функциональном значении посттрансляционных модификаций см. раздел Регуляция.
Внутриклеточная локализация
UBTF — чрезвычайно многочисленный транскрипционный фактор; так, в первичных человеческих фибробластах обнаруживается до 106 молекул на клетку[11]. UBTF — ядрышковый белок, обнаруживается в двух ядрышковых компонентах — плотном фибриллярном компоненте и фибриллярных центрах. Кроме того, он может обнаруживаться в нуклеоплазме[10]. UBTF характеризуется очень высоким сродством к рДНК и в условиях in vivo может связываться с ней в отсутствие промоторов и транскрипции[12]. На клетках HeLa было показано, что ядрышковая локализация UBTF связана с интенсивностью транскрипции генов рРНК (рДНК). В ядрышках, имеющих единственный крупный фибриллярный центр (такие ядрышки характеризуются низким уровнем транскрипции рДНК), UBTF располагается преимущественно там. Однако в ядрышках, характеризующихся интенсивной транскрипцией рДНК и имеющих множество мелких фибриллярных центров, UBTF локализуется в основном на границе фибриллярных центров и плотного фибриллярного компонента[13].
Функции
Долгое время считалось, что единственная функция UBTF — участие в образовании преинициаторного комплекса на промоторах рДНК. Согласно одной из моделей, UBTF связывает вышестоящие и коровые промоторные элементы, в результате чего образуется петля ДНК, на которой собирается похожий на нуклеосому белковый комплекс. Благодаря этому UBTF может взаимодействовать с транскрипционным фактором TIF-1B (SL1). Образующийся комплекс привлекает РНК-полимеразу I. Впрочем, сейчас настоящий механизм образования преинициаторного комплекса и роль UBTF в инициации транскрипции рДНК менее ясны: показано, что в условиях in vitro UBTF не является совершенно необходимым для инициации транскрипции[14].
В ходе экспериментов по интеграции длинного ряда сайтов связывания UBTF из рДНК лягушки Xenopus laevis в геном клеток человека было показано, что UBTF необходим для формирования ядрышка. В этих рядах наблюдалось образование похожих на ядрышки структур, следовательно, UBTF выступал как площадка для сборки ядрышек даже в отсутствие транскрипции, опосредованной РНК-полимеразой I[15]. UBTF совместно с машинерией РНК-полимеразы I, нуклеолином, нуклеофозмином и фибрилларином относится к числу первых факторов, с которых начинается сборка ядрышка и привлечение прочих белковых компонентов ядрышек[16]. UBTF задействован в регуляции биогенеза рибосом[17].
Имеется ряд свидетельств участия UBTF в перестройках хроматина (ремоделирование хроматина). Показано, что UBTF необходим для поддержания структуры эухроматина в области активных ядрышковых организаторов (англ. nucleolar organizer region, NOR). Возможно, что это связано с конкурентным вытеснением UBTF линкерного гистона H1, который участвует в гетерохроматинизации. UBTF совершенно необходим для формирования активных ядрышковых организаторов, в условиях нокаута у мышей соответствующего гена образование NOR нарушено[18]. Таким образом, UBTF препятствует образованию гетерохроматина в области рДНК и способствует поддержанию активной конформации хроматина[14].
Показано, что у мышей метилирование динуклеотида CpG в позиции −133 относительно коровой части промотора рДНК ядрышковым комплексом ремоделирования NoRC обеспечивает транскрипционный сайленсинг генов рРНК и уменьшает связывание UBTF с промоторами рДНК. В конечных стадиях дифференцировки промиелоцитов мыши сайленсинг рДНК увеличивается, при этом связывание UBTF с повторами рДНК также уменьшается. Поскольку экспрессия UBTF постепенно сокращается на конечных стадиях дифференцировки многих клеточных линий, возможно, что регуляция UBTF служит ключевым механизмом сайленсинга рДНК в ходе развития[14]. Действительно, при помощи делеции гена UBTF было показано, что белок UBTF необходим для развития зародыша до стадии морулы. Интересно, что утрата UBTF индуцировала образование в ооцитах и ранних эмбрионах крупных внутриядерных структур, похожих на тельца-предшественники ядрышек (NPB)[19]. Показано, что в отсутствие UBTF у мышей происходит разборка ядрышек в соматических клетках и накопление ключевых факторов транскрипции генов рРНК в плотных внутриядерных тельцах, похожих на NPB. В эмбрионах же сами NPB и окружающий их гетерохроматин разрушены[20].
В 2015 году было показано, что UBTF участвует в поддержании стабильности генома, регулируя гены, активно транскрибируемые РНК-полимеразой II[21].
Регуляция
Активность UBTF может регулироваться посредством посттрансляционных модификаций. Например, фосфорилирование UBTF усиливает транскрипцию генов рДНК[22]. Так, белок mTOR (ключевой регулятор клеточного роста) регулирует транскрипцию генов рРНК через белок S6K1 и фосфорилирование С-концевого домена UBTF[23]. Фосфоинозитид-3-киназа фосфорилирует UBTF в ходе сигнального пути инсулиноподобного фактора роста. UBTF также может быть фосфорилирован киназами ERK1/2. Так, активация пути MAPK/ERK эпидермальным фактором роста (EGF) вызывает опосредованное ERK1/2 фосфорилирование UBTF по первым двум HGM-боксам, что приводит к положительной регуляции транскрипции рДНК за счёт усиления элонгации транскрипции РНК-полимеразой I. Фосфорилирование HGM-боксов 1 и 2 посредством ERK повышает их сродство к линейной ДНК, что облегчает элонгацию транскрипцию, проводимую РНК-полимеразой I[17]. UBTF может активироваться в результате фосфорилирования комплексами циклинов и циклинзависимых киназ, специфичных для фазы G1 клеточного цикла[24]. Человеческий опухолевый супрессор p14ARF подавляет фосфорилирование UBTF и, следовательно, транскрипцию рДНК[25].
Показано, что состояние ацетилированности UBTF изменяется в ходе клеточного цикла и ацетилирование UBTF влияет на его взаимодействие с РНК-полимеразой I[26]. Белковый комплекс RUNX2 и гистондеацетилазы 1 (HDAC1) регулирует экспрессию рРНК, деацетилируя UBTF[27]. Белок hALP может активировать транскрипцию, опосредуемую РНК-полимеразой I, связываясь с UBTF и ацетилируя его[28].
Взаимодействие UBTF с ДНК может непосредственно регулироваться связыванием с фосфатидилинозитол-4,5-бисфосфатом[29].
Взаимодействие с другими белками
В таблице ниже перечислены ключевые белки, с которыми взаимодействует UBTF[30]:
| Белок | Функция | Экспериментальное подтверждение |
|---|---|---|
| PAF53 | Субъединица РНК-полимеразы I | Взаимодействие in vitro и коиммунопреципитация |
| PAF49 | Субъединица РНК-полимеразы I | Взаимодействие in vitro |
| TAFI48 | Субъединица SL1 | Взаимодействие in vitro |
| TBP | Субъединица SL1 | Взаимодействие in vitro |
| Treacle | Взаимодействует с боксом C/D малых ядрышковых РНК | Дрожжевая двугибридная система и коиммунопреципитация |
| SIRT7 | Потенциальная АДФ-рибозилтрансфераза и деацетилаза | Взаимодействие in vitro |
| CTCF | Организация хроматина | Взаимодействие in vitro и ковыделение |
Консервативность
Долгое время считалось, что UBTF имеется только у позвоночных. Это представление подкреплялось отсутствием похожих на UBTF белков у таких модельных организмов, как муха Drosophila, круглый червь Caenorhabditis elegans, дрожжи Saccharomyces cerevisiae и цветковое растение Arabidopsis. Однако с увеличением данных о последовательностях ДНК разнообразных организмов UBTF был найден у животных, не относящихся к позвоночным. Например, UBTF был найден у хордового животного — асцидии Ciona intestinalis. Аминокислотные последовательности N-концевого домена димеризации и первого HGM-бокса у Ciona и человека совпадают на 40 и 54 % соответственно. Более того, у Ciona, как и у человека, UBTF содержит несколько (по крайней мере пять) HGM-боксов[31].
Оказалось, далее, что UBTF имеется у разнообразных членистоногих (например, у клеща Ixodes scapularis, жука Tribolium castaneum, тли Acyrthosiphon pisum). Даже в геноме примитивного животного Trichoplax adhaerens найдена открытая рамка считывания, очень похожая на UBTF. Сравнение UBTF Trichoplax и Ciona выявило 27 % сходства в последовательностях доменов димеризации. Гомолог UBTF Trichoplax также имеет несколько HGM-боксов, причём бокс, соседний с доменом димеризации, имеет 30 % сходства с аналогичным доменом Ciona, однако UBTF Trichoplax не имеет кислого N-концевого домена. По-видимому, у модельных беспозвоночных животных имело место сильная утрата генов, в том числе кодирующих UBTF. У грибов и растений, похоже, UBTF нет. У дрожжей Saccharomyces cerevisiae обнаружен HGM-содержащий белок HMO1, который может играть роли, аналогичные функциям UBTF Metazoa[32].
Клиническое значение
Вирус простого герпеса первого типа вызывает перемещение UBTF из ядрышка клетки-хозяина в компартменты репликации вируса. Однако было показано, что UBTF не способствует репликации вируса, а, напротив, подавляет её[33].
Продемонстрировано, что онкопротеин E7 человеческого папилломавируса стимулирует транскрипцию генов рДНК, увеличивая количество фосфорилированной формы UBTF[34].
Повышенный уровень экспрессии UBTF, соответствующий положительной регуляции транскрипции рДНК, связан с гипертрофией сердца[35]. Напротив, при дифференцировке уровень транскрипции рДНК снижен, что соответствует значительному уменьшению экспрессии UBTF[36].
Установлено, что нарушения ацетилирования UBTF по остатку лизина 352 связаны с нарушениями транскрипции рДНК при болезни Хантингтона[37].
Показано, что у пациентов с гепатоцеллюлярной карциномой наблюдаются повышение уровня экспрессии UBTF, приводящее к онкогенному эффекту. Оказалось, что белок HBx вируса гепатита B активирует злокачественное перерождение клеток через c-Myc-зависимое усиление экспрессии UBTF[38].
Показана связь между утратой волос у человека и уровнем экспрессии UBTF[39].
Примечания
Литература
- The Nucleolus / Ed. by Mark O. J. Olson. — New York: Springer Science+Business Media, 2011. — xxvi + 414 p. — (Protein Reviews, vol. 15). — ISBN 978-1-4614-0514-6. — doi:10.1007/978-1-4614-0514-6.
- Proteins of the Nucleolus / O'Day, Danton H, Catalano, Andrew. — Netherlands: Springer, 2013. — ISBN 978-94-007-5818-6. — doi:10.1007/978-94-007-5818-6.