Мотив (молекулярная биология)
Моти́в в молекулярной биологии — относительно короткая последовательность нуклеотидов или аминокислот, слабо меняющаяся в процессе эволюции и, по крайней мере предположительно, имеющая определённую биологическую функцию[1][2][3]. Под мотивом иногда подразумевают не конкретную последовательность, а каким-либо образом описанный спектр последовательностей, каждая из которых способна выполнять определённую биологическую функцию данного мотива[4].
Мотивы встречаются в живых организмах повсеместно и выполняют множество жизненно важных функций, таких как регуляция транскрипции и трансляции (в случае нуклеотидных мотивов), посттрансляционная модификация и клеточная локализация белков, и частично обуславливают их функциональные свойства (лейциновая молния)[2][5]. Они широко используются в биоинформатике для предсказания функций генов и белков, построения карт регуляции, важны для многих задач генной инженерии и молекулярной биологии в целом[6][7][8].
В связи с практической важностью мотивов, разработаны как биоинформатические методы их поиска (MEME, Gibbs Sampler), так и методы поиска мотивов in vivo (ChIP-seq, ChIP-exo). Последние довольно часто дают приблизительные координаты мотивов и их результаты затем уточняются биоинформатическими методами[1][2][6].Для удобства хранения мотивов в базах данных используются их разные, отличающееся степенью детальности, представления, наиболее распространенными из которых являются консенсус и позиционная весовая матрица[2].
Следует отличать мотив от консервативных участков в близкородственных организмах, необладающих значимыми биологическими функциями, где мутационный процесс не успел ещё достаточно их изменить[9].
Мотивы в нуклеиновых кислотах
В случае с ДНК чаще всего мотивы представляют собой короткие последовательности, являющиеся сайтами связывания для белков, таких, как нуклеазы и транскрипционные факторы, или вовлечённые в важные регуляторные процессы уже на уровне РНК, такие как посадка рибосомы, процессинг мРНК и терминация транскрипции[4].
Изучение мотивов в ДНК стало возможным благодаря появлению в 1973 году[10] процедуры секвенирования ДНК (определения последовательности нуклеотидов фрагмента ДНК). Первыми были определены последовательности lac-оператора и лямбда-оператора[11]. Однако до появления более производительных методов секвенирования[12], количество последовательностей мотивов оставалось достаточно малым. К концу 1970-х годов появилось множество примеров мутантных последовательностей (сайтов), связывающих транскрипционные факторы и последовательностей с изменённой специфичностью[13]. С увеличением количества последовательностей, стали развиваться и методы теоретического предсказания мотивов. В 1982 году была впервые сконструирована позиционно-весовая матрица (ПВМ) мотива сайта инициации трансляции. С помощью построенной ПВМ были предсказаны другие сайты инициации трансляции[14]. Этот подход оказался достаточно мощным и до сих пор в разных формах применяется для поиска известных мотивов в геномах, а конкретные методы различаются только видом весовой функции[4]. Однако подход, основанный на построении ПВМ на базе уже имеющихся последовательностей, не позволял находить принципиально новые мотивы, что является более сложной задачей. Первый алгоритм, решавший эту задачу, был предложен Галласом с коллегами в 1985 году[15]. Этот алгоритм был основан на поиске общих слов в наборе последовательностей и давал большой процент ложноотрицательных результатов, однако он стал основой для целого семейства алгоритмов[16]. Позднее были разработаны более точные вероятностные методы: алгоритм MEME, основанный на процедуре максимизации ожидания[17] и алгоритм Gibbs Sampler, также основанный на процедуре максимизации ожидания[18]. Оба метода оказались очень чувствительными и используются в настоящее время для предсказания мотивов в наборах последовательностей.
После разработки мощных средств для предсказания мотивов связывания транскрипционных факторов и установления соответствия между достаточным количеством транскрипционных факторов и мотивов, стало возможным предсказывать функции оперона, лежащего поблизости от мотива по специфичности транскрипционного фактора, с ним связывающегося и наоборот, предсказывать транскрипционный фактор по генам в опероне, лежащем рядом с определённым мотивом[3].
Характерными примерами регуляции транскрипции, осуществляемой с помощью белка, распознающего специальный мотив, являются:
- Сайт пуринового репрессора PurR у Escherichia coli. PurR связывается с последовательностью в 16 нуклеотидов, которая расположена перед пуриновым опероном и регулирует транскрипцию генов, ответственных за синтез пуриновых и пиримидиновых нуклеотидов[5][19]. Интересно, что у бактерии Bacillus subtilis, эволюционно далёкой от кишечной палочки, также есть пуриновый репрессор, не гомологичный PurR[20];
- Сайт лактозного оперона Lac. Лактозный оперон контролируется репрессором LacI, который, связывая ДНК, препятствует транскрипции генов, ответственных за катаболизм лактозы[6].
Одними из наиболее известных примеров регуляции трансляции при помощи мотив-распознающих регуляторов являются:
- Сайт посадки рибосомы прокариот — последовательность Шайн — Дальгарно[21], здесь связывание происходит с рибопротеином;
- Сайт посадки рибосомы эукариот — последовательность Козак, связывание происходит с эукариотическим фактором инициации трансляции eIF1[7];
- IRE — регуляторные элементы, располагающиеся на 5’UTR и/или 3’UTR мРНК ферментов (к примеру, ферритина), регулирующие содержание железа в клетке. С этими мотивами связываются белки IRP1 (цитозольная форма аконитазы) и IRP2 (каталитически неактивный гомолог аконитазы), регулируя самим фактом своего связывания с мРНК скорость её деградации или скорость трансляции, происходящей с неё[22].
Сила взаимодействия белка или РНК с ДНК мотивом зависит в первую очередь от последовательности данного мотива. Различают «сильные» мотивы, дающие сильное взаимодействие с белком или РНК и «слабые» мотивы, с которыми взаимодействие слабее. Практически всегда удаётся получить так называемую «консенсусную последовательность» («консенсус»), то есть такую последовательность, в каждой позиции которой стоит буква, наиболее часто встречающаяся в соответствующей позиции в последовательностях мотивов из разных организмов. Консенсусная последовательность принимается за самую сильную, каковой она почти всегда и является[23]. Более слабые мотивы получаются из неё с помощью небольшого (чаще всего 1—3) числа замен[24].
В процессе эволюции сила мотивов регулируется с помощью естественного отбора, причём мотив может становиться как сильнее, так и слабее[25]. Характерным примером такой подстройки силы мотива может служить изменчивость последовательности Шайна — Дальгарно (ШД). Есть тесная корреляция между необходимым организму количеством транслируемого белка и силой ШД перед ним[8].
Важно отметить, что в случае с ШД, хотя сила связывания белка и напрямую коррелирует с силой связывания 16S-субъединицы рибосомы, в связи с особенностями инициации трансляции, консенсусная последовательность не обязательно будет гарантировать наиболее эффективную трансляцию (из-за затруднённого ухода рибосомы с сайта инициации)[6]. Поэтому последовательность Шайна — Дальгарно чаще всего содержит 4—5 нуклеотидов из консенсусной последовательности при длине последней примерно в 7 нуклеотидов[26].
Не всегда наличие мотива, явно выполняющего биологически значимую роль, влечёт за собой наличие белка-регулятора. Регуляция также может осуществляться за счёт связывания РНК с каким-либо низкомолекулярным веществом. На этом принципе построены РНК-переключатели — структуры, образующиеся на РНК во время транскрипции, способные связывать малые молекулы[27][28]. Связывание молекулы влияет на способность рибопереключателя останавливать транскрипцию или препятствовать трансляции. В этом случае важной оказывается не последовательность нуклеотидов как таковая, а наличие комплементарных нуклеотидов на нужных местах в последовательности[4].
Регуляция трансляции также может осуществляться только за счёт образуемой нуклеиновой кислотой вторичной структуры.
- Ро-независимый терминатор транскрипции — шпилька, образующаяся на синтезируемой мРНК до начала трансляции, препятствующая дальнейшему синтезу мРНК (Терминатор (ДНК))[29];
- IRES — сложная структура в мРНК вирусов эукариот, обеспечивающий внутреннюю инициацию трансляции[30].
Зачастую, мотивы, связывающие транскрипционные факторы, имеют вид прямых повторов некоторой последовательности, обратных повторов или палиндромных последовательностей. Это можно объяснить работой транскрипционных факторов в виде димеров белков, в которых каждый из мономеров связывает одну и ту же последовательность. Встречаются также мотивы большей повторности[6]. Такое строение мотивов обеспечивает большую резкость реакции на изменение внешних условий. К примеру, если связывание зависит от концентрации одного вещества в клетке, то получаем зависимость силы реакции клетки, описываемую уравнением Михаэлиса — Ментен. С увеличением числа связывающихся единиц белка (будем считать, что действие связывания белка с мотивом проявляется только в случае связывания со всеми повторами) зависимость всё больше становится похожей на сигмоиду, в пределе стремясь к функции Хевисайда, описывающей один из главных принципов реагирования живых систем на многие воздействия — закон «всё или ничего» (англ. all-or-nothing law)[6], к примеру, формирования потенциала действия[31].
Мотивы в белках
Для белков следует различать
- мотив в последовательности аминокислот
- структурный мотив — взаимное расположение нескольких близко расположенных элементов вторичной структуры в пространстве[2][22]. На последовательности же эти элементы могут далеко отстоять друг от друга[32].
Мотивы в первичной структуре похожи на мотивы в нуклеиновых кислотах. Характерными примерами таковых являются:
- сигнальные пептиды — короткие аминокислотные последовательности в составе белка длиной порядка 3—60 аминокислот[33], определяющие, в какой компартмент клетки будет отправлен после синтеза. Пример — сигнал ядерной локализации;
- сайты посттрансляционной модификации белков, представляющие собой консервативные пептиды порядка 5—12 аминокислот[6]. Пример — сайты ацетилирования в белке[34]
В белках структурные мотивы описывают связи между элементами вторичной структуры. Такие мотивы часто имеют участки переменной длины, которые в некоторых случаях могут и вовсе отсутствовать[22].
- Лейциновая молния — характерен для димерных белков, связывающих ДНК. Лейциновая молния обеспечивает контакт двух мономеров белка за счёт гидрофобных взаимодействий[22][35]. Для него характерно наличие в каждой седьмой позиции остатка лейцина.
- Цинковые пальцы — характерен для ДНК-связывающих факторов транскрипции[22][36];
- Спираль-поворот-спираль — ДНК-связывающий мотив, именно такой ДНК-связывающий фрагмент у Lac-репрессора[22].
- Гомеодомен — мотив, связывающий ДНК и РНК. У эукариот белки с гомеодоменами индуцируют дифференцировку клеток, запуская каскады генов, необходимых для образования тканей и органов. Похож на мотив «спираль-поворот-спираль», потому часто отдельно не выделяется[22][37].
- Укладка Россмана — мотив, связывающий нуклеотиды (к примеру — НАД)[38]. Встречается, в частности, в дегидрогеназах, в том числе в глицеральдегид-3-фосфатдегидрогеназе, участвующей в гликолизе.
- EF-рука — мотив, связывающий ионы Са2+, также подобен мотиву «спираль-поворот-спираль»[39].
- Гнездо — три последовательных аминокислотных остатка формируют сайт связывания аниона[40].
- Ниша — три последовательных аминокислотных остатка формируют сайт связывания катиона[41].
- Бета-шпилька — два β-тяжа, соединённых коротким разворотом цепи белка[42].
Кроме бета-шпильки выделяют и множество других мотивов, функция которых состоит в формировании структурного каркаса белка[43].
Близким к термину структурный мотив белка является укладка — характерное расположение элементов вторичной структуры. В силу своей схожести термины часто используются один вместо другого и грань между ними размыта[43][44].
Представление мотивов
Изначально имеется набор мотивов из разных последовательностей и ставится задача[2]:
- представить их компактно и наглядно;
- уметь по представлению мотива осуществлять поиск его новых вхождений.
Существует несколько общепризнанных способов представления мотивов[45]. Часть из них подходит как для белков, так и для нуклеотидов, другая часть — только для белков или нуклеотидов.
Строгим консенсусом мотива назовем строчку, состоящую из самых представленных букв в множестве реализаций мотива. На практике, указывается не просто наиболее частая буква в данной позиции, но и, если максимальная частота встречаемости какой-либо буквы в данной позиции меньше заданного порога, то на этом месте в консенсусе ставится x (любая буква алфавита). По такому консенсусу мы почти наверняка находим последовательности, реально являющиеся мотивами, но упускаем большое число мотивов, отличающихся от консенсуса на несколько замен[2][4][9]. Ниже приведён пример строгого консенсуса для участка мотива пяти взятых из UniProt белков с мотивом лейциновой молнии (порог был взят равным 80 %):
| Номер позиции | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| UniProt ID | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| O35048 | L | S | P | C | G | L | R | L | I | G | A | H | P | I | L |
| Q6XXX9 | L | G | Q | D | I | C | D | L | F | I | A | L | D | V | L |
| Q9N298 | L | G | Q | V | T | C | D | L | F | I | A | L | D | V | L |
| Q61247 | L | S | P | L | S | V | A | L | A | L | S | H | L | A | L |
| B0BC06 | L | T | I | G | Q | Y | S | L | Y | A | I | D | G | T | L |
| Консенсус | L | x | x | x | x | x | x | L | x | x | x | x | x | x | L |
Нестрогим консенсусом назовем последовательность списков букв, наиболее представленных на соответствующем месте. Описываются все или наиболее часто встречающиеся буквы в данной позиции (обычно устанавливается минимальный порог частоты)[2]. Фактически, мотив описывается при помощи регулярного выражения[4][9]. В качестве обозначений используют:
- Алфавит — совокупность отдельных символов, обозначающих определённую аминокислоту/нуклеотид или набор аминокислот/нуклеотидов;
ABC— строка из символов алфавита, обозначающая последовательность символов, следующих друг за другом;[ABC]— любая строка символов, взятых из алфавита в квадратных скобках соответствует любому из соответствующих символов; например [ABC] соответствует или A или B или C;{ABC..DE}— любая строка символов, взятых из алфавита, соответствует любой аминокислоте, кроме тех, что находятся в фигурных скобках; например{ABC}соответствует любой аминокислоте, кромеA,BиC;xв нижнем регистре — любой символ алфавита.
В случае с таким представлением приходится балансировать между чувствительностью консенсуса (количеством реальных мотивов, которые им получится отыскать) и специфичностью (способностью метода отбраковывать мусорные последовательности)[1]. Ниже приведен пример нестрого консенсуса для тех же пяти последовательностей белков, что и для строго консенсуса (порог был взят равным 20 %). Видим, что в позиции 10 мотив не совсем объективен — лейцин (L) и изолейцин (I) — очень близкие по свойствам аминокислоты, и логично было бы их обе занести в консенсус.
| Номер позиции | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| UniProt ID | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| O35048 | L | S | P | C | G | L | R | L | I | G | A | H | P | I | L |
| Q6XXX9 | L | G | Q | D | I | C | D | L | F | I | A | L | D | V | L |
| Q9N298 | L | G | Q | V | T | C | D | L | F | I | A | L | D | V | L |
| Q61247 | L | S | P | L | S | V | A | L | A | L | S | H | L | A | L |
| B0BC06 | L | T | I | G | Q | Y | S | L | Y | A | I | D | G | T | L |
| Консенсус | L | [SG] | [PQ] | x | x | C | D | L | F | I | A | [LH] | D | V | L |
PROSITE использует ИЮПАК для обозначения однобуквенных кодов аминокислот, за исключением символа конкатенации «-», используемого между элементами паттерна. При использовании PROSITE добавляется несколько символов, облегчающих представление белкового мотива[46]:
- '
<' — шаблон ограничивается N-концом последовательности; - '
>' — шаблон ограничивается C-концом последовательности;
Если e — шаблон элемента, и m и n два десятичных целых числа и m <= n, то:
e(m)эквивалентно повторениюeровноmраз;e(m,n)эквивалентно повторениюeровноkраз для любого целогоkудовлетворяющего условию:m<=k<=n;
Пример: мотив домена с сигнатурой C2H2-type цинкового пальца выглядит следующим образом: C-x(2,4)-C-x(3)-[LIVMFYWC]-x(8)-H-x(3,5)-H[47]
Позиционной весовой матрицей называется такая матрица, столбцы которой соответствуют позиции в последовательности, а строчки соответствуют буквам в алфавите. Значениями этой матрицы являются частоты (или монотонные функции от частот) встречаемости данной буквы в данной позиции на последовательности. При этом обычно, чтобы исключить нулевые частоты к числу встреч каждой буквы позиции добавляют некоторое число, исходя из априорного распределения букв в подобных последовательностях[4] (к примеру, вводят поправку Лапласа[48]). Данный подход, как и предыдущие, неявно предполагает, что позиции в мотиве независимы, чего на самом деле не наблюдается даже для нуклеотидных последовательностей[2][4].
Пусть у нас есть 7 последовательностей ДНК, представляющих собой мотив[9]:
| Номер позиции | ||||||||
|---|---|---|---|---|---|---|---|---|
| Номер
последовательности |
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 1 | A | T | C | C | A | G | C | T |
| 2 | G | G | G | C | A | A | C | T |
| 3 | A | T | G | G | A | T | C | T |
| 4 | A | A | G | C | A | A | C | C |
| 5 | T | T | G | G | A | A | C | T |
| 6 | A | T | G | C | C | A | T | T |
| 7 | A | T | G | G | C | A | C | T |
Позиционная матрица для них будет иметь следующий вид (+1 — учёт правила Лапласа)[9]:
| Номер позиции | ||||||||
|---|---|---|---|---|---|---|---|---|
| Нуклеотид | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| A | 5 + 1 | 1 + 1 | 0 + 1 | 0 + 1 | 5 + 1 | 5 + 1 | 0 + 1 | 0 + 1 |
| C | 1 + 1 | 0 + 1 | 1 + 1 | 4 + 1 | 2 + 1 | 0 + 1 | 6 + 1 | 1 + 1 |
| G | 0 + 1 | 1 + 1 | 6 + 1 | 3 + 1 | 0 + 1 | 1 + 1 | 0 + 1 | 0 + 1 |
| T | 1 + 1 | 5 + 1 | 0 + 1 | 0 + 1 | 0 + 1 | 1 + 1 | 1 + 1 | 6 + 1 |
Частоты можно пронормировать на общее число последовательность, тем самым получив оценку вероятности встречи данного нуклеотида в данной последовательности (собственно, обычно в таком представлении и хранится PWM)[2]:
| Номер позиции | ||||||||
|---|---|---|---|---|---|---|---|---|
| Нуклеотид | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| A | 0,55 | 0,18 | 0,09 | 0,09 | 0,55 | 0,55 | 0,09 | 0,09 |
| C | 0,18 | 0,09 | 0,18 | 0,45 | 0,27 | 0,09 | 0,64 | 0,18 |
| G | 0,09 | 0,18 | 0,64 | 0,36 | 0,09 | 0,18 | 0,09 | 0,09 |
| T | 0,18 | 0,55 | 0,09 | 0,09 | 0,09 | 0,18 | 0,18 | 0,64 |
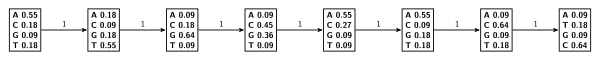
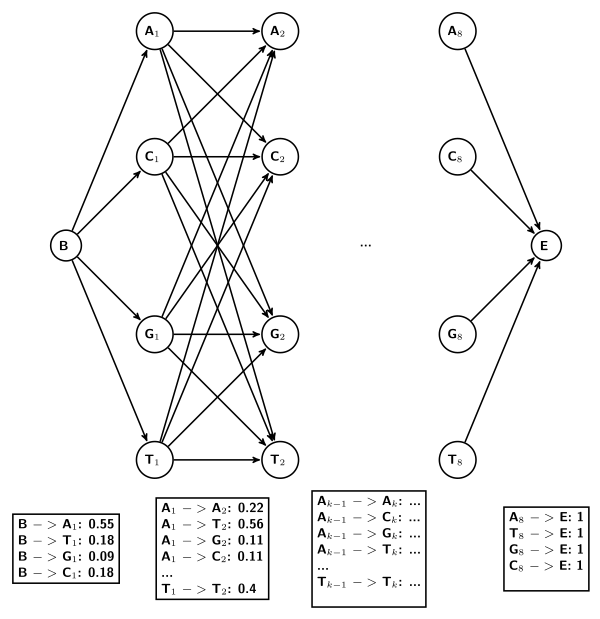
Для большей точности можно учитывать зависимость соседних позиций в мотиве с помощью скрытых марковских моделей первого и более высоких порядков[2][4]. Этот подход сопряжён с некоторыми трудностями, так как для его применения необходимо наличие достаточно представительной выборки вариантов мотивов. В случае предыдущего примера имеем:
- Для марковской модели порядка 0 (вероятность появления нуклеотида в данной позиции от других позиций не зависит — другой способ трактовки PWM)[4];
- Для марковской модели порядка 1 (вероятность появления нуклеотида в данной позиции зависит только от нуклеотида в предыдущей последовательности. Легко заметить, что число параметров модели сильно возросло)[4]. При расчете вероятностей перехода также использовалось правило Лапласа. Эмисионные вероятности для состояний равны 1 для нуклеотидов, которым они соответствуют, 0 — для остальных.
В случае мотивов, содержащих участки переменного размера и нуклеотидного состава, можно было бы вводить отдельно модель для этих участков, отдельно — для консервативных, а затем «склеивать» их в одну модель путём добавления промежуточных «молчащих» состояний и вероятностей перехода в них и из них[4].
В случае мотивов, формирующих вторичные структуры (РНК-переключатели) в РНК, в элементах вторичной структуры важно учитывать возможность спаривания нуклеотидов. С этой задачей справляются СКС. Однако обучение СКС требует ещё большего размера выборки, чем HMM, и сопряжено с рядом трудностей[4].
В тех случаях, когда важна скорость поиска и допустим пропуск некоторых вхождений нашего мотива, исследователи прибегают к различным уловкам, позволяющим с приемлемой точностью зашифровать пространственную структур биополимера (РНК или белка) путём расширения алфавита[49].
Оперон Escherichia coli репрессор лактозы LacI (PDB 1lcc chain A) и ген активатор катаболизма (PDB 3gap chain A) оба имеют мотив спираль-поворот-спираль, но их аминокислотные последовательности не очень схожи. Группой исследователей был разработан код, который они назвали «трёхмерный код цепи», представляющий структуру белка в виде строки из писем. Эта схема кодирования, по мнению авторов, показывает сходство между белками гораздо более отчётливо, чем аминокислотные последовательности[49]:
Пример: сравнение двух упомянутых выше белков при помощи этой схемы кодирования[49]:
| PDB ID | 3D-code | Amino acid sequence |
|---|---|---|
1lccA
|
TWWWWWWWKCLKWWWWWWG
|
LYDVAEYAGVSYQTVSRVV
|
3gapA
|
KWWWWWWGKCFKWWWWWWW
|
RQEIGQIVGCSRETVGRIL
|
| Сравнение | Видно явное сходство между белками | По аминокислотной последовательности белки сильно отличаются |
где W соответствует α-спирали, и E и D соответствует β-нити.
В данной работе с целью применения алгоритма поиска, схожего с BLAST, нуклеотидный алфавит (ATGC, так как поиск осуществлялся в геноме) был расширен за счёт комбинирования нуклеотидов и трех символов, характеризующих их предположительное направление спаривания[50]:
(— нуклеотид спарен с нуклеотидом справа;)— нуклеотид спарен с нуклеотидом слева;.— нуклеотид не спарен.
Таким образом получалось 12 букв нового алфавита (4 нуклеотида * 3 «направления»), при правильном использовании позволяющий осуществлять BLAST-подобный поиск, названный авторами foldedBlast[50].
Для визуального представления мотивов часто используют логотип последовательностей — графического представления консервативности каждой позиции в мотиве. При этом данную визуализацию можно успешно применять как и в случае представления мотива в виде консенсуса или позиционной весовой матрицы, так и для представления HMM модели последовательности, как это сделано в базе белковых семейств Pfam[51].
Кроме того, если использовать, к примеру, яркость каждой нуклеотида в мотиве как индикатор того, насколько часто ему соответствует в этом же мотиве комплементарный нуклеотид, то можно частично представлять и информацию о вторичной структуре мотива. Так сделано, например, в биоинформатическом веб-сервисе RegPredict[52].
Поиск сайтов связывания транскрипционных факторов in silico
В случае поиска в нуклеотидных последовательностях мотивов, отвечающих за связывание регуляторных белков пользуются соображением, что они [мотивы] меняются сравнительно медленно, а значит, если взять организмы, достаточно далёкие друг от друга, чтобы в высоковариабельных позициях их последовательностей успели накопиться мутации, а сайты измениться сильно ещё не успели, то можно пользоваться правилом «что консервативно — то важно»[2]. После получения последовательностей, в которых предполагается наличия специфичного мотива, в основном используют два подхода к поиску последовательности мотива — филогенетический футпринтинг и сведение задачи к задаче поиска вставленного мотива.
Филогенетический футпринтинг — полуавтоматический метод. Последовательности обрабатываются программой множественного выравнивания, и в получившемся выравнивании исследователем ищутся паттерны, которые можно считать мотивами. Одним из наиболее успешных примеров применения данного подхода можно считать расшифровку способа кодирования нерибосомных пептидов нерибосомными пептид-синтетазами (NRPS)[2][53][54]. Данный метод не позволяет полностью автоматизировать процесс поиска мотивов, но при этом и не имеет столь сильных ограничений, как следующие.
В случае с мотивами без (почти без) разрывов и без (почти без) участков переменной длины возможно свести задачу поиска мотива к задаче поиска вставленного мотива (англ. Planted motif search)[2][9].
Формулировка задачи следующая: «На вход предоставлены n строк s1, s2, …, sn длины m, каждая составленная из символов алфавита A, и два числа — l и d. Найдите все строки x длины l такие, что любая из предоставленных строки содержит хотя бы одну подпоследовательность, находящуюся от x на расстоянии Хэмминга не больше d»[55].
Так как в общем случае неизвестно, все ли полученные нами последовательности имеют искомый мотив, а также неизвестна его точная длина, то обычно задачу решают эвристическими методами — максимизируя вероятность найденного мотива при данных последовательностях. На этом принципе построены программы MEME[17] и GibbsSampler[56].
Если задать минимальный порог на число последовательностей, в которых должен содержаться мотив, и как-либо ограничить его длину, то можно использовать и точные способы решения данной задачи, к примеру — алгоритм RISOTTO[57]. Некоторые из них позволяют снимать часть ограничений на искомый мотив — в RISOTTO искомый мотив может иметь разрывы, состоять из нескольких частей.
Однако эти методы редко дают результаты лучше, чем MEME и GibbsSamler, а работают они значительно дольше[2][58].
Поиск сайтов связывания in vitro
Метод анализа ДНК-белковых взаимодействий, комбинирующий идеи иммунопреципитации хроматина (ChIP) и высокоэффективном секвенировании ДНК (белок пришивается к ДНК, затем кусочки ДНК, пришившиеся к белку отправляются на секвенирование). В ходе работы метода получаются участки длиной около 150 нуклеотидов, которые затем можно анализировать in silico на наличие мотива[59].
Как и в случае использования метода ChIP-seq проводится иммунопреципитации хроматина (ChIP), затем сшивка с белком обращается и полученная ДНК гибридизуется с ДНК-микрочипом. Метод ChIP-on-chip дешевле, чем ChIP-seq, однако сильно уступает последнему в точности[6].
Также метод, основанный на иммунопреципитации хроматина (ChIP). Использование экзонуклеазы фага λ, деградирующей ДНК только с 5'-конца и только в случае отсутствия контакта с белком, позволяет добиваться точности порядка нескольких нуклеотидов в определении положения сайта связывания белка[60].
Итеративный метод поиска нуклеотидных последовательностей, хорошо связывающихся с данным белком[61]. Процедура в общем случае выглядит так:
- Интересующий нас белок пришивается к колонке, через которую далее пропускается раствор с набором последовательностей, состоящих из рандомизированного участка и адаптера;
- Последовательности, задержавшиеся на колонке клонируют процедуре ПЦР, причем состав реакционной смеси подобран таким образом, чтобы вносить дополнительные ошибки при копировании. Полученные клоны отправляются на новый раунд SELEX;
- Через каждые несколько участков условия (pH раствора, его ионная сила) ужесточаются, чтобы на колонке оставались все более и более специфичные к белку последовательности;
- Получающиеся на выходе последовательности часто похожи на реальные мотивы связывания белка в живых организмах.
Делается гибридный белок из изучаемого белка и адениновой ДНК-метилтрансферазы Dam[62]. В естественных условиях аденин в большинстве эукариот не метилируется. Когда же гибридный белок связывается с каким-либо сайтом в ДНК организма, метилтрансферазная часть модифицирует аденины в районе этого сайта, что позволяет затем с помощью эндонуклеаз рестрикции выделить участок, на котором с большой долей вероятности находится искомый мотив.
Примечания
Литература
- Дурбин Р., Эдди Ш., Крог А., Митчисон Г. Анализ биологических последовательностей = Biological Sequence Analysis: Probabilistic Models of Proteins and Nucleic Acids. — Регулярная и хаотическая динамика, Институт компьютерных исследований, 2006. — С. 480. — ISBN 5939725597.
- Jones Neil C., Pevzner Pavel A. An Introduction to Bioinformatics Algorithms (англ.). — The MIT Press, 2004. — ISBN 9780262101066.
- Compeau Phillip, Pevzner Pavel. Bioinformatics Algorithms: An Active Learning Approach, 2nd Ed. Vol. 1 by Phillip Compeau (англ.). — Active Learning Publishers, 2015. — P. 384. — ISBN 9780990374619.
- Durbin Richard, Eddy Sean R., Krogh Anders, Mitchison Graeme. Biological Sequence Analysis: Probabilistic Models of Proteins and Nucleic Acids (англ.). — Cambridge University Press, 1998. — P. 372. — ISBN 978-0521620413.
- Nelson David L., Cox Michael M. Lehninger Principles of Biochemistry (англ.). — W. H. Freeman, 2017. — P. 1328. — ISBN 9781464126116.
Ссылки
- Находим скрытые в ДНК сообщения — часть курса по биоинформатике от всемирно известного учёного П. А. Певзнера
- MEME Suite of motif-based sequence analysis tools — сервис для поиска мотивов в последовательностях одноимённым алгоритмом MEME
- The Gibbs Motif Sampler — сервис для поиска мотивов в последовательностях алгоритмом Gibbs Sampler
- RISOTTO motif discovery tool — главная страница программы для точного поиска мотивов RISOTTO
- PMS — точный поиск мотивов при помощи алгоритмов семейства PMS
- Bioprospector — поиск мотивов в последовательностях алгоритмом Gibbs Sampler
- XXmotif — сервис для поиск мотивов в нуклеотидных последовательностях на основании прямой оптимизации статистической значимости PWM
- PROSITE — база данных белковых семейств и доменов
- TRANSFAC — коммерческая (ограниченный публичный доступ) база данных транскрипционных факторов
- HOCOMOCO Архивная копия от 6 июня 2013 на Wayback Machine — коллекция траскрипционных факторов человека и мыши
- Minimotif Miner — поиск коротких известных мотивов
- Wikiomic Sequence motifs page — статья о мотивах в последовательностях
- Cis-analysis — список и короткие описания части программ поиска мотивов в последовательностях