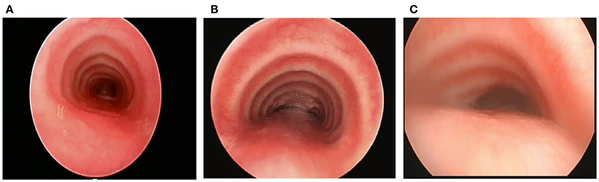
Трахеомаляция
Трахеомаля́ция (лат. tracheomalacia)— это размягчение стенок трахеи из-за аномалий хрящевых полуколец и снижения эластичности мышц. Трахеомаляция может затрагивать часть трахеи или даже всю трахею. Это приводит к сужению просвета дыхательных путей, особенно при выдохе, что может вызывать трудности с дыханием, хрипы, кашель и рецидивирующие инфекции дыхательных путей. Золотым стандартом диагностики является бронхоскопия, которая позволяет визуально оценить податливость стенок трахеи[1]. Лечение лёгкой степени трахеомаляции может быть консервативным, тогда как тяжёлые случаи требуют хирургического лечения. В хирургическом лечении трахеомаляции применяют аортопексию, трахеопексию, резекцию трахеи с анастомозом, использование стентов[2]. При слабо выраженной симптоматике прогноз для пациентов в целом благоприятный[3].
Что важно знать
История
Впервые эту патологию описал в 1949 году J. Lemoine и назвал «ретракция трахеи и бронхов»[4].
Классификация
Выделяют две основные формы трахеомаляции:
- Врождённая трахеомаляция — развивается из-за нарушений формирования трахеальных хрящей во внутриутробном периоде. Может быть изолированной или сочетаться с другими аномалиями, такими как врождённые пороки сердца, атрезия пищевода, трахеопищеводный свищ и др.
- Приобретённая трахеомаляция — возникает вследствие травм, длительной интубации, компрессии трахеи опухолями или сосудистыми структурами, а также при хронических воспалительных заболеваниях.
Также трахеомаляцию делят по степени тяжести (лёгкая, средняя, тяжёлая) и локализации поражения (цервикальная, грудная часть трахеи или диффузная форма)[3].
Этиология
Причинами врождённой трахеомаляции могут являться:
- синдром Элерса — Данлоса;
- бронхолёгочная дисплазия;
- атрезия пищевода со свищем;
- сосудистые кольца;
- правая дуга аорты;
- левостороннее отхождение (правой) безымянной артерии;
- правостороннее отхождение левой общей сонной артерии;
- аномальное отхождение левой лёгочной артерии от правой лёгочной артерии;
- синдромом Мунье — Куна (причина врождённой трахеомаляции у взрослых)
- полихондрит[3][5]
Причинами приобретённой трахеомаляции могут являться:
- длительная трахеостомия;
- длительная интубация;
- травма грудной клетки;
- хронический трахеобронхит;
- рецидивирующий полихондрит;
- эмфизема;
- хронический бронхит;
- хроническое наружное сдавливание трахеи (злокачественные и доброкачественные опухоли, кисты, абсцессы, аневризма аорты);
- бронхоэктатическая болезнь;
- ХОБЛ;
- цилиндрома;
- дилатационная кардиомиопатия[3][5].
Патогенез
Хрящевые полукольца трахеи в норме обеспечивают жёсткость стенки, а задняя стенка является перепончатой (мембранозной). Патологические изменения нарушают опорную структуру хрящевых колец, вызывая сужение просвета трахеи в переднезаднем направлении и выпячивание задней стенки. Хотя физиологическое спадание трахеи на выдохе (до 30 % от своего диаметра у младенцев при форсированном выдохе) допустимо, коллапс более 50 % диаметра расценивается как трахеомаляция, нарушающая вентиляцию лёгких[3]. Трахеомаляция чаще всего поражает дистальную треть трахеи[5].
Врождённая форма заболевания обусловлена аномалией развития хрящевых колец, что вызывает избыточную растяжимость стенки, её уплощение и выпячивание мембранозной части в просвет с динамическим коллабированием при дыхании. При трахеобронхомаляции у детей хрящ теряет способность противостоять повышению внутригрудного давления на выдохе, что ведёт к коллапсу дыхательных путей. Это усугубляется при форсированном дыхании, кашле, а также внешней компрессией со стороны сосудов или пищевода[1][6].
Эпидемиология
Диагностика
Выраженность клинической картины при трахеомаляции зависит от локализации и степени сужения трахеи. Основными проявлениями являются свистящее дыхание (стридор, особенно на выдохе), лающий кашель, затруднённое дыхание, а также склонность к частым и затяжным респираторным инфекциям, таким как рецидивирующие бронхиты и пневмонии. Значительное сужение дыхательных путей может привести к неэффективному кашлю и снижению отхождения мокроты. Может наблюдаться втяжение надключичных и межрёберных промежутков при вдохе. В тяжёлых случаях может развиваться дыхательная недостаточность с непереносимостью нагрузки, эпизодами гипоксии, цианоза и апноэ. Также могут отмечаться охриплость голоса и проблемы с кормлением. Симптомы часто манифестируют у детей в возрасте 2-3 месяцев, хотя при обширном поражении могут проявляться с рождения. Характерно усиление симптоматики при любых действиях, повышающих внутригрудное давление: при кашле, плаче, кормлении, натуживании или в положении лёжа на спине, а также на фоне респираторных инфекций[5][7].
Специфических изменений нет.
Основные методы диагностики:
- Бронхоскопия — является «золотым стандартом» для визуальной оценки податливости стенок трахеи. Бронхоскопию следует проводить под местной анестезией, чтобы убедиться, что ребёнок дышит спонтанно и имеет необходимый кашлевой рефлекс для визуализации размягчения стенок трахеи во время кашля или глубокого выдоха — важный признак, который невозможно наблюдать при спокойном дыхании[1].
- Компьютерная томография (КТ) с мультипланарной реконструкцией. КТ позволяет быстро оценить состояние дыхательных путей. Тем не менее, КТ связана с облучением, и у маленьких детей для этого может потребоваться седативный эффект, который может изменить динамику дыхания[3].
- Функциональные дыхательные тесты — могут показать обструктивные изменения. Результаты спирометрии не демонстрируют значимой корреляции с бронхоскопическими признаками трахеомаляции. Однако было обнаружено, что у пациентов с трахеобронхомаляцией показатель объёмной скорости выдоха достоверно снижен по сравнению с детьми, у которых поражение ограничено только трахеей[8].
Дифференциальная диагностика
Дифференциальная диагностика трахеомаляции включает в себя:
- ларингомаляцию;
- подсвязочный стеноз;
- врождённые кисты;
- паралич голосовых связок;
- гипокальциемическую тетанию;
- бронхиальную астму[5].
Осложнения
- обструкция дыхательных путей;
- дыхательная недостаточность;
- хроническая гипоксия;
- рецидивирующие респираторные инфекции;
- задержка развития[3].
Лечение
Выбор лечения зависит от степени тяжести заболевания.
При лёгкой степени трахеомаляции предпочтение отдаётся консервативному лечению, так как состояние большинства детей улучшается к возрасту 18-24 месяцев. Терапия включает увлажнение воздуха, постуральный дренаж и вибрационный массаж грудной клетки, осторожное кормление, а также своевременное лечение инфекций дыхательных путей. Для пациентов с признаками дыхательной недостаточности может применяться респираторная поддержка методом постоянного положительного давления в дыхательных путях (CPAP), особенно в качестве краткосрочной меры[5]. У взрослых бессимптомная трахеомаляция, выявленная случайно, также требует консервативного подхода. При неэффективности базовой терапии может применяться CPAP. Основой медикаментозного лечения является поддержание мукоцилиарного клиренса, поскольку коллапс дыхательных путей нарушает нормальный механизм отхождения слизи. Для этого назначают ипратропия бромид (сокращает объём мокроты без её сгущения), ингаляции гипертонического физиологического раствора для разжижения секрета и улучшения отхождения мокроты[3][7]. При этом следует избегать длительного или бесконтрольного применения глюкокортикостероидов из-за риска разрушения хрящевой ткани и прогрессирующей трахеомаляции, развития синдрома Кушинга и надпочечниковой недостаточности. Эффективность бронходилататоров и М-холиномиметиков при трахеомаляции изучена недостаточно. Бета-агонисты могут даже ухудшить состояние, снижая тонус гладкой мускулатуры трахеи и усиливая выпячивание её задней мембраны в просвет[7].
Показаниями к хирургическому лечению служат неэффективность консервативной терапии, рецидивирующая пневмония, периодическая обструкция дыхательных путей, рефлекторное апноэ, невозможность экстубации, отставание в развитии, эпизоды цианоза[1][3].
В хирургическом лечении трахеомаляции применяются различные методы, включая аортопексию, трахеопексию, резекцию трахеи с анастомозом, использование стентов. Наиболее распространённой является передняя аортопексия, при которой восходящая аорта фиксируется к грудине. Однако в 10-25 % случаев эта процедура не даёт ожидаемого эффекта. Более новой методикой является задняя трахеопексия — это фиксация мембранозной части трахеи к передней продольной связке позвоночника. Первоначально она применялась для профилактики рецидива трахеопищеводной фистулы при атрезии пищевода, но также показала эффективность при трахеомаляции. Однако у части пациентов сохраняющаяся трахеомаляция может приводить к развитию необратимых бронхоэктазов к 8-летнему возрасту. Поэтому задняя трахеопексия может быть безопасно проведена во время первоначальной реконструкции атрезии пищевода без дополнительного риска осложнений и увеличения длительности операции[2].
Альтернативным методом является стентирование дыхательных путей — это менее инвазивное вмешательство, сокращающее время восстановления после операции. Оно предотвращает коллапс трахеи, но преимущественно применимо при локализованных поражениях, так как установка стентов во все отделы дыхательных путей при диффузном процессе невозможна. Используются металлические стенты, устанавливаемые с помощью гибкой бронхоскопии, и силиконовые, требующие жёсткой бронхоскопии и общей анестезии. Хотя стентирование часто даёт кратковременное улучшение, его продолжительность непредсказуема, а возможные осложнения включают образование грануляционной ткани, гиперплазию слизистой оболочки, обструкцию или перфорацию дыхательных путей. Если пациент хорошо переносит стентирование, это может быть этапом перед радикальной операцией, например трахеобронхопластикой[1][3]. Стенты у детей имеют ограниченное применение из-за риска смещения, перелома, эрозии, грануляций и необходимости замены по мере роста[7].
У пациентов с короткими сегментарными поражениями можно рассмотреть возможность резекции трахеи и наложения анастомоза[3]. Резекция трахеи с анастомозом применяется редко, поскольку врождённые аномалии редко затрагивают короткий сегмент. Резекция трахеи с наложением анастомоза «конец в конец» или в виде скользящей трахеопластики может быть показана пациентам с некоторыми видами врождённой аномалии трахеи, такими как врождённое отсутствие хряща или его серьёзная деформация[7].
Для приобретённой трахеомаляции у взрослых, особенно на фоне ХОБЛ, первично лечат основное заболевание. При неэффективности консервативных мер могут применяться неинвазивная вентиляция с положительным давлением, чтобы обеспечить проходимость дыхательных путей и облегчить отхождение мокроты, хирургическая пластика задней стенки трахеи (например, с использованием полипропиленовой сетки) или трахеостомия[5].
Трахеостомия сопряжена с рисками, особенно у маленьких детей, поскольку требует регулярной замены трубки по мере роста пациента. Трахеостомическая трубка может не обеспечивать поддержку дистального отдела трахеи и не предотвращает коллапс дыхательных путей ниже её конца. К возможным осложнениям относятся повреждение трахеи, образование грануляционной ткани, стеноз, трахеоартериального или трахеопищеводного свища, закупорка просвета, случайная декануляция, задержка речевого развития, а также трудности при окончательном удалении канюли. Кроме того, наличие трахеостомы может привести к развитию вторичной трахеомы и фиброза трахеи[7].
Прогноз
Для пациентов с врождённой трахеомаляцией и слабо выраженными симптомами прогноз, как правило, благоприятный: клинические проявления обычно регрессируют к двум годам. Если заболевание сопровождается другими патологиями, симптомы могут сохраняться. В тех случаях, когда симптомы сохраняются у взрослых, часто отмечается непереносимость физических нагрузок. При вторичной трахеомаляции прогноз определяется характером и тяжестью основного заболевания, вызвавшего изменения трахеи[3].
Диспансерное наблюдение
Индивидуально.
Профилактика
В качестве профилактики респираторных осложнений необходимо проводить вакцинацию в соответствии с возрастом. Профилактика ГЭР, особые режимы кормления необходимы, чтобы избежать аспирации и обеспечить адекватный рост и развитие ребёнка[3].