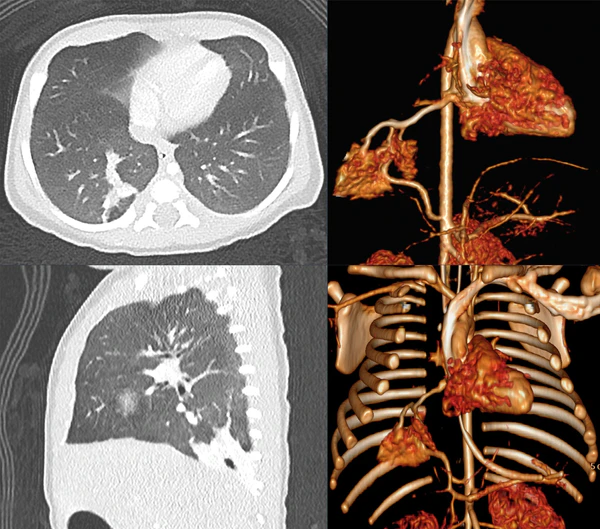
Лёгочная секвестрация
Лёгочная секвестрация (ЛС) — это порок развития, при котором патологический участок лёгочной ткани, частично или полностью отделившийся на ранних стадиях эмбриогенеза от основного лёгкого, развивается самостоятельно и имеет отдельное кровоснабжение аномальной артерией, отходящей от аорты или её ветвей[1]. Клинически ЛС может протекать бессимптомно и стать случайной находкой при проведении рентгенологических исследований[2].
Что важно знать
Классификация
Выделяют 2 основные формы секвестрации лёгкого:
- Интралобарная ЛС (внутридолевая). При данном варианте порока патологический процесс локализуется внутри лёгочной ткани и окружён нормально развитой тканью. Эта форма встречается наиболее часто, составляя 75-86 % всех случаев секвестрации. Около 2/3 интралобарных секвестров локализуются в заднем базальном сегменте нижней доли левого лёгкого. Однако при синдроме Ятагана (частичное аномальное соединение лёгочных вен) чаще поражается правое лёгкое[3][4][2]. Кровоснабжение обычно обеспечивается ветвями грудной или брюшной части аорты. Гораздо реже кровь поступает через ветви подключичной, безымянной, лёгочной или венечной артерии[5].
- Экстралобарная ЛС (внедолевая) характеризуется расположением аномального участка вне лёгочной ткани, как внутри, так и снаружи от висцеральной плевры. На этот вариант приходится 14-25 % от всех случаев ЛС. Такие секвестры могут находиться как в грудной полости (чаще между диафрагмой и нижней долей лёгкого), так и в брюшной полости. Венозный дренаж осуществляется в системные вены, часто в нижнюю долевую вену, непарную вену или полунепарную вену. При общей преобладающей встречаемости ЛС у мужчин, внутрибрюшные экстралобарные формы в 75 % случаев обнаруживаются у женщин, преимущественно в левой забрюшинной области[3][4][2]. Кровоснабжение экстралобарного секвестра осуществляется преимущественно через ветви грудного или брюшного отделов аорты, ветвями других артерий большого круга кровообращения или через лёгочную артерию. Эта форма отличается большим разнообразием возможных локализаций и источников кровоснабжения по сравнению с интралобарным вариантом[5].
Этиология
Лёгочные секвестры формируются из добавочного лёгочного зачатка, расположенного ниже нормального зачатка лёгкого. Точные причины развития не выяснены[6].
Патогенез
Развитие ЛС связано с эмбриогенезом дыхательной системы, когда примитивное бронхиальное дерево развивается как вентральный дивертикул передней кишки на 3-й неделе гестации, который разделяется на правый и левый лёгочные зачатки к 26-му дню, а между 5-й и 8-й неделями происходит формирование лёгочных долей. Возникновение ЛС вероятно, происходит в период с 4-й по 8-ю неделю гестации. При этом раннее нарушение развития (до 6-й недели) может сопровождаться сопутствующими аномалиями, такими как врождённая диафрагмальная грыжа, что подтверждает ранний срок формирования дефекта[6].
Ткань добавочного лёгочного зачатка мигрирует вместе с нормально развивающимся лёгким, но получает кровоснабжение не из лёгочных артерий, а из системных сосудов, отходящих от аорты. В зависимости от времени возникновения аномалии формируются разные типы секвестрации: если нарушение происходит рано, развивается интралобарный вариант, а при более позднем отклонении — экстралобарный вариант[3].
Эпидемиология
Клиническая картина
Интралобарная ЛС часто протекает бессимптомно. Помимо бессимптомного течения, заболевание может проявляться рецидивирующей пневмонией в локализованном сегменте лёгкого. При инфицировании в ЛС происходит нагноение кист, расплавление стенок, формируется связь с нормально развитым бронхиальным деревом, что проявляется в виде усиления кашля и изменения его характера на гнойный, могут наблюдаться эпизоды кровохарканья, в тяжёлых случаях ЛС манифестирует ургентно при формировании альвеолярного кровотечения либо гемоторакса. В ряде случаев ЛС является причиной сепсиса[2]. Также может наблюдаться боль в спине или постоянная одышка при физической нагрузке[4][2].
Экстралобарная ЛС может проявляться уже в периоде новорождённости. При значительном размере проявляется в виде:
- дыхательной недостаточности
- застойной сердечной недостаточности с высоким сердечным выбросом (из-за право-левого шунта)
- периодических спонтанных лёгочных или плевральных кровотечений.
Экстралобарные секвестры реже инфицируются, чаще сочетаются с другими врождёнными пороками такими, как врождённая диафрагмальная грыжа, врождённая кистозная аденоматоидная мальформация, пороки опорно-двигательной системы, врождённый порок сердца, трахеопищеводный свищ, гипоплазия лёгких, бронхогенная киста и врождённый мегаколон[4][8][2].
Диагностика
Пренатальная диагностика ЛС возможна на 12-й нед. беременности, но наиболее информативным периодом является 18-20 неделя гестации. При УЗИ с допплерографией секвестр определяется как гиперэхогенное образование, а при МРТ — как зона повышенной интенсивности сигнала на Т2-взвешенных изображениях. Характерной особенностью данных образований является их динамический рост с 20 по 26 неделю беременности с последующей стабилизацией размеров к 28 неделе. В третьем триместре в 50 % случаев наблюдается значительное уменьшение объёма патологической ткани, что иногда ошибочно интерпретируется как полный регресс. Однако истинное исчезновение образования встречается крайне редко. Важно отметить, что кажущееся исчезновение секвестра может быть связано как с его реальным уменьшением, так и с техническими сложностями визуализации на фоне возрастного повышения эхогенности лёгочной ткани плода. В связи с этим всем пациентам с выявленными изменениями рекомендуется обязательное динамическое наблюдение в постнатальном периоде[4][9] .
- Рентгенография органов грудной клетки — позволяет определить характерные изменения паренхимы при интралобарной ЛС. Патология визуализируется как чётко очерченное треугольное образование, расположенное в базальных сегментах лёгких. Однако стоит учитывать, что многие интралобарные ЛС имеют мелкие размеры и остаются незамеченными.
- УЗИ служит важным методом диагностики внелёгочной секвестрации у детей, особенно при локализации образований в забрюшинном пространстве. Секвестр определяется как гиперэхогенное образование. Особую диагностическую ценность представляет допплеровское исследование, позволяющее выявить характерные питающие артерии (обычно отходящие от аорты) и дренирующие вены, что является ключевым критерием для подтверждения диагноза.
- КТ — метод выбора для диагностики ЛС, позволяет оценить не только приводящие артериальные сосуды, но и отводящие венозные, что важно для дифференциальной диагностики между интра- и экстралобарной формами секвестрации
- МРТ возможно выявить изменения паренхимы лёгких, а также анатомическую локализацию системного артериального кровоснабжения и венозного дренажа ЛС
- Лёгочная или аортальная ангиография, позволяющая выявить аномальные сосуды. Результаты этого исследования важны, чтобы избежать их повреждения в процессе операции[6][9][10][8]
Дифференциальная диагностика
- Кистозная аденоматоидная мальформация
- Бронхогенная киста
- Очаговая бронхоэктазия
- Врождённая долевая эмфизема
- Опухоли забрюшинного пространства при экстралобарных абдоминальных секвестрациях[4]
- Врождённая диафрагмальная грыжа
- Опухоли средостения (тератома, нейробластома)[8]
- Хроническая пневмония
- Абсцесс лёгкого
- Лёгочная артериовенозная мальформация
- Синдром Ятагана[11]
Осложнения
- Хроническое воспаление, которое может быть вызвано синегнойной палочкой, микобактерией туберкулёза, нокардией, аспергиллами
- Кровохарканье
- Геморрагический плеврит
- Малигнизация[4][8]
Лечение
Хирургическое вмешательство остаётся единственным эффективным методом лечения ЛС. Традиционно операция выполняется через заднебоковой торакальный доступ, однако такой доступ может приводить к ряду осложнений, обусловленных неблагоприятным воздействием на формирующийся мышечно-рёберный каркас у пациентов раннего возраста[5][7].
Торакоскопический метод позволяет выполнить секвестрэктомию при экстралобарной ЛС, а при интралобарной секвестрации выполняется торакоскопическая лобэктомия[1].
Одним из методов лечения является эндоваскулярная окклюзия питающей артерии, способствующая регрессу секвестрации. Данная методика рассматривается как альтернатива торакотомии ввиду меньшей инвазивности, однако имеет существенные ограничения, включая значительную продолжительность вмешательства и лучевую нагрузку на пациента. Также требуется повторное проведение эмболизации из-за недостаточной эффективности первичной процедуры. В связи с этим рекомендуются рассматривать эндоваскулярную окклюзию не как самостоятельный метод лечения, а в качестве предоперационной подготовки, позволяющей:
1) уменьшить васкуляризацию патологического образования
2) снизить интраоперационную кровопотерю
3) облегчить выполнение последующей радикальной резекции[5]