VHL
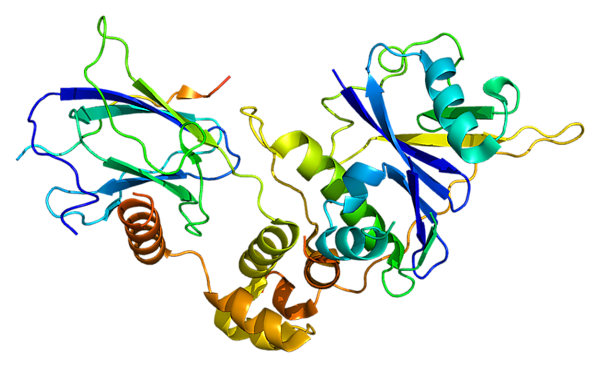
VHL (сокр. от нем. Von Hippel–Lindau), также опухолевый супрессор VHL или pVHL — белок-онкосупрессор (антионкобелок), который кодируется одноимённым геном VHL, расположенным на коротком плече (p-плече) 3-ей хромосомы[5][6]. Мутация гена VHL связана с аутосомно-доминантным заболеванием — болезнью Гиппеля—Линдау[7]. Большинство спорадических светлоклеточных карцином почек характеризуются инактивацией гена-онкосупрессора VHL[8].
Белок состоит из остатков 213 аминокислот, молекулярная масса составляет 24 153 Да[9].
Название белка VHL происходит от названия болезни (von Hippel-Lindau). Впервые его название было использовано в мартовском номере 1988 года журнала Nature, в статье исследователями Bernd Seizinger и его сотрудниками был установлен локус предполагаемого патогенного гена в локусе 3p25[10].
Общие сведения
Структура гена
Ген VHL локализуется на 3-ей хромосоме в локусе 3p26-p25. Ген VHL включает в себя 3 экзона и 642 пары нуклеотидов ДНК[11].
Два из стартовых кодонов гена в первом экзоне приводят к экспрессии двух форм белка VHL. Первый экзон насчитывает 213 пар нуклеотидов, которые транскрибируются на молекулу мРНК, начиная с первого стартового кодона, тогда как второй стартовый кодон находится в положении 54 и предшествует кодирующей последовательности инициации трансляции. Транскрипция гена из этого исходного сайта и трансляция мРНК приводят к синтезу белка VHL1, состоящего из 160 аминокислот, обозначенного VHL19[12], в отличие от первой формы белка с более высокой молекулярной массой — VHL30[13]. Было обнаружено, что изоформы VHL30 в основном локализуются в цитоплазме, а изоформа VHL19 — в клеточном ядре; это указывает на то, что выполняемые функции данных белков не идентичны[14][15]. В одном исследовании присутствие pVHL в митохондриях было продемонстрировано с помощью меченых GFP антител[16]. Когда молекулярная масса не имеет отношения к описанию функции белка, то используется обозначение pVHL.
Было обнаружено, что транскрипт pVHL мРНК альтернативно сплайсирован, что выражается наличием в клетке двух изоформ мРНК, один из которых имеет экзон 2, а другой без экзона. Поскольку люди с мутированным геном VHL лишены экзона 2 и имеют ярко выраженные симптомы болезни von Hippel—Lindau, то похоже, что только более длинная белковая изоформа действует как супрессор. До сих пор не доказано, что альтернативные сплайсирующие мРНК являются трансляционными in vivo[17].

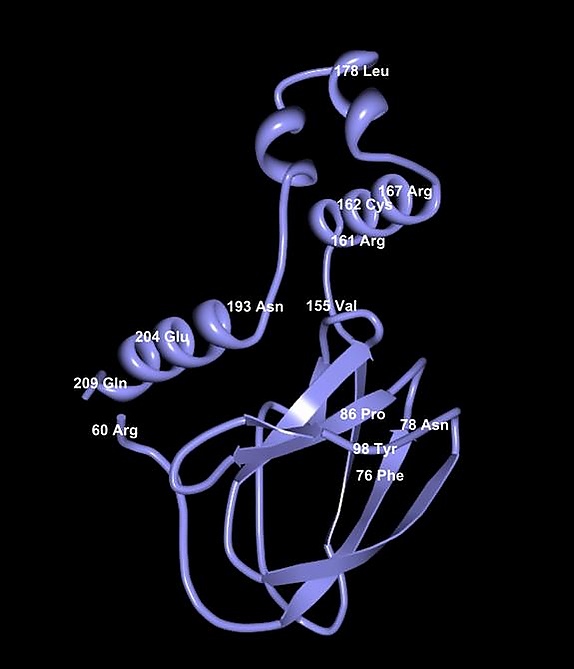
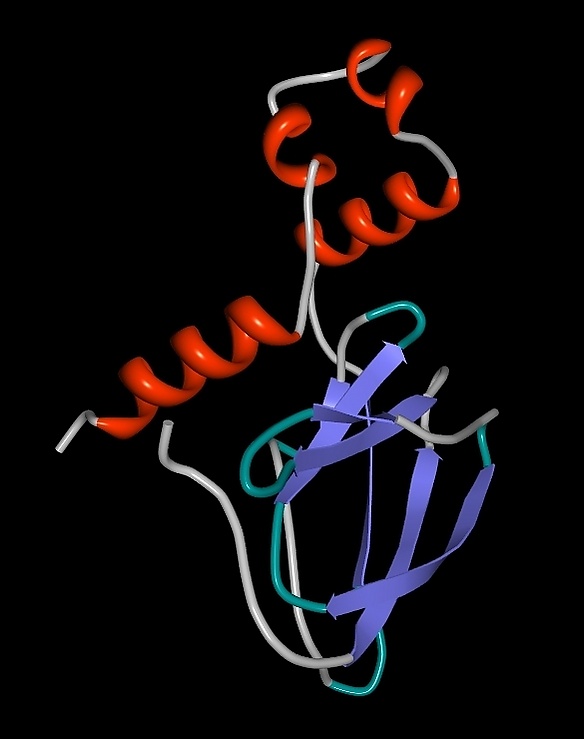
Ген VHL (выше) и VHL-белок. Ген VHL (нуклеотиды 1-4400) содержит три экзона (1-3) окрашены в фиолетовый цвет, нетранслируемые области — 5'UTR и 3'UTR. Белок VHL (ниже) содержит 213 аминокислотных остатков, имеет α и β-домены и два кодона метионина в положениях 1 и 54, которые могут действовать как стартовые кодоны. Маркированная область (GXEEX)8, пентамерный повторяющийся консервативный эволюционный мотив, роль которого не ясна до сих пор[18]
Промоторная последовательность гена VHL богата репликатами GC, не имеет ТАТА-бокса и CCAAT-последовательности; Возникновение транскрипции, вероятно, происходит в точке, предполагающей связывание белка Sp1, 60 пар оснований в направлении 5'-конца нити ДНК от первого стартового кодона VHL. Последовательность промотора имеет множество предсказуемых сайтов для связывания факторов транскрипции, но до сих пор не был идентифицирован механизм контроля экспрессии гена VHL. Последовательность кодирования гена предшествует 3’UTR-области, имеющей 11 повторов Alu[19].
Экспрессия гена
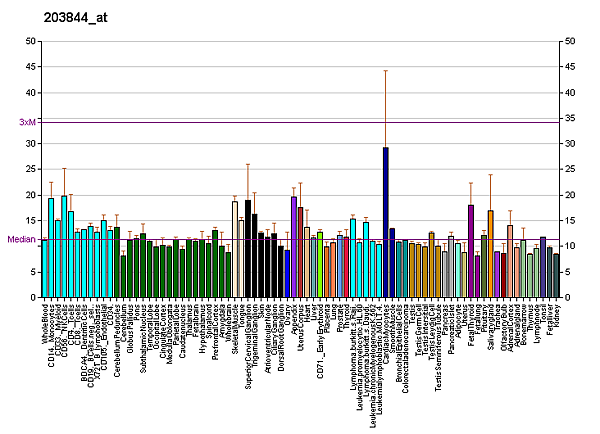
Экспрессия гена VHL не ограничена органами, из которых развиваются опухоли при болезни von Hippel—Lindau. Она происходит во многих типах клеток как у плода, так и у взрослых организмов[11]. В ходе эмбриогенеза мРНК гена VHL была обнаружена практически во всех типах тканей с 6-ой недели жизни. Но особенно большое количество мРНК VHL были найдены в тканях урогенитального тракта, головного мозга, спинного мозга, спинальных ганглиях, глазного нерва и эпителия бронхов[17]. Распределение усиленной экспрессии гена VHL совершенно точно не соответствует тканям при болезни von Hippel—Lindau[18]. В развивающейся нормальной почке (метанефрос) VHL экспрессируется в проксимальной канальце (из которого возникает карцинома почки), но белок pVHL в изобилии синтезируется в петле Генле[17][20]. Нет никаких свидетельств различий в экспрессии двух форм белка VHL19 и VHL30 между различными тканями плода.
Функции
Белок pVHL воздействует на клетки в комплексе, состоящем из многочисленных белков, которые прямо или косвенно взаимодействуют с ним, посредством образования связей. На сегодняшний день известно, что эта группа белков включает:
- элонгин C[22] и элонгин B[22], CUL2[23] и Rbx1 (также называемый ROC1 или Hrt1)[24]; В комплекс также входит ацетилтрансфераза SSAT2[25];
- HIF-1[26];
- фибронектин[27];
- тубулин-формирующие микротрубочки[15];
- sp1 транскрипционный фактор[28];
- протеинкиназы C (PKC-δ изотипы, PKC-ζ и PKC-λ)[29][30];
- белки из семейства деубиквитинизирующих ферментов, VDU1 и VDU2 (VHL-взаимодействующий деубиквитинирующий фермент-1/2)[31][32];
- белок-онкосупрессор P53[33];
- гиперфосфорилированный Rpb1-белок, субъединицы РНК-полимеразы II[34];
- имидопептидаза, которая прикрепляется к N-концу белка в аминокислотных остатках 1-57;
- Tat 1 связывающий белок (белок Tat 1 вируса иммунодефицита человека (ВИЧ-1)) прикрепляется к области pVHL 1: 87;
- Филамин (актинсвязывающий белок, АБП) также прикрепляется к этой области.
При высоких концентрациях в клетке молекулы белка pVHL могут связываться друг с другом через аминокислотные остатки 96-122, но не было продемонстрировано, чтобы молекулы pVHL связывались друг с другом при физиологических (нормальных) концентрациях[35].
Основные функции, выполняемые белком pVHL:
- в комплексе с элонгином C, элонгином B и куллином (CUL2) с активной убиквитинлигазы E3 в качестве субстратного белка участвует в убиквитинировании белка HIF1-α[36]. Данный комплекс разрушает белок HIF1-α в протеасоме и ингибирует транскрипцию индуцированных гипоксией генов, активированных HIF1-α;
- ингибирование транскрипции определённых факторов роста (например, VEGF) через Sp1;
- модификация внутриклеточных сигнальных процессов, посредством ингибирования атипичных путей белка протеинкиназами PKC-δ, PKC-ζ и PKC-λ, а также путём убиквитинирования[29][30][37];
- при связывании с фибронектином pVHL может влиять на образование внеклеточного матрикса[18];
- связывание с тубулином из микротрубочек ингибирует их деполимеризацию; Эта функция pVHL не зависит от активности убиквитинлигазы Е3, входящей в комплекс VBC, потому что мутантный pVHL-белок, не имеющий элонгин С связывающего сайта, сохраняет способность стабилизации микротрубочек[15];
- Необъяснимым образом контролирует клеточный цикл; VHL-/- (не содержащие VHL) клетки не могут покинуть цикл после экспериментального ответа на такой фактор, как удаление сыворотки культуральной среды[38][39]; Возможность выхода из клеточного цикла была восстановлена при введении pVHL; Контроль цикла с помощью pVHL проявляется многофакторно: два исследования показали, что pVHL ингибирует циклин D1, который является митогеном[40][41]; В другом исследовании показано, что pVHL ингибирует TGF-α, ген которого недавно был идентифицирован как регулируемый белком HIF[42].
В одном исследовании было продемонстрировано, что pVHL связывается in vivo с белком P53, стабилизируя и предотвращая убиквитинирование P53 белком Mdm2; Кроме того, в условиях повреждения ДНК (генотоксический стресс) pVHL способствует взаимодействию белков P53 и P300 и последующему ацетилированию P53, что приводит к увеличению транскрипционной активности этого белка и эффективной остановки клеточного цикла и, как следствие к индукции апоптоза. По-видимому, это может быть искомый, нелетальный механизм действия HIF-α, в котором pVHL выполняет роль супрессорного белка[33]. Важность взаимодействия pVHL с филамазой и ВИЧ-связывающим белком Tat неясна[17].
Регуляция функций
В пределах нуклеотидной последовательности гена VHL было найдено несколько консенсусных киназных последовательностей, поэтому регулирование функции белка pVHL может основываться на киназном фосфорилировании[18]. Недавно было показано, что VHL30 является субстратом для киназы 3 гликогенсинтазы (GSK3) in vitro и in vivo[43]. Фермент фосфорилирует VHL30 по сериновому остатку 68; прежде белок должен быть фосфорилирован на серине 72, который in vitro катализирует казеинкиназу I. Как показано в той же работе, мутантный некиназный VHL30-белок не имеет функции стабилизации микротрубочек.
Эквиваленты гена VHL у животных
Генетическая последовательность VHL высоко консервативна у гомологичных человекообразных приматов и грызунов[44][45]. Гомологичный ген был обнаружен у нематод Caenorhabditis elegans[44] и в плодовой мушке[46]. Сохранение последовательностей генов особенно велико в областях, связывающих домены с другими белками[47]. Комплекс pVHL-элонгин B-элонгин С напоминает комплекс SCF у дрожжей, который проявляет функцию полиубиквитинирования белков посредством их протеолиза. Элонгин C и Cul2 представляют собой, соответственно эквивалентные дрожжевые белки Skp1 и Cdc53. Сходство этих белков было подтверждено позже предположением о том, что белковый комплекс pVHL функционирует в клетках человека как убиквитин-E3-лигаза[48]. Область гена VHL между кодонами 14-53, кодирует восемь репликатов, содержащие кислые аминокислоты (с повышенным содержанием карбоксильных групп) [Gly-X-Glu-Glu-X]8 (GXEEX8), которая гомологична мембранному белку Trypanosoma brucei[44]. Значение этого факта остается неизвестным[18].
Патологии, связанные с мутацией гена VHL
| Общий объём описанной мутации | 823 |
| Сдвигов рамки считывания | 297 (36,08 %) |
| Делеции | 235 (28,55 %) |
| Инсерции | 62 (7,53 %) |
| Точечные мутации | 496 (60,27 %) |
| Миссенс-мутации | 399 (48,48 %) |
| Нонсенс-мутации | 97 (11,79 %) |
| G>A | 29 |
| G>A w CpG | 42 |
| C>T | 65 |
| C>T at CpG | 57 |
| A>T | 10 |
| A>G | 20 |
| A>C | 17 |
| T>G | 20 |
| T>C | 76 |
| T>A | 29 |
| C>A | 30 |
| C>G | 47 |
| G>T | 41 |
| G>C | 29 |
| Комплексные мутации | 2 (0,24 %) |
Гомозиготные мыши с VHL-/- живут 10,5-12,5 дней внутриутробной жизни; причиной выкидыша является нарушение вагулогенетики плаценты. Вероятно, это очень редкая мутация обоих аллелей VHL, которая у людей также препятствует раннему развитию эмбриона[50][51].
Как упоминалось ранее, мутация гена VHL у гетерозигот человека почти всегда вызывает болезнь von Hippel—Lindau. Клиническое распространение заболевания из-за частоты отдельных симптомов, особенно светлоклеточной карциномы почки и феохромоцитомы, коррелирует с характером мутации в гене VHL. Таким образом, большое количество делеций и преждевременное прекращение трансляции, приводящие к укороченной молекуле pVHL, характерны для заболевания типа 1, и точечные мутации, особенно миссенс, отвечают за тип 2[18]. Известно более 500 различных мутаций зародышевой линии в гене VHL; все случаи новых мутаций сообщаются в международный реестр.
| Тип | Тип мутации | Молекулярный дефект | HB R | HB CNN | RCC | Pheo | GEP |
|---|---|---|---|---|---|---|---|
| 1 | Делеции, нонсенс | Гиперэкспрессия HIF и сверхэкспрессия генов ответа гипоксии | +
|
+
|
+
|
-
|
-
|
| 2A | Миссенс | Гиперэкспрессия HIF и сверхэкспрессия генов ответа гипоксии Дестабилизация микротрубочек |
+
|
+
|
-
|
+
|
+
|
| 2B | Миссенс | Гиперэкспрессия HIF и сверхэкспрессия генов ответа гипоксии | +
|
+
|
+
|
+
|
+
|
| 2C | Миссенс | Нарушение ECM-образования фибронектином Механизм зависит от P53 (?) |
-
|
-
|
-
|
+
|
? |
| HB R — гемангиомы сетчатки; HB CNN — гемангиомы центральной нервной системы; RCC — карцинома почек; Pheo — феохромоцитома; GEP — нейроэндокринная опухоль поджелудочной железы | |||||||
Соматические мутации в гене VHL также обнаружены в спорадических опухолях почек и зародышевых клетках. Соматическая мутация гена VHL встречается примерно в 50 % случаев спорадического рака почки, и примерно в 10-20 % ген гиперметилируется[18]. Сообщалось также о 30 % случаев спорадических эмбриональных аномалий, но гиперметилирование VHL до сих пор не обнаруживалось в опухолевых клетках[18]. LOH (сокр. от англ. loss of heterozygosity — утрата гетерозиготности) гена VHL описана в спорадических панкреатических микрососудистых аденомах[53] и эндотелиальных опухолях (ELST)[54]. Мутации VHL встречаются редко при спорадической феохромоцитоме и очень редки в других формах рака: лёгких, молочной железы, яичника, яичек, шейки матки, эндометрия, простаты, колоректальный рак, карцинома мочевого пузыря, рака кожи (злокачественная меланома), плевральной карциномы, плоскоклеточной карциномы полового члена и фолликулярного рака щитовидной железы[17].
Недавно было высказано предположение, что делеция дистальных участков 11q 3-ей хромосомы в клетках нейробластомы и связанная с этим потеря гена VHL в данных клетках, могут быть причиной более агрессивного фенотипа болезни[55]. Это было бы связано с предыдущими сообщениями о дифференцировке клеток незрелых опухолей нейробластомы под влиянием гипоксии, связанной с более агрессивным курсом[56]. Наблюдалась сильная корреляция между сниженными уровнями мРНК VHL и низкой выживаемостью пациентов (p = 0,013). По-видимому, наивысшая прогностическая ценность VHL обнаружена в опухолях, экспрессирующих NTRK1 (TRKA)[55].
| Мутация | OMIM | Тип мутации | Тип болезни (комментарии) |
|---|---|---|---|
| Leu63Pro | 608537.0016 | VHL | |
| Arg64Pro | 608537.0015 | VHL | |
| Ile75DEL (Ile146DEL) | 608537.0001 | 437 делеция 3 п.н. | VHL тип 1 |
| Phe76DEL | 226-228 делеция TTC | VHL (9 семей в UMD Central[57]) | |
| 76DEL | 227-229 делеция TCT | VHL (6 семей в UMD Central[57]) | |
| Asn78Ser/His/Ter | |||
| Ser80Leu | VHL тип 2C[58] | ||
| Pro81Ser | 608537.0020 | Транзиция 454C>T | VHL тип 2C |
| Val84Leu (Val155Leu) | 608537.0025 | Трансверсия 463G>T | VHL тип 2C[59] |
| Pro86Leu | |||
| Gly93Ser | 608537.0026 | Транзиция 490G>A | Спорадическая феохромоцитома[60] |
| Tyr112His | 608537.0012 | VHL тип 2A | |
| Tyr112Asn | 608537.0017 | Трансверсия 547T>A | VHL |
| Asp126Tyr | 608537.0022 | ECYT2[61] | |
| Val130Leu | 608537.0021 | ECYT2[61] | |
| Leu135Phe | 608537.0008 | Трансверсия 618A>C | Спорадическая гемангиома эмбрионального мозжечка[62] |
| 147DEL | Делеция T | VHL (5 семей в UMD Central[57]) | |
| Ser149Ala | 658G>T[63] | ||
| Trp159Ser (Trp88Ser) | 608537.0007 | Трансверсия 476G>C | VHL спорадическая гемангиома эмбрионального мозжечка[62] |
| Arg161TER | 608537.0006 | Транзиция 694C>T | VHL тип 1 спорадическая кистозная аденома придатка яичка[64] |
| Cys162Tyr/Phe/Trp | |||
| Leu163Pro | 608537.0018 | Транзиция 701T>C | RCC |
| Val166Phe | 608537.0013 | VHL тип 2A | |
| Arg167Trp (Arg23Trp) | 608537.0003 | Транзиция 712C>T | VHL typu 2B |
| Arg167Gly | 608537.0004 | VHL тип 2B | |
| Arg167Gln | 608537.0005 | VHL тип 2B | |
| Tyr169His (Tyr98His) | 608537.0009 | Транзиция 505T>C | VHL тип 2A (мутация Black Forrest)[65][66] |
| Leu178Pro | |||
| Ser183TER (Ser254TER) | 608537.0002 | Трансверсия 761C>A | RCC |
| Leu188Val | 608537.0014 | VHL тип 2C[67][68] | |
| His191Asp | 608537.0024 | Трансверсия 571C>G | ECYT2[61] |
| Pro192Ser | 608537.0023 | Транзиция 574C>T | ECYT2[61] |
| Arg200Trp | 608537.0019 | Транзиция 598C>T | ECYT2[69] |
VHL — болезнь von Hippel—lindau
RCC — карцинома почек
ECYT — семейная эритроцитемия тип 2
Взаимодействия с белками
Примечания
Для углубленного изучения
- Conaway R.C., Conaway J.W. The von Hippel–Lindau tumor suppressor complex and regulation of hypoxia-inducible transcription (англ.) // Advances in Cancer Research : journal. — 2003. — Vol. 85. — P. 1—12. — doi:10.1016/S0065-230X(02)85001-1. — PMID 12374282.
- Czyzyk-Krzeska M.F., Meller J. von Hippel–Lindau tumor suppressor: not only HIF's executioner (англ.) // Trends (journals) : journal. — 2004. — April (vol. 10, no. 4). — P. 146—149. — doi:10.1016/j.molmed.2004.02.004. — PMID 15162797.
- Esteban M.A., Harten S.K., Tran M.G., Maxwell P.H. Formation of primary cilia in the renal epithelium is regulated by the von Hippel–Lindau tumor suppressor protein (англ.) // Journal of the American Society of Nephrology : journal. — 2006. — July (vol. 17, no. 7). — P. 1801—1806. — doi:10.1681/ASN.2006020181. — PMID 16775032.
- Hoebeeck J., Vandesompele J., Nilsson H., De Preter K., Van Roy N., De Smet E., Yigit N., De Paepe A., Laureys G., Påhlman S., Speleman F. The von Hippel–Lindau tumor suppressor gene expression level has prognostic value in neuroblastoma (англ.) // International Journal of Cancer : journal. — 2006. — August (vol. 119, no. 3). — P. 624—629. — doi:10.1002/ijc.21888. — PMID 16506218.
- Kaelin W.G. The von Hippel–Lindau tumor suppressor gene and kidney cancer (англ.) // Clinical Cancer Research : journal. — 2004. — September (vol. 10, no. 18 Pt 2). — P. 6290S—5S. — doi:10.1158/1078-0432.CCR-sup-040025. — PMID 15448019.
- Kaelin W.G. The von Hippel–Lindau tumor suppressor protein and clear cell renal carcinoma (англ.) // Clinical Cancer Research : journal. — 2007. — January (vol. 13, no. 2 Pt 2). — P. 680s—684s. — doi:10.1158/1078-0432.CCR-06-1865. — PMID 17255293.
- Kamura T., Conaway J.W., Conaway R.C. Roles of SCF and VHL ubiquitin ligases in regulation of cell growth (англ.) // Progress in Molecular and Subcellular Biology : journal. — 2002. — Vol. 29. — P. 1—15. — doi:10.1007/978-3-642-56373-7_1. — PMID 11908068.
- Kralovics R., Skoda R.C. Molecular pathogenesis of Philadelphia chromosome negative myeloproliferative disorders (англ.) // Blood Reviews : journal. — 2005. — January (vol. 19, no. 1). — P. 1—13. — doi:10.1016/j.blre.2004.02.002. — PMID 15572213.
- Lonser R.R., Glenn G.M., Walther M., Chew E.Y., Libutti S.K., Linehan W.M., Oldfield E.H. von Hippel–Lindau disease (англ.) // The Lancet. — Elsevier, 2003. — June (vol. 361, no. 9374). — P. 2059—2067. — doi:10.1016/S0140-6736(03)13643-4. — PMID 12814730.
- Neumann H.P., Wiestler O.D. Clustering of features of von Hippel–Lindau syndrome: evidence for a complex genetic locus (англ.) // The Lancet : journal. — Elsevier, 1991. — May (vol. 337, no. 8749). — P. 1052—1054. — doi:10.1016/0140-6736(91)91705-Y. — PMID 1673491.
- Russell R.C., Ohh M. The role of VHL in the regulation of E-cadherin: a new connection in an old pathway (англ.) // Cell Cycle : journal. — 2007. — January (vol. 6, no. 1). — P. 56—9. — doi:10.4161/cc.6.1.3668. — PMID 17245122.
- Schipani E. Hypoxia and HIF-1 alpha in chondrogenesis (англ.) // Seminars in Cell and Developmental Biology : journal. — 2006. — Vol. 16, no. 4—5. — P. 539—546. — doi:10.1016/j.semcdb.2005.03.003. — PMID 16144691.
- Takahashi K., Iida K., Okimura Y., Takahashi Y., Naito J., Nishikawa S., Kadowaki S., Iguchi G., Kaji H., Chihara K. A novel mutation in the von Hippel–Lindau tumor suppressor gene identified in a Japanese family with pheochromocytoma and hepatic hemangioma (англ.) // Internal Medicine : journal. — 2006. — Vol. 45, no. 5. — P. 265—269. — doi:10.2169/internalmedicine.45.1547. — PMID 16595991.
- Graff J.W. The VHL Handbook: What You Need to Know about VHL (неопр.) // VHL Family Alliance. — 2005. — Т. 12, № 1. — С. 1—56.
Ссылки
- VHL Alliance
- The VHL mutations database
- Gen VHL на странице ExPASy Proteomics
- Ген VHL в базе Ensembl
- Ген VHL и его гомологи в базе HomoloGene