Пирролизин
Пирролизин — это нестандартная протеиногенная Аминокислоты, которая входит в состав некоторых ферментов метаболизма метана у метаногенных архей. Он был обнаружен в 2002 году на активном участке фермента метилтрансферазы из метан продуцирующего археона, Methanosarcina barkeri[1][2]. У человека пирролизин отсутствует.
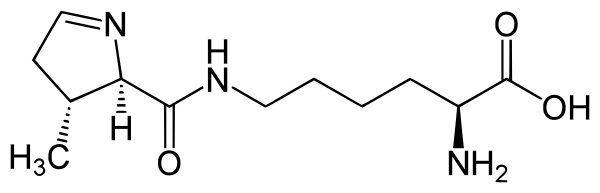
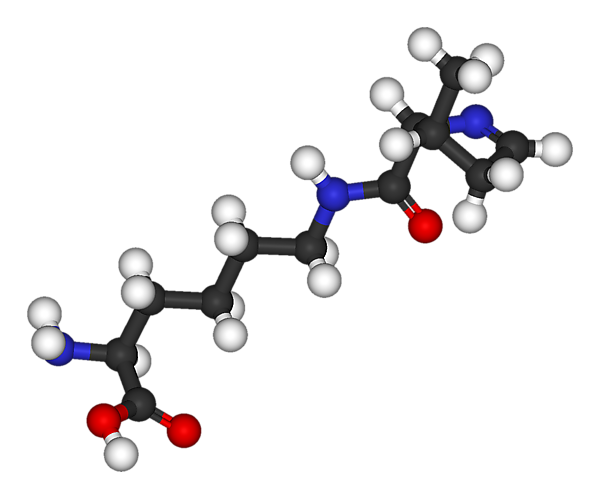
Пирролизин содержит α-аминогруппу (которая находится в протонированной форме NH3+ в биологических условиях), группу карбоновых кислот (которая находится в депротонированной форме COO- в биологических условиях). Его пирролиновая боковая цепь сходна с цепью лизина по своей основности и положительному заряду при нейтральном pH.
Для обозначения пирролизина ИЮПАК рекомендует трёхбуквенное сокращение Pyl и однобуквенное O. Его также можно назвать 22-й аминокислотой.
Общие сведения
| Пирролизин | |
|---|---|
| Общие | |
| Хим. формула | C12H21N3O3 |
| Физические свойства | |
| Молярная масса | 255,313 г/моль |
| Классификация | |
| Рег. номер CAS | 448235-52-7 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 5460671 |
| UNII | H3214Y96LP |
| CompTox Dashboard EPA | DTXSID70420110 |
| SMILES | |
| InChI | |
| ChEBI | 21860 |
| ChemSpider | 4574156 |
Строение
Как определено с помощью рентгеновской кристаллографии[2] и масс-спектрометрии, пирролизин представляет собой лизин, ϵ-азот которого состоит в пептидной связи с (4r, 5r)-4-замещённым пирролин-5-карбоксилатом[3].
Синтез
Пирролизин синтезируется в естественной среде путем соединения двух молекул L-лизина. Одна молекула лизина сначала преобразуется в (R)-3-метил-D-орнитин, который затем лигируется со вторым лизином. Группа -NH2 удаляется, после чего следует стадия циклизации и дегидратации с получением L-пирролизина[4]. В синтезе пирролизина задействован фермент пирролизил-т-РНК синтетаза (pyrrolysyl-tRNA synthetase) [5]
Генетическое кодирование
Пирролизин закодирован кодоном UAG (обычно стоп-кодон). Он используется реже, чем другие стоп-кодоны, и, если встречается в открытой рамке считывания, за ним, как правило, следуют другие стоп-кодоны. Тем не менее, синтез аминокислоты и включение её в белок опосредуется биологическим механизмом, кодируемым кластером генов pylTSBCD[6].
Рядом с кластером генов переноса метильной группы археи Methanosarcina barkeri располагается ген pylT, который кодирует необычную тРНК с антикодоном CUA. Соседний ген pylS кодирует аминоацил-тРНК-синтетазу второго класса, которая присоединяет пирролизин к тРНК-продукту гена pylT. Оперон, содержащий гены pylT и pylS также найден в геномах других секвенированный представителей семейства Methanosarcinaceae. Гомологи генов pylS и pylT обнаружены также в грам-положительной бактерии Desulfitobacterium hafniense, хотя функции этих гомологов у данной бактерии неизвестны.[7]
Первоначально было показано, что продукт гена pylT — тРНК с антикодоном (CUA) — может быть «заряжена» аминокислотой лизином с помощью белка PylS. Относительно недавно было показано, что тРНК с антикодоном CUA может быть «заряжена» лизином в условиях in vitro последовательным взаимодействием с лизиновыми тРНК-синтетазами первого и второго класса из M. barkeri. Последние данные указывают на то, что происходит прямое присоединение пирролизина к тРНК с антикодоном CUA при помощи белкового продукта гена pylS. Это означает, что пирролизин представляет собой 22-ю аминокислоту, закодированную генетически.[8]
Каталитическая функция
Дополнительное пирролиновое кольцо включено в активный центр нескольких метилтрансфераз, где, как полагают, оно вращается относительно свободно. Считается, что кольцо участвует в позиционировании и отображении метильной группы метиламина для атаки корриноидным кофактором. Предложенная модель состоит в том, что соседний остаток, несущий карбоновую кислоту, глутамат, протонируется, и протон затем может быть перенесен в азот иминового кольца, подвергая соседний кольцевой углерод нуклеофильному присоединению метиламином. Положительно заряженный азот, созданный этим взаимодействием, может затем взаимодействовать с депротонированным глутаматом, вызывая сдвиг в ориентации кольца и подвергая метильную группу, полученную из метиламина, связывающей расщелине, где он может взаимодействовать с корриноидом. Таким образом, чистый CH3+ переносится на атом кобальта кофактора с изменением состояния окисления с I на III. Затем высвобождается аммиак метиламинового происхождения, восстанавливая исходный имин[2].
См. также
- Генетический код
- Трансляция
- Селеноцистеин, 21-я аминокислота. Как и пирролизин, закодирована стоп-кодоном.