Пептидная связь
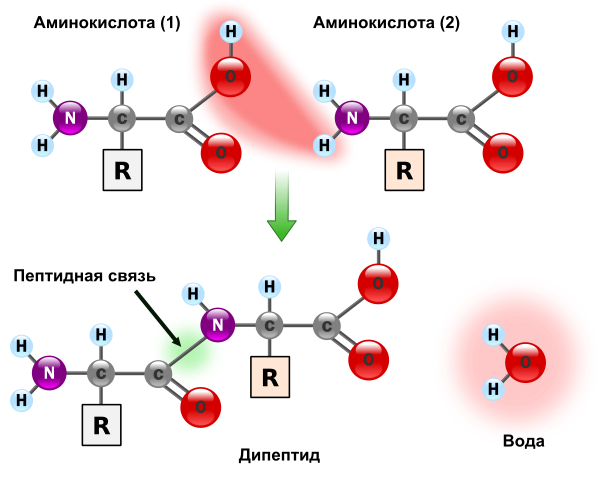
Пептидная связь — вид амидной связи, возникающей при образовании белков и пептидов в результате взаимодействия α-аминогруппы (—NH2) одной аминокислоты с α-карбоксильной группой (—СООН) другой аминокислоты.
Из двух аминокислот (1) и (2) образуется дипептид (цепочка из двух аминокислот) и молекула воды. По этой же схеме рибосома генерирует и более длинные цепочки из аминокислот: полипептиды и белки. Разные аминокислоты, которые являются «строительными блоками» для белка, отличаются радикалом R.
Свойства пептидной связи
Как и в случае любых амидов, в пептидной связи за счет резонанса канонических структур связь C-N между углеродом карбонильной группы и атомом азота частично имеет характер двойной:
Это проявляется, в частности, в уменьшении её длины до 1,33 ангстрема:
Это обусловливает следующие свойства:
- 4 атома связи (C, N, O и H) и 2 α-углерода находятся в одной плоскости. R-группы аминокислот и водороды при α-углеродах находятся вне этой плоскости.
- H и O в пептидной связи, а также α-углероды двух аминокислот транс-ориентированы (транс-изомер более устойчив). В случае L-аминокислот, что имеет место во всех природных белках и пептидах, R-группы также транс-ориентированы.
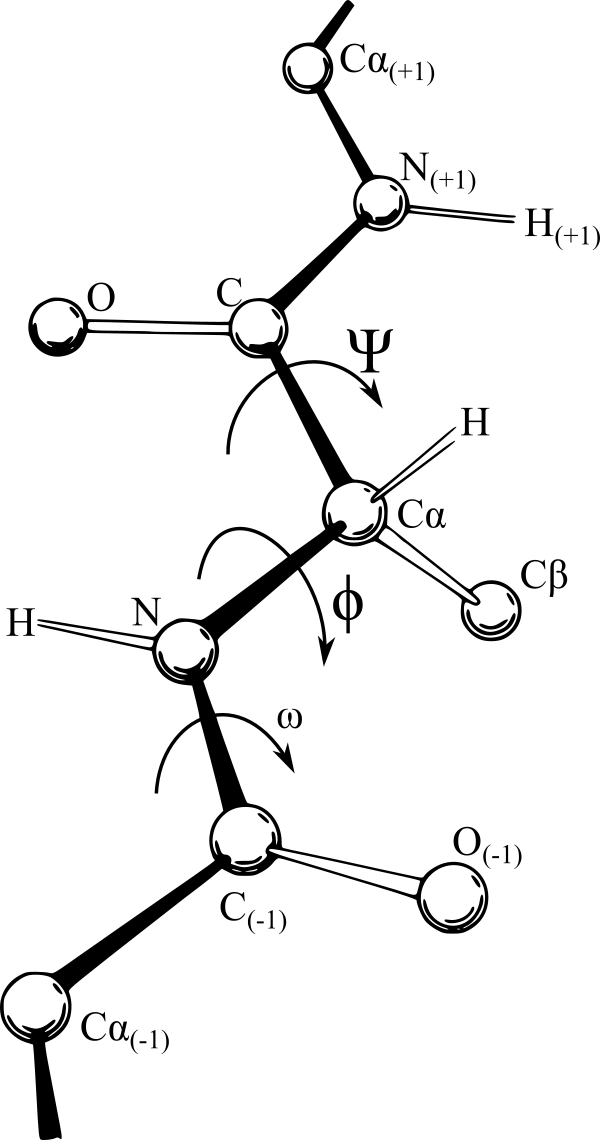
- В случае полипептида вращение возможно вокруг связи около азота (N-C, угол вращения обозначен как ψ) или между углеродами каждого пептидного звена (C-C, угол вращения обозначен как φ), но невозможно в месте соединения звеньев из-за их частично двойного характера связи.
Конформация полипептидов
Углы φ и ψ могут принимать различные значения, и число возможных пространственных конфигураций для полипептидной цепи может быть бесконечно большим. Однако в реальных условиях ряд конфигураций не реализуется из-за пространственных затруднений.
В пределах стерически дозволенных углов φ и ψ наиболее вероятна такая конфигурация пептидной цепи, при которой потенциальная энергия системы минимальна. Выигрыш потенциальной энергии происходит в результате целого ряда взаимодействий между атомами и атомными группами внутри полипептидной цепи (нековалентные взаимодействия, дипольные взаимодействия, торсионный потенциал).
Существует некоторое минимальное расстояние между центрами атомов, при котором их дальнейшее сближение невозможно. Эти расстояния, оценены в основном по данным кристаллографии[1].
Для обнаружения белков и пептидов, а также их количественного определения в растворе используют биуретовую реакцию.