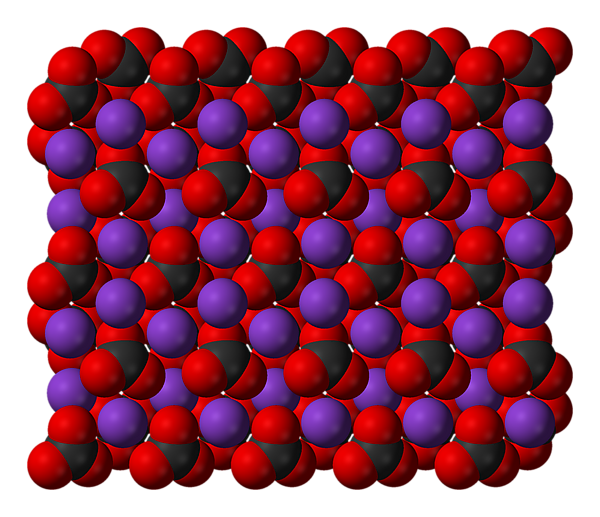
Карбонат калия
Карбона́т ка́лия, углеки́слый калий, арх. пота́ш K2CO3 — средняя соль калия и угольной кислоты. Белое кристаллическое вещество, хорошо растворимое в воде. Малотоксичен, относится к III классу опасности[1].
Старое название соли пота́ш из нидерл. potasch напрямую или через нем. Pottasche, фр. potasse[2].
Общие сведения
| Карбонат калия | |
|---|---|
| Общие | |
| Систематическое наименование |
Карбонат калия |
| Традиционные названия | углекислый калий, поташ |
| Хим. формула | K2CO3 |
| Физические свойства | |
| Состояние | кристаллическое |
| Молярная масса | 138,205 г/моль |
| Плотность | 2,44 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 891 °C |
| • разложения | 1200 °C |
| Энтальпия | |
| • образования | -1146,1 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 110,5 г/100мл (20 °C) |
| Классификация | |
| Рег. номер CAS | 584-08-7 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 11430 |
| UNII | BQN1B9B9HA |
| CompTox Dashboard EPA | DTXSID2036245 |
| Рег. номер EINECS | 209-529-3 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E501(i) и E501 |
| RTECS | TS7750000 |
| ChEBI | 131526 |
| ChemSpider | 10949 |
| ECHA InfoCard | 100.008.665 |
| Безопасность | |
| NFPA 704 | |
История
Поташ — одна из солей, известных людям ещё в древности. Обычно поташ загрязнён различными примесями, поэтому не имеет такого чисто-белого цвета, как измельчённый карбонат калия. До XX века в Европе поташ был одним из важнейших промышленных химических реагентов. Его получали путём водной экстракции из растительной золы с дальнейшей очисткой до необходимого уровня. Производство было сосредоточено в местах, богатых лесом, в Европе, но, в основном, в России и Северной Америке.
В России Пётр I в 1721 году установил монополию на производство поташа: «Нигде никому отнюдь поташа не делать и никому не продавать под страхом ссылки в вечную каторжную работу» — с целью сбережения леса, поскольку вводил технологию производства поташа из «худых бочек, сучьев и прочих обрезков»[3]. До введения монополии крупнейшим центром производства поташа́ в XVII веке в России, а следовательно и в мире были Нижегородский, Арзамасский и Муромский уезды с их богатыми лесами, позаимствованной из Литвы технологии и с привлечением литовских специалистов уничтожавшимися на зольных «майданах» или «будах» (будных станах)[4].
Физические и химические свойства
При нормальных условиях выглядит как бесцветные или белые кристаллы (моноклинная модификация), плотностью 2,44 г/см3. При 420 °C переходит в гексагональную модификацию плотностью 2,27 г/см3. Плавится при 891 °C[5].
При нагревании до 1200 °C разлагается на углекислый газ и оксид калия[6]:
Хорошо растворим в воде: 105,5 г/100 мл (0 °C), 110,5 (20 °C), 155,7 (100 °C), гигроскопичен. Образует несколько кристаллогидратов: K2CO3·5H2O, K2CO3·1,5H2O и K2CO3·0,5H2O, второй из них образуется при кристаллизации из водных растворов и хранении безводной формы на воздухе. Все перечисленные гидраты полностью обезвоживаются при 150—160 °C[5][7].
Водные растворы карбоната калия присоединяют углекислый газ с образованием гидрокарбоната калия[5].
С двуокисью серы водные растворы реагируют с образованием гидросульфита калия и двуокиси углерода[5].
Получение
Карбонат калия получают:
- как побочный продукт получается при переработке нефелинов[7].
- воздействием CO2 на раствор гидроксида калия[7]:
- путём электролиза хлорида калия, в результате чего образуется гидроксид калия, который, вступая в реакцию с углекислым газом, образует воду и карбонат калия (см. выше).
Для использования в качестве удобрения поташ получают из щёлока при выщелачивании водой золы из злаков или водорослей, так как именно карбоната калия больше всего в растворимой части растительных остатков (белая «зола» от костра — в основном поташ). Принцип добычи: в глиняный обожжённый сосуд с небольшим отверстием на дне насыпали золу и слегка утрамбовывали. Потом его заливали определённым количеством воды. Воду, прошедшую через сосуд, тщательно собирали и ею заливали следующую партию. И так до тех пор, пока жидкость не приобретала сиропообразную консистенцию. После лишнюю жидкость выпаривали в металлической посуде и получали поташ.
Применение
Карбонат калия применяют:
- для изготовления жидкого мыла[7];
- для производства пигментов[7];
- для производства хрустального, оптического[7] или тугоплавкого стекла;
- для крашения;
- для выращивания сельскохозяйственных культур (соли калия являются хорошим удобрением для растений);
- в фотографии как элемент проявителей[8];
- в качестве добавки в строительный раствор и бетон для понижения температуры замерзания (даёт белые пятна, поэтому разрабатываются специальные противоморозные присадки, не дающие разводов);
- для производства других соединений калия[7];
- как поглотитель сероводорода при очистке газов[7];
- как обезвоживающий агент[7];
- в качестве средства экстренного пожаротушения (в продукте Firevase компании Samsung)
- зарегистрирован в качестве пищевой добавки E501.
Безопасность
Карбонат калия считается «общепризнанным безопасным» (GRAS) в США в качестве пищевой добавки для человека Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA). Он используется в качестве ароматизатора и адъюванта, питательной добавки, средства контроля рН или вспомогательного средства для обработки пищевых продуктов без каких-либо ограничений[9]. В Европейском союзе карбонат калия указан в Постановлении Комиссии (ЕС) № 231/2012 в качестве разрешённой безопасной пищевой добавки и отнесён к категории «добавки, отличные от красителей и подсластителей»[10][11]. Объединённый экспертный комитет ФАО/ВОЗ по пищевым добавкам в 1965 году не стал устанавливать допустимое суточное потребление (ДСП) для карбоната калия, присвоив добавке статус «ДСП не определён»[12]. Это происходит в тех случаях, когда в ходе исследований за животными и людьми не удаётся определить вредный уровень для здоровья, а значит нет необходимости регулировать количество добавки в пищевых продуктах.
См. также
Примечания
Литература
- Гурлев Д. С. Справочник по фотографии (обработка фотоматериалов). — К.: Тэхника, 1988.
- Калия карбонат // Химический энциклопедический словарь / Гл. ред. И. Л. Кнунянц. — М. : Сов. энциклопедия, 1983. — 792 с.
- Ксензенко В. И., Стасиневич Д. С. Калия карбонат // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1990. — Т. 2: Даффа — Меди. — С. 288. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
Ссылки
- ГОСТ Р 55053-2012. Добавки пищевые. Калия карбонаты Е501. Общие технические условия
- ГОСТ 10690-73.