Инфаркт лёгкого
Инфа́ркт лёгкого (лёгочный инфаркт) — заболевание, возникающее при блокировке лёгочной артерии, от чего часть лёгкого воспаляется[1]. Инфаркт лёгкого представляет собой поражение лёгочной ткани, возникающее вследствие закупорки дистальных отделов лёгочной артерии, чаще всего обусловленной острой тромбоэмболией лёгочной артерии (ТЭЛА), которая встречается примерно в 30 % случаев. Нарушение кровотока приводит к ишемии тканей, что сопровождается кровоизлиянием и дальнейшим развитием некроза поражённой области лёгочной паренхимы. Современные методы диагностики основываются преимущественно на выявлении характерных рентгенологических изменений[2][3].
Благодаря двойному кровоснабжению лёгких как из бронхиального, так из лёгочного кровотока, ткань лёгкого более устойчива к инфаркту. Закупорка бронхиального кровообращения не вызывает инфаркта, но всё же он может возникать при тромбоэмболии лёгочной артерии, когда лёгочное кровообращение заблокировано и бронхиальное кровообращение не может полностью его компенсировать[4].
Общие сведения
Эпидемиология
Эпидемиология инфарктов лёгких тесно связана с частотой и исходами ТЭЛА. ТЭЛА является основной причиной инфаркта лёгких, на которую приходится около двух третей всех случаев. Распространённость инфаркта лёгких при ТЭЛА варьирует в зависимости от метода исследования: при аутопсии он выявляется у 15-68 % пациентов с ТЭЛА, а при компьютерной томографии — у 9-36 % пациентов[3].
Общая заболеваемость ТЭЛА составляет примерно 1 случай на 1000 человек в год, а риск летального исхода в первые 30 дней достигает 17,4 % в острых случаях. Долгосрочная выживаемость также варьирует: смертность в течение года после эпизода ТЭЛА составляет 19 %, а через три года достигает 30 %. При этом инфаркт лёгких ассоциирован с более высоким риском неблагоприятного исхода, особенно у пожилых пациентов или пациентов с онкологическими заболеваниями[5].
Смертность пациентов с инфарктом лёгких значительно снизилась благодаря улучшению диагностики и терапии ТЭЛА, включая применение тромболитической терапии и антикоагулянтов. Современные данные показывают, что в условиях специализированного лечения выживаемость пациентов с инфарктом лёгких достигает 97 %. Однако до сих пор отсутствует достаточное количество исследований, изучающих частоту и прогноз инфаркта лёгких отдельно от других осложнений ТЭЛА, что оставляет значительное поле для дальнейшего изучения этой проблемы[2].
Этиология
Наиболее распространённой причиной инфаркта лёгкого является ТЭЛА, которая сопровождается закупоркой ветвей лёгочной артерии эмболами. Однако существуют и другие состояния, способные вызывать инфаркт лёгкого. К ним относятся инфекционные процессы, злокачественные новообразования, хирургическая ятрогения, амилоидоз, серповидноклеточная анемия и системные васкулиты. Эти заболевания, независимо от их природы, нарушают кровоток, вызывают гипоксию и повреждают лёгочную ткань[2].
Одним из факторов риска развития инфаркта лёгкого является курение. Оно способствует хроническому воспалению, увеличивает проницаемость альвеолярно-капиллярного барьера и делает лёгочную ткань более уязвимой к ишемическим процессам. Другим фактором риска является высокий рост, хотя механизм этой связи до конца не изучен. Ожирение, наоборот, связано с меньшей вероятностью инфаркта лёгкого от ТЭЛА, что может объясняться особенностями распределения кровотока[2].
Возраст и состояние сердечно-сосудистой и лёгочной систем играют ключевую роль в этиологии инфаркта лёгкого. Молодые пациенты (в среднем около 40 лет), не имеющие хронических сердечно-сосудистых и лёгочных заболеваний, чаще сталкиваются с инфарктом лёгкого, особенно на фоне ТЭЛА. Это связано с недостаточным развитием бронхиального коллатерального кровообращения, которое могло бы компенсировать ишемию. У пациентов с хроническими заболеваниями сердца и лёгких, напротив, лучше развита сосудистая сеть, которая формируется в ответ на длительную гипоксию, что защищает лёгочную ткань от инфаркта даже при острой тромбоэмболии. Современные исследования показывают, что хроническая гипоксия у таких пациентов стимулирует коллатеральный ангиогенез, что снижает вероятность ишемического повреждения[2][3].
Серповидноклеточная анемия также играет двойную роль в этиологии инфаркта лёгкого. С одной стороны, это заболевание само по себе может приводить к инфаркту из-за образования серповидных эритроцитов, которые блокируют микроциркуляцию в лёгких. С другой стороны, при ТЭЛА серповидноклеточная анемия усиливает ишемические процессы, поскольку гипоксия и вазоконстрикция усугубляют деформацию эритроцитов и их ретенцию в лёгочных капиллярах[3].
Патофизиология
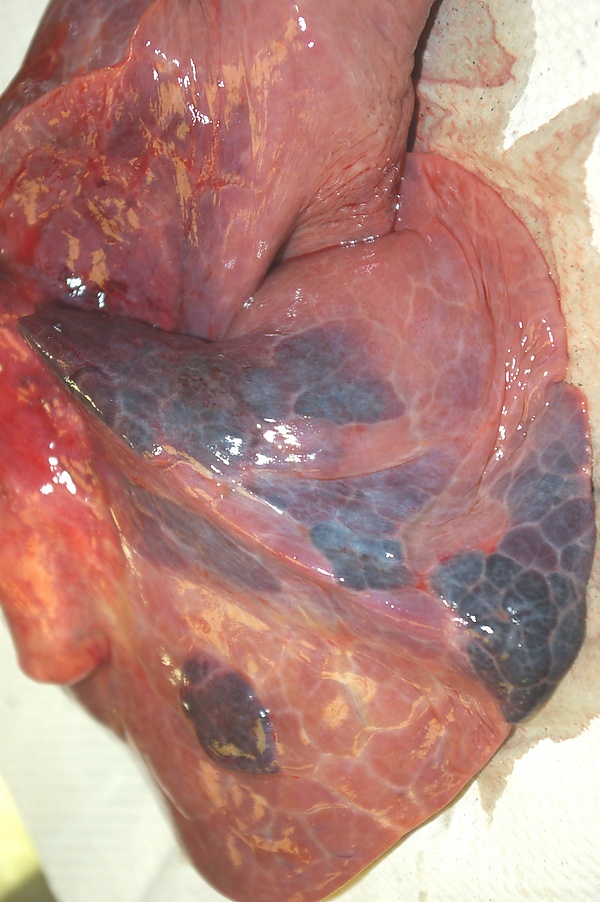
Лёгкие обладают двойным кровоснабжением: дезоксигенированная кровь поступает из лёгочных артерий, а насыщенная кислородом — из бронхиальных артерий. Бронхиальное кровообращение снабжает стенки бронхов, висцеральную плевру и паренхиму лёгких, а также поддерживает перфузию через анастомозы с лёгочными сосудами. При ТЭЛА ишемия возникает в участках, где коллатеральное кровоснабжение недостаточно. Ишемия вызывает повышение сосудистой проницаемости и экстравазацию эритроцитов в альвеолы. Первоначально это проявляется как внутриальвеолярное кровоизлияние («неполный инфаркт»), которое в некоторых случаях может быть обратимым. Если кровь не резорбируется, развивается некроз ткани и формируется истинный инфаркт. Хроническая венозная гипертензия и нарушенный кровоток в бронхиальных артериях, например, при сердечной недостаточности, ухудшают резорбцию крови и способствуют прогрессированию некроза. Инфаркт лёгкого чаще всего локализуется в субсегментарных ветвях лёгочных артерий (<3 мм) и прилегает к плевре[3].
Ишемия лёгочной ткани также сопровождается воспалительной реакцией, которая приводит к вазоконстрикции, нарушению микроциркуляции и дальнейшему повреждению эндотелиального барьера. Поскольку альвеолы остаются вентилируемыми, гипоксия эндотелиальных клеток усугубляется локальной гиперперфузией из бронхиального кровообращения. Это повышает проницаемость сосудов, вызывает кровоизлияние и усиливает повреждение[3].
Инфаркт лёгкого развивается вследствие сочетания факторов: сосудистой обструкции, нарушения коллатерального кровотока, капиллярной ишемии и воспалительной реакции, которая ухудшает газообмен и ведёт к некрозу ткани[3].
Клиническая картина
Основным симптомом является острая боль в грудной клетке, которая часто локализуется на стороне поражения. Боль усиливается при вдохе, кашле или движениях. Одышка развивается внезапно, пациент ощущает нехватку воздуха, даже в покое, её интенсивность нарастает при физической нагрузке. Кашель может быть сухим или сопровождаться кровянистой мокротой (кровохарканье), что связано с разрывом мелких сосудов в области некроза. Часто наблюдается повышение температуры тела до субфебрильных или фебрильных значений, связанное с воспалительной реакцией. У некоторых пациентов наблюдается цианоз, то есть посинение кожи и слизистых, особенно губ и носогубного треугольника, из-за недостатка кислорода в крови. Общая слабость и головокружение могут сопровождаться потливостью, нитевидным пульсом и низким артериальным давлением, что указывает на гипоксию и снижение сердечного выброса. В тяжёлых случаях возможна потеря сознания. Тахикардия, возникает как компенсаторная реакция на снижение уровня кислорода в тканях. Иногда симптомы осложняются плевритом, что сопровождается шумом трения плевры, усиливающим боль в грудной клетке. Инфаркт может также сопровождаться инфарктной пневмонией, проявляющейся кашлем с выделением мокроты и более выраженной лихорадкой[2][6][7].
Диагностика
Диагностика инфаркта лёгкого основывается на клинических данных, инструментальных и лабораторных исследованиях.
В клиническом анализе крови выявляется лейкоцитоз и увеличение СОЭ. В биохимическом анализе крови: повышение уровня D-димера свидетельствует о тромбообразовании, однако тест не специфичен; повышение уровня С-реактивного белка; возможно повышение уровня ЛДГ. При исследовании газов крови выявляют гипоксемию[7].
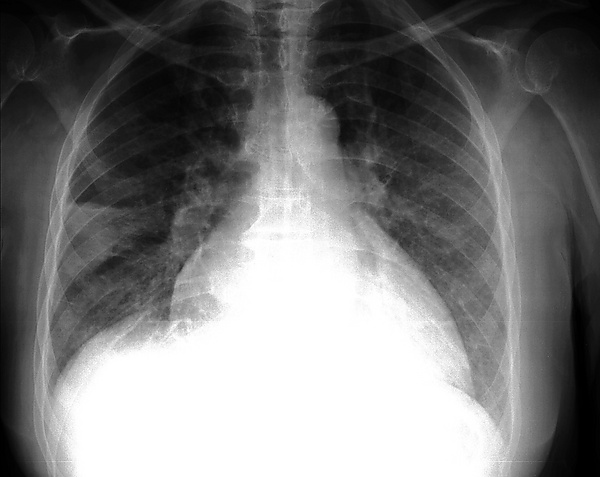
Рентгенография грудной клетки при инфаркте лёгкого позволяет выявить характерные, но не всегда специфичные признаки. Наиболее типичным является горб Хэмптона — клиновидное уплотнение с основанием, прилегающим к плевре, и вершиной, направленной к корню лёгкого. Также возможно выявление ателектаза с высоким стоянием диафрагмы и небольшого одностороннего плеврального выпота[3].
Затемнение на рентгенограмме обычно имеет треугольную форму, но при инфильтрации окружающих тканей может становиться округлым или неправильным. В некоторых случаях определяется горизонтальная тень на 2-3 см выше диафрагмы. Возможны также признаки лёгочного сердца, такие как выбухание лёгочного ствола, расширение правых отделов сердца и верхней полой вены[7].
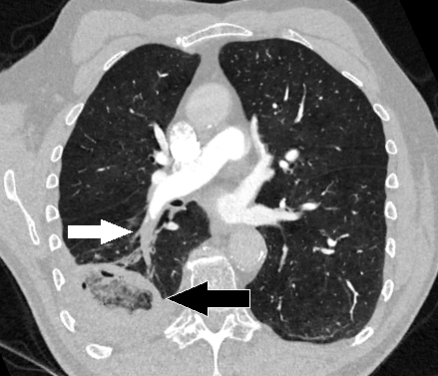
КТ является основным методом диагностики при подозрении на инфаркт лёгкого. На КТ инфаркт лёгкого часто проявляется как периферическая клиновидная консолидация. Также на КТ можно выявить очаги с уменьшенным контрастированием что связано с нарушением лёгочной перфузии. При некротическом инфаркте лёгкого выявляется специфический радиологический признак — обратный знак ореола. Он проявляется как кольцеобразное затемнение с центральным участком пониженной плотности, окружённое более плотной тканью. Также на КТ могут быть обнаружены плевральный выпот и ателектаз. Новые методы, такие как двухэнергетическая КТ, позволяют более точно выявить периферические окклюзии и изменения, характерные для инфаркта лёгкого[3].
Признаки перегрузки правых отделов сердца:
- отклонение электрической оси сердца вправо;
- признаки правожелудочковой недостаточности (S1-Q3-T3) — синдром Мак—Джина—Уайта;
- тахикардия[3].
Позволяет выявить наличие тромбов в лёгочных артериях, включая мелкие ветви, определить уровень поражения, оценить степень закупорки артерий, оценить кровоток в лёгочной сосудистой системе. Используется редко в связи с инвазивностью метода[3].
ЭхоКГ позволяет выявить перегрузку правого желудочка, расширение правых отделов сердца, тромбы в правом желудочке или предсердии, повышение давления в лёгочной артерии[3].
Применяется для оценки кровотока в лёгких. При инфаркте лёгкого или ТЭЛА выявляются зоны сниженной перфузии. Этот метод используется, если КТ противопоказана[3].
Дифференциальная диагностика
- Тромбоэмболия лёгочной артерии
- Инфекционный эндокардит
- Острый грудной синдром при серповидно-клеточной анемии
- Артериовенозная мальформация
- Злокачественная опухоль
- ДВС-синдром
- Диффузное альвеолярное кровотечение
- Амилоидоз
- Лёгочная инфекция, например, пневмония или аспергиллёз
- Васкулиты
- Инструментальные вмешательства, например, эмболизация бронхиальной артерии, катетерная абляция[2]
Лечение
При подозрении на ТЭЛА пациента необходимо немедленно госпитализировать в отделение интенсивной терапии, так как задержка в лечении значительно повышает риск летального исхода. На догоспитальном этапе вводится гепарин (10 000 ЕД) для предотвращения роста тромба. Для купирования болевого синдрома применяются анальгетики: ненаркотические — внутривенно при умеренной боли и наркотические анальгетики при сильной боли для устранения одышки и снижения нагрузки на сердце[6][7].
В стационаре продолжают кислородную поддержку через назальные катетеры или маску. В случае тяжёлой гипоксии используется искусственная вентиляция лёгких. Антикоагулянтная терапия начинается с введения гепарина внутривенно, который устраняет спазмы сосудов и бронхов, улучшая кровообращение. Гепаринотерапия длится 7-10 дней, после чего назначаются пероральные антикоагулянты, например, варфарин или фениндион, для предотвращения дальнейшего тромбообразования. При менее тяжёлых формах ТЭЛА применяются низкомолекулярные гепарины, например, эноксапарин натрия или надропарин кальция[6][7].
Тромболитическая терапия, направленная на разрушение тромба, включает использование препаратов, например, стрептокиназа, урокиназа или альтеплаза. Она наиболее эффективна в первые 3-5 дней от начала заболевания. Раннее введение тромболитиков улучшает прогноз заболевания. Если медикаментозное лечение неэффективно, проводится хирургическая тромбэктомия[6][7].
При плевральной боли, возникающей во время дыхания или кашля, вводится 50 % раствор метамизола натрия. Спазмы сосудов и бронхов купируются с помощью спазмолитиков, например, дротаверин, папаверин, или аминофиллина[6][7].
Для лечения шока применяются вазопрессоры, такие как допамин, добутамин. При гипотонии вводятся преднизолон и декстран, при этом тромболитики и антикоагулянты строго противопоказаны[6].
Антибиотикотерапия проводится для предотвращения инфекционных осложнений. Назначаются препараты широкого спектра действия: цефтриаксон, амоксициллин, азитромицин или ципрофлоксацин. Сердечные гликозиды используются для поддержки сердечной деятельности[6].
Для профилактики повторных эмболий устанавливают кава-фильтр в нижнюю полую вену, который предотвращает попадание тромбов в системный кровоток. Также назначаются антиагреганты для снижения риска тромбообразования[6].
Прогноз
Прогноз зависит от своевременности диагностики и лечения. При раннем выявлении и адекватной терапии прогноз благоприятный. Без соответствующей терапии или при позднем начале терапии возможно развитие тяжёлых осложнений[6].
Осложнения
- Вторичное инфицирование с абсцедированием поражённой области
- Кавитация лёгких в зоне некроза
- Бронхоплевральная фистула
- Эмпиема плевры
- Пневмоторакс
- Лёгочное кровотечение
- Постинфарктная пневмония
- Ателектаз
- Гангрена лёгкого
- Гнойный плеврит
- Лёгочный фиброз
- Рубцевание
- Лёгочная гипертензия
- Сепсис
- Правожелудочковая сердечная недостаточность
- Отёк лёгких[3][6][7]
Профилактика
Профилактика направлена на предотвращение тромбообразования и улучшение кровообращения. Основные меры:
- массаж ног,
- компрессионная терапия,
- ранняя активизация больных,
- профилактика инфекционных заболеваний,
- своевременное лечение тромбофлебита,
- контроль факторов риска[6][8].
Примечания
Литература
Фтизиатрия. — С. 256.