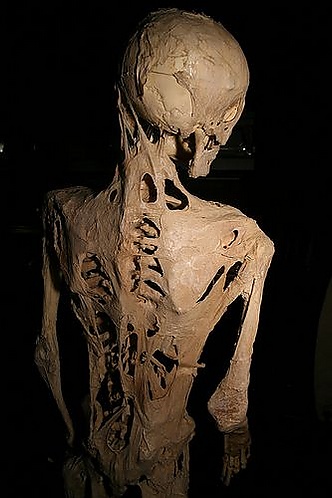
Фибродисплазия оссифицирующая прогрессирующая
Фибродисплази́я оссифици́рующая прогресси́рующая (ФОП; прогресси́рующий оссифици́рующий миози́т, синдро́м ка́менной боле́зни, параосса́льная гетеротопи́ческая оссифика́ция и боле́знь Мюнхе́ймера) представляет собой редкое генетическое заболевание из группы нарушений, связанных с гетеротопической оссификацией, обусловленное мутацией в гене ACVR1. ФОП наследуется аутосомно-доминантно с полной пенетрантностью. Патология характеризуется прогрессирующим формированием качественно нормальной костной ткани в нехарактерных для этого местах, таких как соединительная ткань, мышцы и связки, что происходит по механизму эндохондрального окостенения уже после рождения. Типичным признаком заболевания является врождённая деформация больших пальцев стоп. Течение болезни сопровождается обострениями, которые чаще всего провоцируются травмами или перенесёнными вирусными инфекциями, и в такие периоды происходит образование новых очагов гетеротопической кости. На сегодняшний день этиологическое лечение, направленное на устранение причины заболевания, не разработано[2][3].
Общие сведения
История
Первые описания случаев заболевания ФОП относятся к концу семнадцатого века, когда в 1692 году его описал Ги Патен, а позднее, в 1739 году, Джон Фрике. В 1918 году Дж. Розенштирн опубликовал обзор медицинской литературы, обобщив данные уже о 115 случаях этой патологии. Первоначально болезнь получила название «прогрессирующий оссифицирующий миозит», что подчёркивало роль мышечного воспаления в процессе последующего окостенения. Однако в дальнейшем выяснилось, что патологический процесс не ограничивается мышцами, а распространяется на соединительную ткань, включая суставные капсулы, связки и фасции. Это потребовало пересмотра терминологии, и в 1970 году Виктор Маккьюсик предложил новое, более точное название — «фибродисплазия оссифицирующая прогрессирующая», которое используется по сей день. В России первое клиническое описание данного заболевания было представлено в 2014 году в работе Н. А. Коваленко-Клычковой с соавторами[2].
Этиология
ФОП вызвано соматической миссенс-мутацией de novo в гене рецептора активина типа 1 (ACVR1), который также известен как рецепторная киназа, подобная активину 2. Этот ген кодирует рецептор, участвующий в сигнальном пути костных морфогенетических белков. Наиболее распространённым вариантом, встречающимся примерно у 97 процентов пациентов, является мутация R206H в глицин-сериновом активационном домене гена. Данный патогенный вариант усиливает передачу сигналов путей, связанных с костными морфогенетическими белками, что направляет дифференцировку мезенхимальных стволовых клеток в хондрогенном и остеогенном направлениях, приводя к формированию гетеротопической костной ткани в мышцах, сухожилиях, связках, фасциях и апоневрозах. Наследование патогенного варианта гена ACVR1 происходит по аутосомно-доминантному типу, при этом ген может передаваться как по материнской, так и по отцовской линии, также описан случай материнского мозаицизма[2][4].
Патогенез
Патогенез ФОП обусловлен мутацией в гене рецептора активина первого типа, который участвует в сигнальном пути костных морфогенетических белков. Патогенный вариант гена повышает чувствительность рецептора к этим белкам, что ведёт к гиперактивности сигнального пути и изменению дифференцировки клеток-предшественников соединительной ткани в остеогенном направлении. В ответ на повреждение тканей, часто спровоцированное травмой или воспалением, в поражённой области развивается локальная фибробластическая пролиферация с образованием лимфоцитарного инфильтрата, состоящего из макрофагов и фибробластов. Эта инфильтрация предшествует некрозу мышечных волокон. Вслед за воспалительной фазой наступает фибропролиферативная реакция, сопровождающаяся ангиогенезом, после чего фибропролиферативная ткань подвергается аваскулярной конденсации с формированием хряща. Завершающим этапом является реваскуляризация и эндохондральное окостенение, приводящее к образованию зрелой пластинчатой кости с элементами костного мозга[2].
Ключевую роль в этом процессе играет дисбаланс между костным морфогенетическим белком BMP-4 и его антагонистами. У пациентов с ФОП наблюдается избыточная продукция BMP-4 и недостаточная выработка подавляющих его факторов, таких как ноггин и гремлин. В норме активация BMP-4 запускает механизм отрицательной обратной связи, ограничивающий остеогенез, однако при данном заболевании этот механизм нарушен, что приводит к непрерывной стимуляции образования костной ткани[2].
Гистологически процесс характеризуется последовательной сменой стадий: периваскулярная лимфоцитарная инфильтрация Т- и В-клетками, мышечный некроз, фибропролиферация с неоваскуляризацией, формирование хрящевой ткани и её последующее замещение костной. Образующаяся гетеротопическая кость гистологически идентична нормальной скелетной кости и содержит костномозговые элементы[2].
Эпидемиология
По оценкам международных экспертов, распространённость ФОП в 2011 году составляла один случай на два миллиона населения, в то время как популяционная частота ФОП оценивается как 0,61 случая на один миллион населения, что эквивалентно одному случаю на 1,65 миллиона человек. Предрасположенность к данному заболеванию в различных этнических группах, расах и географических зонах ранее не изучалась. Некоторые исследования указывают на возможное преобладание мужчин (по данным некоторых источников соотношение 4:1), однако другие данные свидетельствуют об отсутствии значимых различий между полами[2][5].
Диагностика
При рождении дети с ФОП выглядят абсолютно здоровыми, за исключением характерной врождённой деформации больших пальцев стоп, которая служит важным диагностическим признаком. В течение первых десяти лет жизни у детей возникают спорадические эпизоды болезненных припухлостей мягких тканей, которые нередко ошибочно принимают за опухолевые образования. Некоторые из этих эпизодов могут спонтанно регрессировать, однако в большинстве случаев они запускают процесс трансформации скелетных мышц, сухожилий, связок, фасций и апоневрозов в гетеротопическую костную ткань по механизму эндохондральной оссификации. Образующиеся оссификаты охватывают суставы, вызывая их полное обездвиживание[2].
Процесс гетеротопической оссификации имеет характерную последовательность: он дебютирует в дорсальных, аксиальных, краниальных и проксимальных отделах тела, а затем распространяется на вентральные, аппендикулярные, каудальные и дистальные области. Важно отметить, что любые попытки хирургического удаления сформировавшейся гетеротопической кости приводят к новым, ещё более тяжёлым обострениям. Провоцирующими факторами новых обострений могут выступать механические травмы, повреждения мягких тканей, растяжения мышц, физическое перенапряжение, внутримышечные инъекции, стоматологические вмешательства, падения и вирусные инфекции. Иммобилизация пациентов носит накопительный характер, и большинство из них становятся прикованными к инвалидному креслу уже к концу второго десятилетия жизни[2][6].
Важной особенностью является то, что диафрагма, язык, глазодвигательные мышцы, миокард и гладкая мускулатура не вовлекаются в патологический процесс. На ранних стадиях заболевания нередко обнаруживается ригидность шейного отдела позвоночника, предшествующая появлению оссификатов в этой области. Аномалии шейного отдела включают крупные оссификаты по задней поверхности, высокие и узкие тела позвонков, слияние фасеточных суставов, причём шейный отдел часто анкилозируется уже в раннем возрасте. Помимо деформации больших пальцев стоп, к другим скелетным особенностям относятся клинодактилия, короткая и широкая шейка бёдра, а также проксимальные медиальные остеохондромы большеберцовой кости[2].
Выделяют также особые формы заболевания. У некоторых пациентов с классическими признаками ФОП наблюдаются нетипичные особенности, что классифицируется как синдром ФОП-плюс. К таким атипичным проявлениям относятся внутрисуставной синовиальный остеохондроматоз бедренных костей, дегенеративное поражение тазобедренных суставов, поредение волос на голове, лёгкие когнитивные нарушения, выраженная задержка роста, катаракта, отслойка сетчатки, глаукома, краниофарингиома, сохранение молочных зубов во взрослом возрасте, аномалии мозжечка, церебральная дисфункция с судорогами, полиостотическая фиброзная дисплазия, первичная аменорея, апластическая анемия, гипоспадия и церебральные каверномы. Существуют также варианты заболевания с атипичным течением, например, с отсутствием характерных деформаций больших пальцев стоп или с тяжёлыми пороками развития стоп[2].
Молекулярно-генетический анализ может быть выполнен двумя способами[7]:
- секвенирование гена ACVR1 для выявления наиболее распространённого патогенного варианта, а также других миссенс-вариантов, ассоциированных с фибродисплазией оссифицирующей прогрессирующей;
- в качестве альтернативы может использоваться мультигенная панель, включающая ACVR1 и другие гены, представляющие интерес в рамках дифференциальной диагностики.
Рентгенография костей скелета: характерными признаками ФОП являются пороки развития суставов, особенно больших пальцев стоп. К ним относятся двусторонняя вальгусная деформация, деформация первой плюсневой кости, а также отсутствие или сращение межфалангового сустава. Кроме того, на рентгенограммах отчётливо визуализируются участки оссификации мягких тканей[2][7].
При проведении компьютерной и магнитно-резонансной томографии можно обнаружить параоссальные поражения и так называемые молодые, то есть недавно сформировавшиеся, очаги гетеротопической оссификации. В то время как стандартное рентгенологическое исследование лучше всего выявляет уже полностью сформировавшиеся и зрелые участки патологического костеобразования[2].
При пренатальном ультразвуковом исследовании вальгусная деформация большого пальца стопы может быть выявлена уже на сроке беременности двадцать три недели[7].
Аудиометрия: возможно выявление кондуктивной тугоухости[8].
Дифференциальная диагностика
Дифференциальная диагностика ФОП проводится со следующими заболеваниями[7][8]:
- наследственные множественные остеохондромы;
- прогрессирующая оссифицирующая гетероплазия;
- метахондроматоз;
- брахидактилия тип b1;
- ювенильный фиброматоз;
- педиатрическая остеосаркома.
Осложнения
Прогрессирующая иммобилизация может осложняться значительной потерей массы тела вследствие анкилозирования челюсти, что затрудняет питание. Развитие пневмонии и правожелудочковой сердечной недостаточности связано с синдромом дыхательной недостаточности, обусловленным деформацией грудного отдела позвоночника и грудной клетки. В период обострений может наблюдаться отёк конечностей, иногда выраженный настолько, что приводит к внесосудистой компрессии нервов и лимфатических сосудов. У некоторых пациентов с поражением нижних конечностей развиваются венозный застой и лимфедема. Снижение слуха обычно носит кондуктивный характер из-за оссификации структур среднего уха, однако у части пациентов оно является нейросенсорным вследствие вовлечения внутреннего уха, улитки или слухового нерва[2].
Лечение
Лечение ФОП направлено преимущественно на предотвращение обострений, контроль симптомов и повышение качества жизни пациентов, что включает также обучение и консультирование самих пациентов и членов их семей. Ведение детей с этим диагнозом должно осуществляться после консультации с врачом, компетентным в отношении данной патологии. Согласно клиническим рекомендациям, все медикаментозные препараты, используемые при ФОП, подразделяются на три класса в зависимости от их назначения и доказательной базы. К первому классу относятся средства, широко применяемые для контроля симптомов обострений, таких как отёк и болевой синдром, а именно глюкокортикостероиды и нестероидные противовоспалительные препараты. Второй класс составляют препараты, применение которых теоретически обосновано их воздействием на патогенетические механизмы заболевания, однако они одобрены для лечения других состояний. К ним относятся бисфосфонаты, стабилизаторы мембран тучных клеток, антилейкотриеновые средства и специфические ингибиторы тирозинкиназы. Лекарственные средства этой группы могут применяться с осторожностью по решению врачебной комиссии. Третий класс включает экспериментальные и незарегистрированные лекарственные средства, которые проходят исследования или используются в рамках клинических испытаний, такие как селективные ингибиторы сигнальной трансдукции, моноклональные антитела и агонисты определённых рецепторов. В перспективе разработка новых методов лечения направлена на воздействие на ключевые патогенетические звенья, включая блокировку сигнальных путей, таргетное воздействие на ферменты, участвующие в дифференцировке клеток, а также регуляцию транскрипционных факторов. В настоящее время проводятся клинические испытания ряда перспективных препаратов, среди которых агонисты определённых рецепторов, моноклональные антитела и ингибиторы клеточной сигнализации. Имеются также описания случаев успешного экспериментального лечения с использованием ингибиторов интерлейкина, что позволило достичь снижения частоты обострений заболевания[2][9].
Прогноз
По мере накопления гетеротопической костной ткани при ФОП происходит прогрессирующая утрата объёма движений, что приводит к практически полной обездвиженности. У пациентов с ФОП развивается синдром торакальной недостаточности, который может вызывать угрожающие жизни осложнения. Пневмония и правожелудочковая сердечная недостаточность являются основными угрожающими жизни состояниями, возникающими в результате этого синдрома. Средняя продолжительность жизни пациентов составляет приблизительно сорок один год, и летальный исход часто наступает вследствие осложнений синдрома торакальной недостаточности[8].
Диспансерное наблюдение
Профилактика
В рамках вторичной профилактики ФОП важное значение имеет предотвращение факторов, способных спровоцировать обострение заболевания. Поскольку падения могут приводить к обострениям, стратегии их предотвращения включают ограничение видов деятельности, сопряжённых с высоким риском падений, оборудование жилых помещений поручнями и другими приспособлениями, а также использование головных уборов для смягчения удара при возможном падении[2].
Учитывая, что вирусные инфекции также способны провоцировать обострения, необходимо соблюдение гигиенических мер, направленных на профилактику заражения. Вопросы вакцинации решаются индивидуально, исходя из соотношения потенциальной пользы и риска для конкретного пациента, при этом оценивается вероятность провокации обострения, риск заражения вакциноуправляемой инфекцией и количество доз вакцины, полученных до дебюта заболевания. При принятии решения о проведении иммунизации соблюдаются определённые правила: вакцины не вводятся во время обострения и в течение шести-восьми недель после него, их введение противопоказано вблизи суставов или мышц с уже сформировавшимися оссификатами, а также категорически исключается внутримышечный способ введения вакцин[2].
Примечания
Литература
- Kaplan F. S., Al Mukaddam M., Baujat G., et al. Medical guidelines for fibrodysplasia ossificans progressiva (англ.) // JBMR Plus. — 2025. — 19 September (vol. 9, no. 11). — P. ziaf150. — doi:10.1093/jbmrpl/ziaf150.
- Anwar S., Yokota T. Navigating the Complex Landscape of Fibrodysplasia Ossificans Progressiva: From Current Paradigms to Therapeutic Frontiers (англ.) // Genes. — 2023. — Vol. 14, no. 12. — P. 2162. — doi:10.3390/genes14122162.
- Sun D., Liu P., Wang Z., et al. Fibrodysplasia ossificans progressiva: A rare disease with spinal deformity and severe hip dysfunction (англ.) // Frontiers in Pediatrics. — 2022. — Vol. 10. — P. 981372. — doi:10.3389/fped.2022.981372.
- Сермягина И. Г., Баязутдинова Г. М., Браславская С. И., и др. Молекулярные причины прогрессирующей оссифицирующей фибродисплазии у российских пациентов // Медицинская генетика. — 2018. — Т. 17, № 2. — С. 35—38. — doi:10.25557/2073-7998.2018.02.35-38.
- Кораблёва Н. Н., Берестнев Е. В., Киселёв С. М., и др. Фибродисплазия оссифицирующая прогрессирующая: литературный обзор и описание клинического случая // Вопросы современной педиатрии. — 2022. — Т. 21, № 6S. — С. 558—569. — doi:10.15690/vsp.v21i6S.2482.