Тетрахлорметан
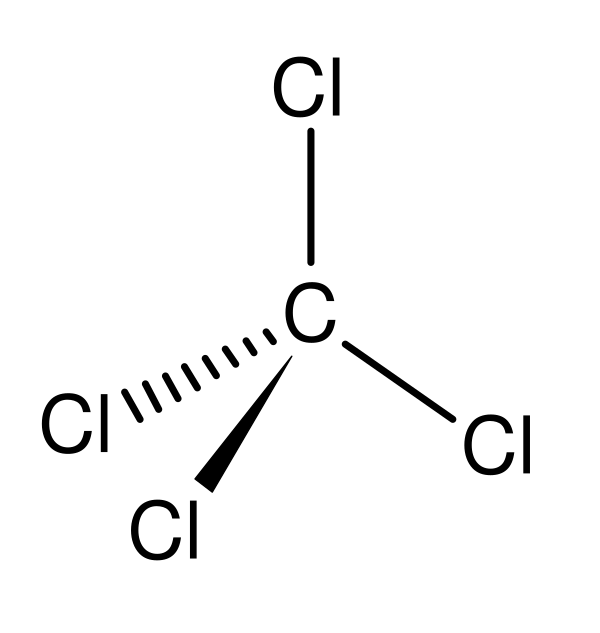
Тетрахлорид углерода (четырёххлóристый углерóд, фреóн-10, асорди́н, хладóн-10) — хлорорганическое соединение с химической формулой CCl4, галогеноалкан, бесцветная тяжёлая жидкость, по запаху напоминающая хлороформ (при сравнительно высокой концентрации имеет неприятный запах хлора). Негорюч и невзрывоопасен. Плохо растворяется в воде, смешивается с большинством органических растворителей.
Неагрессивен по отношению к алюминию и нержавеющей стали. Токсичен.
Общие сведения
| Тетрахлорид углерода | |
|---|---|
| Общие | |
| Систематическое наименование |
Тетрахлорметан, перхлорметан, хлорид углерода 4, тетрахлорид углерода |
| Сокращения | ЧХУ |
| Традиционные названия | четырёххлористый углерод, асордин |
| Хим. формула | CCl4 |
| Рац. формула | CCl4 |
| Физические свойства | |
| Состояние | жидкость с неприятным запахом |
| Молярная масса | 153,83 г/моль |
| Плотность | 1,5954 (при 20 °C) |
| Поверхностное натяжение | 26,43 ± 0,01[1] |
| Энергия ионизации | 11,47 ± 0,01[2] |
| Термические свойства | |
| Температура | |
| • плавления | −22,87 °C |
| • кипения | 76,75 °C |
| • вспышки | не воспламеняется °C |
| Критическая точка | 283,2 °C / 45 бар |
| Энтальпия | |
| • образования | −139,3 (298 К) кДж/моль |
| Давление пара | 91 ± 1[2] и 11,6 |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,08 (25 °C) |
| Оптические свойства | |
| Показатель преломления | 1,4607 (20 °C, для D-линии натрия) |
| Структура | |
| Дипольный момент | 0 Д |
| Классификация | |
| Рег. номер CAS | 56-23-5 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 5943 |
| UNII | CL2T97X0V0 |
| CompTox Dashboard EPA | DTXSID8020250 |
| Рег. номер EINECS | 200-262-8 |
| SMILES | |
| InChI | |
| RTECS | FG4900000 |
| ChEBI | 27385 |
| Номер ООН | 1846 |
| ChemSpider | 5730 |
| ECHA InfoCard | 100.000.239 |
| Безопасность | |
| Предельная концентрация | 20 мг/м³ |
| ЛД50 | 203 мг/кг (крысы, перорально) |
| Токсичность | токсичен |
| Пиктограммы ECB |
|
| NFPA 704 | |
Свойства
Тяжёлая бесцветная жидкость, имеющая резкий сладковатый запах. Молярная масса составляет 153,83 г/моль, плавится при −22,96 °C, кипит при 76,7 °C. Образует азеотроп с водой, в котором его содержится 95,9 %, имеющий температуру кипения 66 °C[3].
Тетрахлорметан химически инертен и не реагирует с воздухом, устойчив к воздействию света. При нагревании с водой до 250 °C происходит гидролиз: при недостатке воды образуется фосген, при избытке — хлор. В условиях нагрева до 500 °C превращается в смесь тетрахлорэтилена и гексахлорэтана с выделением свободного хлора[3].
Не реагирует с концентрированной серной кислотой, но взаимодействует с олеумом с образованием фосгена. Может быть восстановлен до хлороформа цинком и до метана металлами восьмой группы[3].
Гидролизуется водой при комнатной температуре в присутствии катализатора (Fe):
- .
Получение
В промышленности тетрахлорметан производят хлорированием, например, метана или хлорметана, нагревая их смесь с хлором до температуры 400—500 °C. При этой температуре происходит серия химических реакций, постепенно превращающих метан или метилхлорид в соединения с большим содержанием хлора:
Общая реакция:
Результатом процесса является смесь, состоящая из метилхлорида, дихлорметана, хлороформа и тетрахлорметана. Разделение веществ осуществляется ректификацией.
Основные сферы использования
Применяется как растворитель (жиров, смол, каучука и др.), для получения фреонов. С переменным успехом применялся как экстрагент, а также в медицинской практике.
Тетрахлорметан квалификации «эвс» используется для анализа водных сред на нефтепродукты методом инфракрасной спектроскопии.
Тетрахлорметан с 1930-х годов широко использовался в качестве наполнителя ручных и стационарных огнетушителей для военной, авиационной и другой техники (так называемый «тетрахлорный огнетушитель», в том числе с ручным приводом насоса), особенно до широкого распространения углекислотных, фреоновых и порошковых систем. Пары́ и продукты разложения тетрахлоруглерода не поддерживают горения, как тушащий агент он имеет много достоинств: жидкий при нормальных условиях, легко испаряется, при этом значительно охлаждая зону горения, неэлектропроводен, не требует для хранения сосудов высокого давления, не вызывает коррозии медных и лужёных сосудов, относительно инертен к обрабатываемым поверхностям (для использования в холодное время требуется добавка низкозамерзающих растворителей). Однако из-за токсичности продуктов разложения в гражданских системах применения не получил. Ручное тушение пожара в машине требовалось выполнять в противогазах — при попадании тетрахлоруглерода на горячие поверхности происходила химическая реакция частичного замещения хлора атмосферным кислородом с образованием фосгена — сильнодействующего ядовитого вещества удушающего действия.
Ранее применялся в качестве хладагента, но был запрещён к использованию для этой цели Монреальским протоколом 1987 года из-за разрушающего воздействия на озоновый слой[3].
Безопасность
При высоких температурах на воздухе он разлагается или горит, образуя ядовитый фосген. Это было распространённой проблемой, когда четырёххлористый углерод использовался в качестве огнетушителя[4] и сообщалось о смертях, вызванных его превращением в фосген.[5]
Четырёххлористый углерод предположительно является канцерогеном для человека, но достаточных доказательств его канцерогенности для человека нет.[6] Всемирная организация здравоохранения сообщает, что четыреххлористый углерод может вызывать гепатоцеллюлярную карциному (гепатомы) у мышей и крыс. Дозы, вызывающие опухоли печени у мышей и крыс, выше, чем дозы, вызывающие клеточную токсичность.[7] Международное агентство по изучению рака (МАИР) отнесло это соединение к группе 2B, «возможно канцерогенное для человека».[8]
Тетрахлорметан является одним из самых сильнодействующих гепатотоксинов (ядов для печени), настолько сильнодействующих, что он широко используется в научных исследованиях для оценки гепатопротекторных средств.[9] Воздействие высоких концентраций тетрахлорметана (в том числе паров) может повлиять на центральную нервную систему и привести к дегенерации печени и почек,[10] а длительное воздействие может привести к коме или смерти.[11] Хроническое воздействие тетрахлорметана может вызвать поражение печени[12][13] и почек, а также привести к раку.[14][15]
Употребление алкоголя усиливает токсическое действие тетрахлорметана и может вызвать более серьёзные повреждения органов, такие как острая почечная недостаточность, у людей, злоупотребляющих алкоголем. Дозы, которые могут вызвать лёгкое отравление у тех, кто не употребляет алкоголь, могут быть смертельными для тех, кто злоупотребляет алкоголем.[16]
Воздействие тетрахлорметана на здоровье человека и окружающую среду было оценено в рамках REACH в 2012 году в контексте оценки этого вещества во Франции.[17]
В 2008 году исследование распространённых чистящих средств выявило наличие тетрахлорметана в «очень высоких концентрациях» (до 101 мг/м3) в результате смешивания производителями поверхностно-активных веществ или мыла с гипохлоритом натрия (отбеливателем).[18]
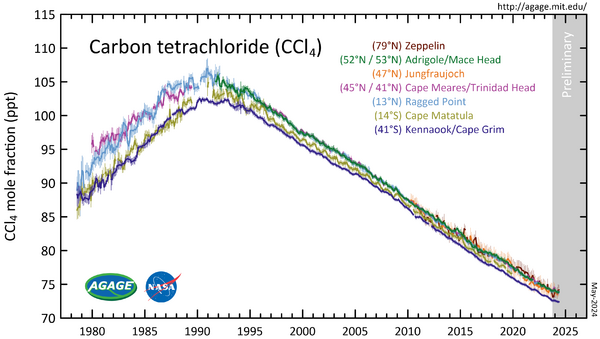
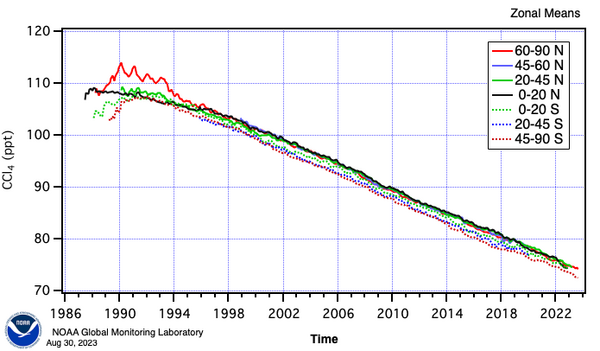
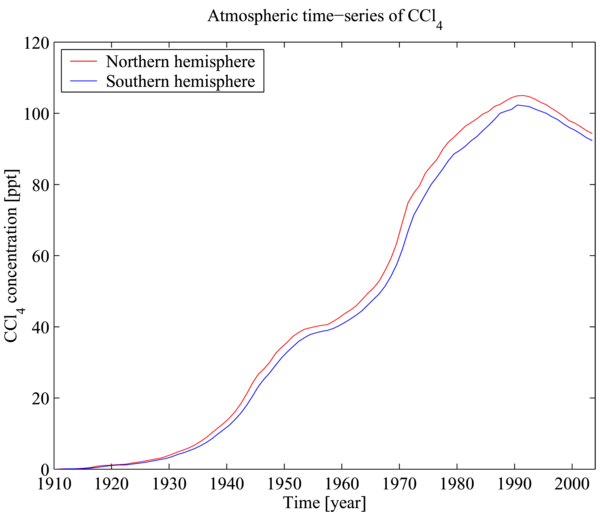
Тетрахлорметан также является озоноразрушающим веществом[19] и парниковым газом.[20] Однако с 1992 года[21] его концентрация в атмосфере снижается по причинам, описанным выше (см. графики концентрации в атмосфере в галерее). CCl4 имеет время жизни в атмосфере 85 лет.[22]
Галерея
Примечания
Литература
- Трегер Ю. А. Четыреххлористый углерод // Химическая энциклопедия : в 5 т. / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1998. — Т. 5: Триптофан — Ятрохимия. — С. 392—393. — 783 с. — 10 000 экз. — ISBN 5-85270-310-9.

![{\displaystyle {\ce {CCl4 + 2H2O ->[Fe] 4HCl\, ^ + CO2 ^}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/e7d6c9a086e536619054ac74af6c56de94cc0ba6)