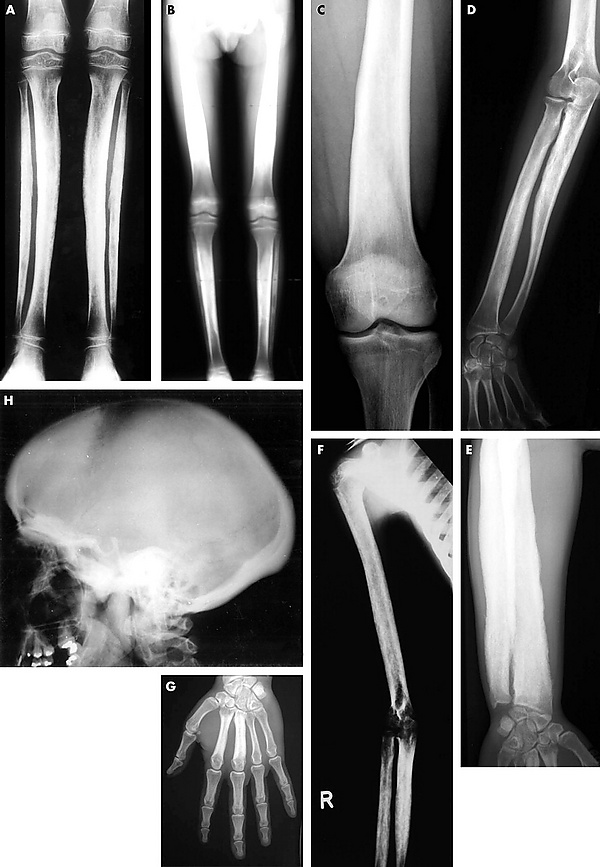
Болезнь Камурати — Энгельманна
Болезнь Камурати — Энгельманна — это редкое прогрессирующее заболевание, развитие которого связано с мутациями гена трансформирующего фактора роста бета-1. Эти мутации приводят к повышенному высвобождению активного фактора роста из костной ткани в процессе резорбции, что вызывает аномально высокую скорость ремоделирования и усиление костного обмена. Заболевание характеризуется генерализованным остеосклерозом, гиперостозом основания черепа и утолщением кортикального слоя диафизов трубчатых костей. Эти изменения провоцируют различные клинические проявления, такие как головные боли, глухота, паралич лицевого нерва и другие неврологические нарушения, схожие с симптомами других склерозирующих патологий костной системы[2].
Общие сведения
История
Первоначально заболевание было описано Кокейном в 1920 году. В 1922 году итальянский ортопед Камурати и позднее, в 1929 году, немецкий хирург и ортопед Энгельманн описали заболевание, проявляющееся в детском возрасте. Его характерными признаками были боли в костях конечностей, нарастающая мышечная слабость и атрофия мышц, своеобразная «утиная» походка, а также симметричное утолщение кортикального слоя длинных трубчатых костей. В медицинской литературе эта патология получила название болезни Камурати — Энгельманна (БКЭ)[3][4].
Этиология
Причина заболевания связана с мутациями в гене, кодирующем трансформирующий фактор роста бета-1 (TGFB1), расположенном на хромосоме 19 (участок 19q13.1). Этот фактор регулирует ключевые клеточные процессы: рост, размножение, дифференциацию, миграцию и апоптоз. Большинство мутаций (7/10) при БКЭ — это миссенс-мутации в экзоне 4, кодирующем участок, ответственный за гомодимеризацию. На их долю приходится 82,2 % всех известных мутаций. Остаточный аргинин в позиции 218 является «горячей точкой» мутаций, составляя 60 % случаев. Прочие мутации включают дупликацию 9 пар нуклеотидов в экзоне 1 (сигнальный пептид) и две миссенс-мутации в экзонах 1 и 2. Болезнь передаётся по аутосомно-доминантному типу наследования[3][4].
Патогенез
TGF-β1 регулирует рост и размножение клеток, их созревание и специализацию (дифференцировку), движение клеток, а также запрограммированную гибель клеток. Он играет ключевую роль в эмбриональном развитии, участвуя в формировании кровеносных сосудов, регуляции мышечной ткани, развитии жировой прослойки, заживлении ран и функционировании иммунной системы. Наибольшая концентрация этого белка наблюдается в костной ткани и внеклеточном матриксе, который обеспечивает структурную поддержку и питание окружающим клеткам. В норме TGF-β1 находится в неактивном состоянии и активируется только при поступлении соответствующего сигнала. Однако мутации в гене TGFB1, приводящие к БКЭ, вызывают постоянную активацию гена. Это приводит к повышенной минерализации костей, снижению объёма жировой и мышечной ткани и характерной клинической картине заболевания[5].
Эпидемиология
В медицинской литературе описаны преимущественно спорадические случаи заболевания. Оно встречается в разных этнических группах и не зависит от пола. Точная частота и распространённость болезни неизвестны, поскольку во многих случаях она протекает бессимптомно и выявляется случайно при рентгенологическом обследовании. Описано около 300 случаев СКЭ в возрасте от 1 года до 76 лет[4].
Диагностика
Клиническая картина
Заболевание проявляется не сразу после рождения ребёнка, а значительно позже. Дети начинают ходить сравнительно поздно — только на третьем или четвёртом году жизни, при этом иногда испытывают трудности при ходьбе. Во многих случаях наблюдается отставание в физическом развитии: дети растут худыми, бледными, плохо набирают вес, у них отмечается гипогонадизм. Нередко присутствуют общая слабость, мышечная слабость и сонливость. В остальном больные дети ничем не отличаются от сверстников и имеют нормальный внешний вид[4].
Поражение костей развивается медленно и прогрессирует с течением времени, отличаясь разнообразием проявлений — от бессимптомных форм до выраженных случаев с болевым синдромом, деформациями конечностей и контрактурами суставов. Боли в костях встречаются в 94 % случаев и описываются пациентами как постоянные, ноющие. Характерно усиление боли при физической активности, стрессе или переохлаждении. У детей младшего возраста гиперостоз чаще носит несимметричный, очаговый характер: участки с утолщением кортикального слоя чередуются с неизменёнными зонами. С возрастом гиперостоз становится симметричным и генерализованным. В 52 % случаев утолщение диафизов можно обнаружить при пальпации. Иногда поражённые сегменты конечностей приобретают цилиндрическую форму. Возможны сгибательные контрактуры в тазобедренных и коленных суставах. К проявлениям болезни также относятся сглаженность поясничного лордоза, кифоз, сколиоз, плоскостопие. Из-за увеличения минеральной плотности кости риск переломов в поражённых областях снижается, однако в случае перелома консолидация может протекать медленнее[4].
Склероз отверстий черепных нервов может приводить к их непосредственному сдавлению или нейроваскулярным нарушениям. Дефицит черепных нервов наблюдается у 38 % пациентов. Наиболее распространённые нарушения включают потерю слуха, проблемы со зрением и паралич лицевого нерва. Кондуктивная тугоухость может быть вызвана сужением наружного слухового прохода, костным сдавлением слуховых косточек или сужением овального и круглого окон. Нейросенсорная тугоухость возникает вследствие сужения внутреннего слухового прохода и компрессии улиткового нерва или сосудов. Нейросенсорная тугоухость также может развиться после попыток хирургической декомпрессии лицевого нерва[6].
Вестибулярные нарушения, включая шум в ушах и головокружение, также были зарегистрированы у некоторых пациентов[6].
Поражение глазницы может приводить к нечёткости зрения, экзофтальму, отёку диска зрительного нерва, слезотечению, глаукоме, подвывиху глазного яблока и отслойке сетчатки[6].
Гиперостоз свода черепа может вызывать повышение внутричерепного давления, хронические (иногда выраженные) головные боли и лобный бугор[6].
Гипопитуитаризм был описан у ряда пациентов, проявляясь низкорослостью, задержкой полового развития и гипокортицизмом. Развитие гипопитуитаризма связывают с остеосклерозом основания черепа, приводящим к уменьшению размеров турецкого седла и сдавлению гипофиза на фоне внутричерепной гипертензии. Кроме того, гипопитуитаризм может быть следствием прямого воздействия TGFB1 на гипофиз[6].
Гипотиреоз встречается редко и может развиваться как вследствие поражения гипофиза, так и в результате аутоиммунного тиреоидита[6].
Лабораторная диагностика
При клиническом и биохимическом анализе крови не определяются специфические изменения[4].
Инструментальная диагностика
- гиперостоз одной или нескольких длинных костей начинается в области диафизов и может распространяться на метафизы, редко затрагивая эпифизы. Гиперостоз обычно симметричный в конечностях, но в некоторых случаях бывает асимметричным. Он начинается в области передней и средней черепных ямок и часто распространяется на лобную кость;
- вовлечение надкостницы приводит к неравномерному утолщению кортикального слоя и увеличению диаметра кости;
- эндостальный склероз может вызывать сужение костномозгового канала;
- умеренный остеосклероз наблюдается в задней дуге позвонков и некоторых плоских костях, соответствующих по структуре диафизам[6].
Поражённые участки демонстрируют повышенное накопление радиофармпрепарата технеция-99m при сцинтиграфии скелета, что отражает усиленную остеобластическую активность[7].
Дифференциальная диагностика
Дифференциальная диагностика проводится со следующими состояниями[5][7]:
- Болезнь ван Бюхена — наследственное заболевание с прогрессирующим гиперостозом черепа и кортикальным утолщением длинных костей.
- Остеопетроз.
- Болезнь Риббинга.
- Синдром Кенни-Коффи 2-го типа — редкое генетическое заболевание, характеризующееся задержкой роста, гипокальциемией и утолщением кортикального слоя костей.
- Ювенильная болезнь Педжета.
Лечение
Медикаментозное лечение
Основой медикаментозной терапии являются глюкокортикостероиды, которые обладают противовоспалительным и иммуносупрессивным действием. В костной ткани они снижают плотность костей: во-первых, увеличивая апоптоз остеобластов и остеоцитов, подавляя пролиферацию и дифференцировку остеобластов, а также синтез костного матрикса; во-вторых, усиливая пролиферацию и дифференцировку предшественников остеокластов; в-третьих, уменьшая всасывание кальция в кишечнике. Несмотря на положительные эффекты, длительная терапия глюкокортикоидами не рекомендуется из-за риска задержки роста у детей и остеопороза. Поэтому важно подбирать минимально эффективную дозу[3].
Применение бисфосфонатов при БКЭ остаётся спорным. В некоторых случаях они усугубляли течении болезни, в других — приносили временное облегчение[3].
Нестероидные противовоспалительные препараты, такие как аспирин, могут уменьшать боль, но не влияют на костные изменения[3].
Хирургическое лечение
Альтернативой медикаментозной терапии является хирургическое вмешательство. Избыточный рост костной ткани в диафизах, сужение костномозгового канала и деформации могут корректироваться с помощью остеотомии. Однако, учитывая прогрессирующий характер заболевания, симптомы со временем могут рецидивировать[3].
Диспансерное наблюдение
Пациентам с БКЭ показана оценка[6]:
- двигательных функции: оценка развития крупной моторики у детей, контроль подвижности, мышечной слабости, контрактур и костных болей на каждом приёме;
- активности болезни: при острых костных болях — остеосцинтиграфия для оценки активности процесса;
- состояния костной системы: ежегодная денситометрия для пациентов, получающих кортикостероидную терапию;
- неврологического статуса: ежегодный неврологический осмотр с оценкой черепно-мозговых нервов и жалоб на головные боли. Контроль признаков внутричерепной гипертензии на каждом визите. При склерозе основания черепа с неврологической симптоматикой — компьютерная томография головы и шеи для определения объёма поражения и планирования возможного хирургического вмешательства;
- физического развития: регулярная оценка роста и полового созревания в детском возрасте.
Прогноз
Прогноз для жизни у пациентов с БКЭ благоприятный, в отношении функции конечностей — зависит от тяжести и течения заболевания[4].
Примечания
Литература
- Горбунова В. Н., Кадурина Т. И., Белоног О. Л., Арсентьев Вадим Геннадиевич, Шабалов Н. П. Наследственные нарушения соединительной ткани в детской ортопедической практике (Обзор литературы). Часть I // Российский вестник детской хирургии, анестезиологии и реаниматологии. — 2011. — № 1.
- Горбунова В. Н., Кадурина Т. И., Белоног О. Л., Арсентьев Вадим Геннадиевич, Шабалов Н. П. Наследственные нарушения соединительной ткани в детской ортопедической практике. Часть II // Российский вестник детской хирургии, анестезиологии и реаниматологии. — 2011. — № 2.