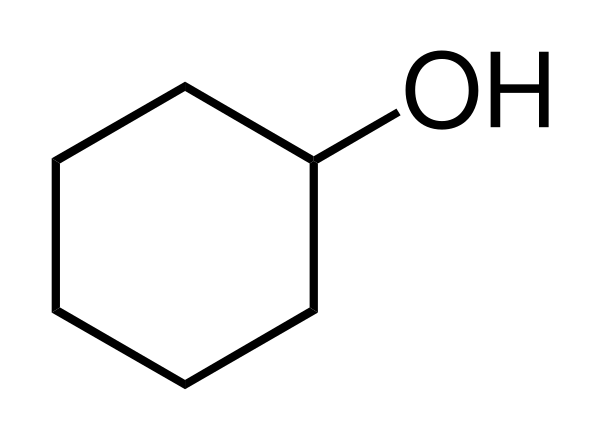
Циклогексанол
Циклогексано́л (гексали́н, химическая формула — C6H11OH) — органический алициклический спирт.
При стандартных условиях, циклогексанол — это бесцветные кристаллы со слабым запахом камфоры.
Общие сведения
| Циклогексанол | |
|---|---|
| Общие | |
| Систематическое наименование |
Циклогексанол |
| Традиционные названия | Гексалин |
| Хим. формула | C6H12O |
| Рац. формула | C6H11OH |
| Физические свойства | |
| Состояние | Твёрдое |
| Молярная масса | 100,16 г/моль |
| Плотность | 0,962 г/см³ |
| Энергия ионизации | 10 ± 1[1] |
| Термические свойства | |
| Температура | |
| • плавления | 25,4 °C |
| • кипения | 160,8 °C |
| • вспышки | 154 ± 1[1] |
| Давление пара | 1 ± 1[1] |
| Классификация | |
| Рег. номер CAS | 108-93-0 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 7966 |
| UNII | 8E7S519M3P |
| CompTox Dashboard EPA | DTXSID4021894 |
| Рег. номер EINECS | 203-630-6 |
| SMILES | |
| InChI | |
| RTECS | GV7875000 |
| ChEBI | 18099 |
| ChemSpider | 7678 |
| ECHA InfoCard | 100.003.301 |
| Безопасность | |
| NFPA 704 | |
Физические свойства
Химические свойства
Циклогексанол образует все характерные для спиртов производные (алкоголяты, сложные эфиры и др.); каталитическое окисление его кислородом воздуха приводит к образованию циклогексанону:
Окисление в более жёстких условиях (окисление азотной кислотой, хромовой смесью или перманганатом калия) приводит к образованию адипиновой кислоты:
.
Циклогексанол легко дегидратируется с образованием циклогексена (C6H10):
Поскольку фенолы обладают более сильными кислотными свойствами, чем спирты, а спирты реагируют с активными металлами, то очевидно, что и фенолы тоже могут реагировать с ними. Однако, желательно реакцию проводить при нагревании, поскольку фенол является твёрдым веществом.
2C6H5OH+2Na=2C6H5ONa+H2
Получение
1) Каталитическое гидрирование фенола:
2) Окисление циклогексана (в этом случае обычно в смеси с циклогексаноном):
и многими другими способами.
Применение
Применяют как полупродукт в производстве капролактама, из полимера которого изготовляют полиамидное волокно, и как растворитель.
Примечания
Литература
- Зефиров Н.С. и др. т.5 Три-Ятр // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1998. — 783 с. — ISBN 5-85270-310-9.

![{\displaystyle {\mathsf {C_{6}H_{11}OH{\xrightarrow[{-H_{2}O}]{O_{2},t,kat:Co(C_{17}H_{35}COO)_{2}}}C_{6}H_{10}O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/ed18a855fccf937e84aabee0a6fdcfd9f9eca54d)
![{\displaystyle {\mathsf {C_{6}H_{11}OH+2O_{2}{\xrightarrow[{-H_{2}O}]{t,HNO_{3}/K_{2}Cr_{2}O_{7}+H_{2}SO_{4}}}COOH(CH_{2})_{4}COOH}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/61316812d8dcbc571d1ccad67374b75dddfb2f34)

![{\displaystyle {\mathsf {C_{6}H_{5}OH+3H_{2}{\xrightarrow[{}]{t,p,kat:Pd/Al_{2}O_{3},Ni/Cr/Al_{2}O_{3}}}C_{6}H_{11}OH}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/27ba311415d21befb860e6464799229eb22ae252)
![{\displaystyle {\mathsf {2C_{6}H_{12}{\xrightarrow[{-H_{2}O}]{3/2O_{2},t,p,kat:CoO*B_{2}O_{3}/Co(C_{17}H_{35}COO)_{2}}}C_{6}H_{11}OH+C_{6}H_{10}O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/61b8a3864a496e05440e5a2eeb5458068e0545e5)