Лихорадка чикунгунья
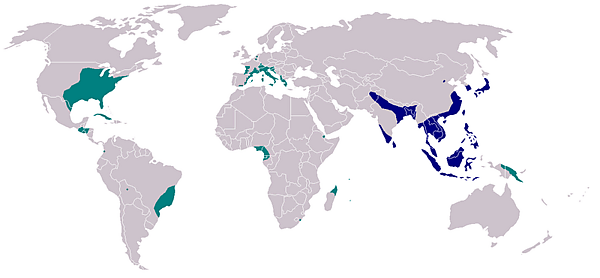
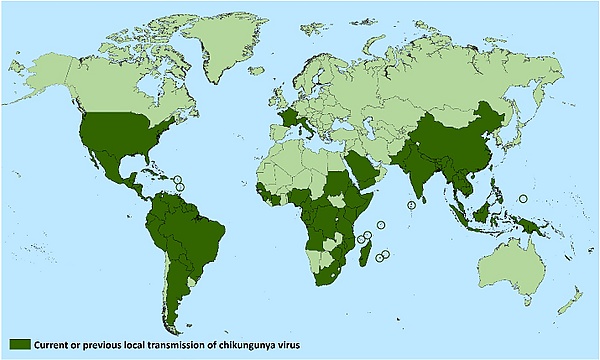
Лихорадка чикунгунья — это инфекция, вызываемая вирусом чикунгунья (англ. Chikungunya virus, CHIKV)[1][2][3]. Заболевание было впервые выявлено в 1952 году в Танзании и названо по аналогии со словом «искривляться» языка кимаконде. Чикунгунья стала глобальной проблемой здравоохранения из-за её быстрого географического распространения, повторяющихся вспышек, отсутствия эффективных противовирусных методов лечения и потенциальной угрозы высокой заболеваемости. Основные симптомы — это лихорадка и боль в суставах. Вирус Чикунгунья широко распространён в тропических и субтропических регионах с тёплым климатом. Многочисленные популяции комаров-переносчиков (A. aegypti и A. albopictus) способствуют его передаче[4].
История
Впервые это заболевание было описано Мэрион Робинсон[5] и У.Х.Р. Ламсденом[6] в двух статьях 1955 года, после вспышки в 1952 году на плато Маконде, вдоль границы между Мозамбиком и Танганьикой (материковая часть современной Танзании). С тех пор вспышки время от времени происходили в Африке, Южной и Юго-Восточной Азии; недавние вспышки привели к распространению болезни в более широком диапазоне[7][8].
Первая зарегистрированная вспышка, вероятно, произошла в 1779 году[9]. Это согласуется с данными молекулярной генетики, которые предполагают, что вирус развился примерно в 1700 году[10].
Согласно оригинальной статье Ламсдена, термин «чикунгунья» происходит от глагола kungunyala, имеющего корень в языке Маконде, что означает высыхать или становиться деформированным. В ходе параллельного исследования Робинсон более конкретно сформулировал термин «kungunyala» как «то, что изгибается вверх». Подразумевается, что это относится к искривлённой позе людей, страдающих от сильных болей в суставах и симптомов артрита, связанных с этим заболеванием[11]. Последующие авторы упустили из виду ссылки на язык маконде и предположили, что этот термин произошёл от суахили, основного языка региона и являющегося частью другой ветви языков банту. Ошибочное отнесение к суахили повторялось во многих печатных источниках[12].
Чикунгунья — один из более чем десятка возбудителей, исследованных в качестве потенциального биологического оружия[13][14].
Это заболевание входит в группу забытых тропических болезней[15].
Первая вакцина против вируса чикунгунья была одобрена для медицинского применения в Соединённых Штатах в ноябре 2023 года. Вакцины против вируса чикунгунья также были разрешены в Европейском союзе в мае 2024[3].
Исторически сложилось так, что чикунгунья была распространена в основном в развивающихся странах. По оценкам, ежегодно это заболевание вызывает около 3 миллионов случаев инфицирования. Эпидемии в Индийском океане, на островах Тихого океана и в Северной и Южной Америке продолжают изменять распространение болезни[16]. В Африке чикунгунья распространяется «лесным циклом», то есть без участия человека, при котором вирус в основном передаётся от других приматов, к мелким млекопитающим и комарам, в промежутках между вспышками заболевания среди людей[17]. Во время вспышек из-за высокой концентрации вируса в крови людей, находящихся в острой фазе инфекции, вирус может передаваться от человека к комарам и обратно к человеку. Распространение за пределы Африки, возможно, началось ещё в 18 веке. Имеющиеся данные не указывают на то, произошло ли проникновение вируса чикунгунья в Азию в 19 веке или позже, но эпидемический азиатский штамм вызывает вспышки в Индии и продолжает циркулировать в Юго-Восточной Азии. В Африке вспышки, как правило, были связаны с обильными осадками, которые приводили к увеличению популяции комаров. Во время недавних вспышек в городских центрах вирус распространялся, циркулируя между людьми и комарами[18][19].
Глобальные показатели распространения инфекции чикунгунья варьируются в зависимости от вспышек. Когда чикунгунья была впервые выявлена в 1952 году, её распространение в Западной Африке было незначительным, а уровень заражения был связан с количеством осадков. Начиная с 1960-х годов, периодические вспышки были зафиксированы в Азии и Африке. Однако с 2005 года, после нескольких десятилетий относительного бездействия, чикунгунья вновь проявила себя и вызвала крупные вспышки в Африке, Азии и Северной и Южной Америке. Например, в Индии чикунгунья вновь появилась после 32-летнего отсутствия вирусной активности[20]. Вспышки заболевания произошли в Европе, Карибском бассейне и Южной Америке — районах, в которых чикунгунья ранее не выявлялась. Местная передача вируса также произошла в Соединённых Штатах и Австралии, странах, в которых вирус ранее был неизвестен[21]. В 2005 году вспышка на острове Реюньон была самой крупной из зарегистрированных на тот момент: по оценкам, на острове с населением около 770 000 человек было зарегистрировано 266 000 случаев заболевания[22]. Во время вспышки в 2006 году Индия сообщила о 1,25 миллиона предполагаемых случаев заболевания[23]. Чикунгунья была завезена в Америку в 2013 году, впервые обнаружена на французском острове Сен-Мартен[24], и в течение следующих двух лет ПОЗ зарегистрировала в Северной и Южной Америке 1 118 763 подозрительных случая и 24 682 подтверждённых случая[25]. В 2023 году в Бразилии произошла крупная вспышка, когда было зарегистрировано более 180 000 случаев заболевания, что потребовало активизации мер общественного здравоохранения и возобновления исследований вирусных мутаций и схем передачи[26]
Анализ генетического кода вируса Чикунгунья позволяет предположить, что усиление тяжести вспышки в 2005 году может быть связано с изменением генетической последовательности, которая изменила сегмент E1 белка вирусной оболочки вируса, на вариант под названием E1-A226V. Эта мутация потенциально позволяет вирусу легче размножаться в клетках комаров. Это изменение позволяет вирусу использовать азиатского тигрового комара (инвазивный вид) в качестве переносчика в дополнение к более строго тропическому основному переносчику, Aedes aegypti. Усиленная передача вируса Чикунгунья A. albopictus может означать повышенный риск вспышек в других районах, где присутствует азиатский тигровый комар. A. albopictus — инвазивный вид, который распространился по Европе, Северной и Южной Америке, Карибскому бассейну, Африке и Ближнему Востоку[27][28][29].
После обнаружения вируса Зика в Бразилии в апреле 2015 года, первого в истории Западного полушария, считается, что некоторые случаи лихорадки чикунгунья и лихорадки денге на самом деле могут быть случаями заражения вирусом Зика или сочетанными инфекциями[30][31].
Этиология
В кровь человека вирус, как правило, попадает при укусе комара-переносчика. Также встречается вертикальная передача вируса от матери к ребёнку во время беременности или при родах — однако такой вариант передачи встречается значительно реже[32]. В теории возможна передача вируса через инфицированные препараты крови и донорство органов, но ни одного такого случая не было задокументировано[33].
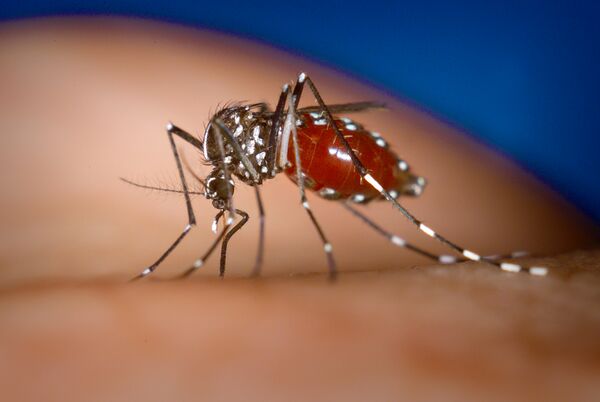
Чикунгунья передаётся через укусы комаров Aedes, вид A. aegypti был идентифицирован как наиболее распространённый переносчик. В начале 20-го века было показано, что вирус могут переносить и представители многих других видов комаров, включая A. albopictus. Исследования, проведённые Институтом Пастера в Париже, показали, что штаммы вируса чикунгунья во время вспышки на острове Реюньон в 2005—2006 годах претерпели мутацию, которая способствовала передаче вируса азиатским тигровым комаром (A. albopictus). К другим видам, потенциально способным передавать вирус чикунгуньи, относятся Ae. furcifer-taylori, Ae. africanus и Ae. luteocephalus[34].
Чикунгунья связана с комарами, средой их обитания и поведением человека. Адаптация комаров к меняющемуся климату Северной Африки около 5000 лет назад заставила их искать места, где люди запасали воду. В то время человеческое жильё и среда обитания комаров были очень тесно связаны. Во время эпидемий люди являются резервуаром вируса[35]. Поскольку в начале острой инфекции в крови присутствует большое количество вируса, вирус может передаваться от человека с виремией к комару и обратно к человеку. В другие времена резервуарами служили обезьяны, птицы и другие позвоночные животные[36].
Патогенез
Вирус чикунгунья передается человеку, когда инфицированный комар прокусывает кожу и вирус попадает в кровоток. Патогенез лихорадки чикунгунья у людей плохо изучен, несмотря на описанные вспышки заболеваемости. Похоже, что in vitro вирус чикунгуньи способен размножаться в эпителиальных и эндотелиальных клетках человека, первичных фибробластах и макрофагах, происходящих из моноцитов. Вирусная репликация обладает высокой цитопатической активностью, но чувствительна к интерферону I и II типов. В исследованиях In vivo выяснилось, что вирус чикунгунья реплицируется в фибробластах, клетках-предшественниках скелетных мышц и миоволокнах[37].
Реакция организма на интерферон I типа играет важную роль в иммунном ответе организма на вирус чикунгунья. При заражении лихорадкой чикунгунья фибробласты хозяина вырабатывают альфа- и бета-интерфероны 1-го типа (IFN-α и IFN-β). В ходе исследований на мышах было установлено, что дефицит INF-1 у мышей, подвергшихся воздействию вируса, вызывает повышенную заболеваемость и смертность. Специфичные для чикунгуньи восходящие компоненты интерферонового пути 1-го типа, участвующие в реакции организма на инфекцию чикунгунья, до сих пор неизвестны. Тем не менее, исследования на мышах показывают, что IPS-1 является важным фактором, и что значимость IRF3 и IRF7 зависит от возраста. Исследования на мышах также показывают, что чикунгунья обходит защитные механизмы организма и противодействует реакции интерферона I типа, продуцируя NS2, неструктурный белок, который разрушает RBP1 и отключает способность клетки-хозяина транскрибировать ДНК. NS2 вмешивается в сигнальный путь JAK-STAT и предотвращает фосфорилирование STAT[38].
В острой фазе лихорадки чикунгунья вирус обычно присутствует в тех областях, где проявляются симптомы, особенно в скелетных мышцах и суставах. Предполагается, что в хронической фазе персистенция вируса (неспособность организма полностью избавиться от вируса), недостаточный клиренс антигена или и то, и другое вместе способствуют возникновению боли в суставах. Воспалительная реакция как на острой, так и на хронической стадиях заболевания частично является результатом взаимодействия вируса с моноцитами и макрофагами. Заболевание, вызванное вирусом Чикунгунья, у людей связано с повышенным уровнем специфических цитокинов и хемокинов в сыворотке крови. Высокие уровни специфических цитокинов были связаны с более тяжелым течением острого заболевания: интерлейкина-6 (IL-6), IL-1β, RANTES, белка-хемоаттрактанта моноцитов 1 (MCP-1), монокина, индуцируемого гамма-интерфероном (MIG), и белка 10, индуцируемого гамма-интерфероном (IP-10). Цитокины также могут способствовать развитию хронического заболевания, вызванного вирусом Чикунгунья, поскольку постоянная боль в суставах связана с повышенным уровнем IL-6 и гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF). У пациентов с хроническими симптомами наблюдалось незначительное повышение уровня С-реактивного белка, что свидетельствует о продолжающемся хроническом воспалении. Однако существует мало доказательств связи между хроническим заболеванием, вызванным вирусом Чикунгунья, и развитием аутоиммунных заболеваний[37][39].
Эпидемиология
С начала 2025 года и по состоянию на начало июня в 14 странах/территориях было зарегистрировано около 220 000 случаев заболевания CHIKVD и 80 смертей, связанных с CHIKVD. Случаи заболевания зарегистрированы в Северной и Южной Америке, Африке и Азии, и, хотя в континентальной Европе случаев заболевания не зарегистрировано, на островах Реюньон и Майотта (самые отдаленные регионы Европейского Союза) вспышки CHIKVD продолжаются[40].
В 2025 году на Северную и Южную Америку приходится наибольшее число случаев CHIKVD в мире. По состоянию на июнь 2025 года (данные собраны 26 мая 2025 года) странами, сообщающими о наибольшем числе случаев CHIKVD, являются Бразилия (141 436), Аргентина (2521), Боливия (605) и Перу (46)[40].
По состоянию на начало июня 2025 года в Азии было зарегистрировано более 33 000 случаев CHIKVD из Индии, Шри-Ланки и Пакистана. В Африке случаи CHIKVD в 2025 году были зарегистрированы в Сенегале[40].
На сегодняшний день в континентальной Европе в 2025 году не было зарегистрировано ни одного аутохтонного случая CHIKVD. Однако по состоянию на конец мая 2025 года в самом отдалённом регионе Франции, Реюньоне, было зарегистрировано более 51 000 случаев CHIKVD. Случаи заболевания зарегистрированы во всех муниципалитетах острова. Уровень 4 системы ORSEC «Арбовирусы» остаётся активным, что соответствует циркуляции средней интенсивности эпидемии. На Майотте также зарегистрировано 560 аутохтонных случаев CHIKVD. Согласно бюллетеню, опубликованному 2 июня 2025 года, Майотта перешла в фазу эпидемии (фазу 3), что свидетельствует об интенсивном и широком распространении вируса по всей территории[41].
Диагностика
Лихорадка чикунгунья диагностируется на основе клинических, эпидемиологических и лабораторных критериев[21].
Клинически значимыми симптомами являются лихорадка и сильная боль в суставах. Эпидемиологические критерии состоят в том, бывал ли человек в районе, где распространён вирус чикунгунья, в течение последних двенадцати дней (то есть потенциального инкубационного периода). Главный лабораторный критерий — это снижение количества лимфоцитов, соответствующее виремии. Однако окончательный лабораторный диагноз может быть поставлен путём выделения вируса, определение РНК вируса чикунгунья в крови методом полимеразной цепной реакции с обратной транскрипцией или выявлением антител к вирусу чикунгунья в сыворотке крови[21].
Около 85 % людей, инфицированных вирусом Чикунгунья, испытывают симптомы, которые обычно начинаются с внезапной высокой температуры выше 39 °C (102 °F). За лихорадкой вскоре следует сильная боль в мышцах и суставах. Боль обычно поражает несколько суставов рук и ног и носит симметричный характер — то есть, если поражён один локоть, то и другой тоже. Люди, больные лихорадкой чикунгунья, также часто испытывают головную боль, боли в спине, тошноту и повышенную утомляемость. Примерно у половины заболевших появляется сыпь с покраснением и иногда небольшими бугорками на ладонях, подошвах ног, туловище и лице. У некоторых людей сыпь остаётся ограниченной на небольшом участке тела; у других сыпь может быть обширной, покрывая более 90 % кожи. Некоторые люди испытывают проблемы с желудочно-кишечным трактом, сопровождающиеся болью в животе и рвотой. У других наблюдаются проблемы со зрением, а именно чувствительность к свету, конъюнктивит и боль в заглазничном пространстве. Этот первый набор симптомов, называемый «острой фазой» лихорадки чикунгунья, длится около недели, после чего большинство симптомов проходят самостоятельно[18].
У многих людей симптомы продолжают проявляться и после того, как проходит «острая фаза». Этот период называется «постострой фазой» для симптомов, длящихся от трёх недель до трёх месяцев, и «хронической стадией» для симптомов, длящихся более трёх месяцев. В обоих случаях длительными симптомами, как правило, являются боли в суставах: артрит, тендовагинит и/или бурсит. Если у пострадавшего уже были проблемы с суставами, они, как правило, усугубляются. Чрезмерная нагрузка на сустав может привести к болезненному отёку, скованности движений, повреждению нервов и невропатической боли. Как правило, со временем боль в суставе проходит; однако хроническая стадия может длиться от нескольких месяцев до нескольких лет[18].
Боль в суставах отмечается в 87-98 % случаев и почти всегда возникает более чем в одном суставе, хотя припухлость суставов встречается редко. Как правило, поражённые суставы локализуются на обеих руках и ногах. Суставы чаще поражаются, если они ранее были повреждены в результате артрита. Боль чаще всего возникает в периферических суставах: запястья, лодыжки и суставы кистей и стоп, а также в некоторых более крупных суставах, обычно в плечах, локтях и коленях[18][42]. Боль также может возникать в мышцах или связках. Более чем в половине случаев нормальная активность ограничена значительной усталостью и болью. В редких случаях может возникать воспаление глаз в виде иридоциклита или увеита, а также могут возникать поражения сетчатки[43]. Может произойти временное повреждение печени[44].
У людей, больных лихорадкой чикунгунья, иногда развиваются неврологические расстройства, чаще всего отёк или дегенерация головного мозга, воспаление или дегенерация миелиновых оболочек вокруг нейронов, синдром Гийена-Барре, острый диссеминированный энцефаломиелит, гипотония (у новорождённых) и проблемы со зрением. В особо редких случаях у людей могут развиться изменения в поведении, судороги, раздражение мозжечка или мозговых оболочек, паралич глазодвигательного нерва или паралич глазных мышц[18].
Новорождённые особенно чувствительны к тяжёлому течению инфекции чикунгунья. Признаки инфекции обычно начинаются с повышения температуры, сыпи и отёка конечностей. Примерно у половины новорождённых заболевание протекает в лёгкой форме, которая проходит сама по себе; у другой половины заболевание протекает в тяжёлой форме с воспалением головного мозга и судорогами. В тяжёлых случаях у пострадавших новорождённых также могут быть проблемы с кровотечением и кровотоком, а также с работой сердца[18].
Помимо новорождённых, более тяжёлое течение лихорадки чикунгунья характерно для пожилых людей, а также людей с сахарным диабетом, болезнями сердца, печени и почек и инфицированных вирусом иммунодефицита человека. Примерно от 1 до 5 из 1000 человек с симптомами лихорадки чикунгунья умирают от этого заболевания[18].
Окончательный диагноз можно поставить на основе выделения вируса, однако эта процедура требует времени (от одной до двух недель), а также специальных условий: выделение вируса должно производиться в лабораториях биологической безопасности уровня III. Методика включает воздействие на определённые клеточные линии образцов цельной крови и выявление специфичных для вируса Чикунгунья реакций. ОТ-ПЦР с использованием вложенных пар праймеров применяется для амплификации нескольких специфичных для вируса Чикунгунья генов из цельной крови, создавая тысячи или миллионы копий генов для их идентификации. ОТ-ПЦР также может количественно определять вирусную нагрузку в крови. При помощи ОТ-ПЦР диагностические результаты можно получить через один-два дня[45].
Выявление специфических антител к вирусу чикунгунья в сыворотке крови требует большего количества крови, чем другие методы. Для измерения уровней специфичных для вируса Чикунгунья IgM в сыворотке крови применяется иммуно-ферментный анализ. Одним из преимуществ серологической диагностики является то, что сывороточный IgM можно обнаружить от 5 дней до месяцев после появления симптомов. Недостатки этого метода заключаются в том, что для результатов может потребоваться от двух до трёх дней, и могут возникать ложные положительные результаты при заражении другими родственными вирусами: вирус О’Ньонг’Ньонг и вирус леса Семлики[45][46].
Дифференциальная диагностика
Дифференциальную диагностику проводят с другими заболеваниями, переносимые комарами: лихорадка Денге или малярия, или другие инфекции, например, грипп. Хроническая рецидивирующая полиартралгия возникает по крайней мере у 20 % пациентов с лихорадкой чикунгунья через год после заражения, тогда как при лихорадке Денге такие симптомы редко встречаются[47]. Вирус Чикунгунья тесно связан с вирусом О’Ньонг-Ньонг (ONNV), который имеет сходные генетические и клинические характеристики[48].
Лечение
Лекарство от лихорадки чикунгунья в 2025 году разработала российская компания «Промомед»[49]. Как сообщил председатель совета директоров компании Пётр Белый, единственный существующий и медицински оправданный способ лечения — это индукция собственных интерферонов в организме человека. Препарат прошёл все необходимые клинические испытания и доказал свою эффективность[50]. До этой разработки применялась поддерживающая терапия, заключающаяся в симптоматическом лечение лихорадки и болей в суставах. Для этого применяются: нестероидные противовоспалительные препараты: напроксен, и анальгетики, не содержащие аспирин, например, парацетамол (ацетаминофен). Аспирин не рекомендуется принимать из-за повышенного риска кровотечения. Несмотря на противовоспалительный эффект, кортикостероиды не рекомендуются во время острой фазы заболевания, так как они могут вызвать подавление иммунитета и усугубить инфекцию[18][51].
Пассивная иммунотерапия имеет потенциальные преимущества при лечении лихорадки чикунгунья. Исследования на животных с использованием пассивной иммунотерапии оказались эффективными. Пассивная иммунотерапия включает внутривенное введение гипериммунных человеческих антител (иммуноглобулинов) к вирусу чикунгунья лицам, подверженным высокому риску заражения[52].
Оксатомид — это антигистаминный препарат H1, аналогичный бенадрилу. Было показано, что он обладает противовирусным действием против вируса венесуэльского энцефаломиелита лошадей (ВЭЛ)[53], который является альфавирусом Нового Света и более смертоносен, чем Чикунгунья. Оксатомид — это безрецептурный препарат, который можно приобрести онлайн. Пока неясно, будет ли это соединение эффективно против вируса CHIKV, необходимы дополнительные исследования, чтобы установить его эффективность против других альфавирусов[53].
Прогноз
Воспалительный полиартрит является наиболее распространенным долгосрочным осложнением инфекции чикунгунья. Однако есть сообщения об алопеции, гиперпигментации кожи, хронической усталости и депрессии как о персистирующих последствиях. Другие долгосрочные последствия после вирусного поражения центральной нервной системы вирусом чикунгунья - это персистирующие неврологические последствия, проявляющиеся эпилепсией или постинфекционной деменцией[54]. Энцефалит или энцефалопатия у новорожденных и детей имеют ухудшенную нейрокогнитивную функцию с тяжелыми дефицитами развития. Хотя и в небольшом количестве, ранее сообщалось о глазных осложнениях, приводящих к потере остроты зрения и постоянной неврологической инвалидности после острого рассеянного энцефаломиелита[55].
Профилактика
Несмотря на существование одобренных вакцин, наиболее эффективными средствами профилактики являются защита от контакта с комарами-переносчиками и регуляция численности комаров путём ограничения их среды обитания.[56] Доступ к вакцине против вируса чикунгунья остаётся ограниченным во многих эндемичных регионах. Борьба с комарами направлена на устранение стоячей воды, в которой комары откладывают яйца и развиваются в виде личинок[19]. Наиболее часто регистрируемые побочные эффекты от вакцинации: головная боль, усталость, мышечные боли, боли в суставах, лихорадка, тошнота и болезненность в месте инъекции. По состоянию на июнь 2025 года регулирующие органы в области лекарственных средств в США, ЕС и Великобритании приостановили применение вакцины у пожилых пациентов на время расследования сообщений о серьёзных неврологических побочных эффектах и летальных исходах[57][58].
Распространение заболевания в России
25 августа 2025 года глава Роспотребнадзора Анна Попова заявила, что обитающие на территории России комары не заражены лихорадкой чикунгунья и не представляют высоких эпидемиологических рисков, однако завозные случаи заражения этим вирусом вполне вероятны[59].
Борьба с распространением
В августе 2025 года в Китае для борьбы с распространяющими инфекцию комарами Aedes стали использовать гигантских комаров-каннибалов, личинки которых пожирают более мелких вредителей[60]. Специалисты сообщили о специальном выпуске в дикую природу личинок «слоновьих комаров» Toxorhynchites splendens, способных в течение жизни поглотить от 80 до 100 личинок комаров-переносчиков[61].
Также сообщалось, что в водоемы провинции Гуандун для сдерживания крупнейшей в истории страны вспышки вируса было запущено пять тыс. рыб, питающихся личинками комаров[62].