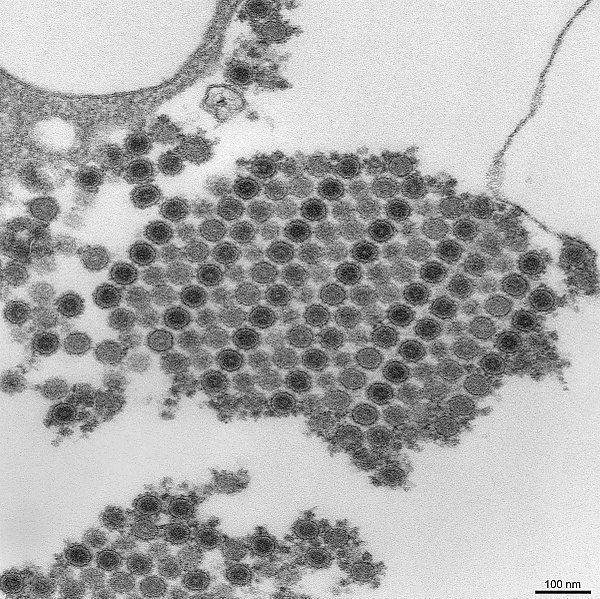
Вирус Чикунгунья
Вирус чикунгунья[2] (англ. Chikungunya virus, CHIKV, от глагола языка кимаконде «стать искривлённым»[3]) — это арбовирус рода Alphavirus семейства тогавирусов (Togaviridae), передающийся посредством укусов комаров рода кусаков[4]. Заразиться вирусом чикунгунья можно на Индийском субконтиненте, в Африке или Азии, в настоящее время комары-переносчики распространились также в Европе и Северной Америке[5][6].
Общие сведения
| Вирус Чикунгунья | |
|---|---|
| Научная классификация | |
|
Реалм: Царство: Тип: Класс: Порядок: Семейство: Тогавирусы (Togaviridae) Род: Вид: Вирус Чикунгунья |
|
| Международное научное название | |
| Chikungunya virus | |
| Группа по Балтимору | |
| IV: (+)оцРНК-вирусы |
История распространения
Впервые вирус чикунгунья был выделен в 1953 году в Танзании. Были описаны три генотипа этого вируса: западноафриканский, восточно/центрально/южноафриканский и азиатский генотипы[7]. Азиатская линия возникла в 1952 году и впоследствии разделилась на две линии – индийскую (линия Индийского океана) и юго-восточноазиатскую. Впервые об этом вирусе на американском континенте сообщили в 2014 году. Филогенетические исследования показали, что в Бразилии встречаются два штамма – азиатский и Восточно–/центрально-/южноафриканский - и что азиатский штамм прибыл в Карибский бассейн (скорее всего, из Океании) примерно в марте 2013 года. Было подсчитано, что средняя скорость молекулярной эволюции составляет 5 × 10−4 замены на сайт в год (плотность вероятности на 95% выше 2.9–7.9 × 10-4)[8].
Первая европейская вспышка заболевания чикунгуньей была в Италии[5]. С августа 2015 года заболевание активно распространялось в Мексике, Гватемале[6].
В 2025 году российская компания «Промомед» разработала препарат для лечения инфекции, вызываемой вирусом Чикунгунья[9].
В июле 2025 года в связи с заявлением Всемирной организации здравоохранения о случаях передачи чикунгуньи во Франции и Италии пресс-служба Роспотребнадзора проинформировала, что в РФ завозные случаи лихорадки не зарегистрированы[10][11]. В августе 2025 года власти Китая усилили противоэпидемические меры в южной провинции Гуандун на фоне вспышки вируса чикунгунья: менее чем за месяц в городском округе Фошань зарегистрировали более 6500 заражений лихорадкой[12].
29 августа 2025 года Роспотребнадзор сообщил, что в России выявлен первый завозной случай лихорадки чикунгунья[13]. Заболевший прибыл в Москву из Шри-Ланки, где отдыхал десять дней. Поначалу врачи предположили, что у пациента лихорадка денге, однако ПЦР-тест в ЦНИИ Эпидемиологии Роспотребнадзора показал положительный результат на вирус чикунгунья[14]. Пресс-служба ведомства пояснила, что угрозы распространения данной лихорадки в России нет, поскольку она не передаётся от человека к человеку[13].
В октябре 2025 года случай местного заражения впервые зарегистрирован в Гонконге. Как сообщил журналистам руководитель Центра охраны здоровья мегаполиса Эдвин Сюй, риску заражения теперь подвержены до 10 тысяч человек, живущих в районе[15].
В феврале 2026 года завозной случай лихорадки чикунгунья выявлен в России. Заболевшая прибыла в Москву после отдыха на Сейшелах[16].
Вирусология
Вирус чикунгунья (CHIKV) является представителем рода Alphavirus и семейства Togaviridae. Вирус чикунгунья имеет икосаэдрический капсид, окруженный липидной оболочкой, диаметром 70 нм. Он представляет собой одноцепочечный РНК-вирус с положительной полярностью, длина генома составляет около 11,8 кб[17]. Этот вирус входит в комплекс вирусов леса Семлики и тесно связан с вирусом Росс Ривер, вирусом О'Ньонг-Ньонг и вирусом леса Семлики. Поскольку он передается членистоногими, а именно комарами, его также можно отнести к арбовирусам (arbopod-borne virus). В Соединенных Штатах он классифицируется как приоритетный патоген категории В, и для работы с ним требуются меры предосторожности III уровня биобезопасности[18].
Геном вируса чикунгунья состоит из структурных и неструктурных белков, что типично для геномной организации альфавируса. Структурные белки, включая капсид, E3, E2, 6K и E1, отвечают за инкапсуляцию вирусного генома и сборку новых вирусных частиц. Эти белки имеют решающее значение для проникновения вируса в клетки хозяина. Между тем, неструктурные белки nsP1, nsP2, nsP3 и nsP4 играют важную роль в репликации вируса, трансляции и уклонении от иммунитета[19].
Передача вируса
В кровь человека вирус, как правило, попадает при укусе комара-переносчика. Также встречается вертикальная передача вируса от матери к ребёнку во время беременности или при родах - однако такой вариант передачи встречается значительно реже. В теории возможна передача вируса через инфицированные препараты крови и донорство органов, но ни одного такого случая не было задокументировано[20]. Инкубационный период лихорадки чикунгунья чаще всего составляет от трех до семи дней, но может колебаться от одного до двенадцати дней[21].
Чикунгунья передается через укусы комаров Aedes, и вид A. aegypti был идентифицирован как наиболее распространенный переносчик. В начале 20-го века было показано, что вирус могут переносить и представители многих других видов комаров, включая A. albopictus. Исследования, проведенные Институтом Пастера в Париже, показали, что штаммы вируса чикунгунья во время вспышки на острове Реюньон в 2005-2006 годах претерпели мутацию, которая способствовала передаче вируса азиатским тигровым комаром (A. albopictus). К другим видам, потенциально способным передавать вирус чикунгуньи, относятся Ae. furcifer-taylori, Ae. africanus и Ae. luteocephalus[22].
Чикунгунья связана с комарами, средой их обитания и поведением человека. Адаптация комаров к меняющемуся климату Северной Африки около 5000 лет назад заставила их искать места, где люди запасали воду. В то время человеческое жилье и среда обитания комаров были очень тесно связаны. Во время эпидемий люди являются резервуаром вируса. Поскольку в начале острой инфекции в крови присутствует большое количество вируса, вирус может передаваться от человека с виремией к комару и обратно к человеку[23]. В другие времена резервуарами служили обезьяны, птицы и другие позвоночные животные[24].
Репликация вируса
Вирус состоит из четырех неструктурных белков и трех структурных белков. Структурные белки — это белок капсида и два гликопротеина оболочки: E1 и E2, которые образуют гетеродимерные шипы на поверхности вириона. E2 связывается с клеточными рецепторами, чтобы проникнуть в клетку хозяина посредством опосредованного рецепторами эндоцитоза. E1 содержит пептид слияния, который при воздействии кислотности эндосомы в эукариотических клетках диссоциирует от E2 и инициирует слияние мембран, что позволяет высвобождать нуклеокапсиды в цитоплазму хозяина, способствуя инфицированию. Зрелый вирион содержит 240 гетеродимерных шипиков E2/E1, которые после высвобождения отпочковываются на поверхности инфицированной клетки, где они высвобождаются посредством экзоцитоза для заражения других клеток[25].
Репликация генома происходит в мембранных органеллах репликации (называемых «сферулами»)[26]. Они представляют собой мембранные инвагинации, которые возникают в результате ремоделирования мембраны клетки хозяина во время инфицирования. Каждая сферула содержит репликационный комплекс (РК), образованный из четырех вирусно-кодируемых неструктурных белков (nsP), которые кооперативно участвуют в синтезе РНК. Внутри РК: nsP4 (является РНК-зависимой РНК-полимеразой), nsP2 (обладает геликазной активностью и протеолитически расщепляет nsP от вирусного полипротеинового предшественника для формирования зрелых РК), nsP3 (играет роль в привлечении факторов хозяина к сферуле). NsP1 является мембранным якорем для РК, образуя додекамерные поры, которые монотопически связываются с мембраной в шейках сферул, чтобы обеспечить их вход. В качестве фермента nsP1 также играет роль в кэпировании 5′ конца положительно-полярной вирусной РНК. Структуры кэпа, минимально образованные ковалентной связью мотива (m7GMP) с первым нуклеозидом РНК через 5′-5′ трифосфатную (3p) связь (Cap0), повсеместно встречаются в мРНК хозяина и необходимы для обработки, стабильности и трансляции транскриптов. У высших эукариот 2′O рибоза может быть дополнительно метилирована (Cap1) вместе с внутренними основаниями мРНК. Таким образом, для вирусов кэпирование вирусных РНК часто используется как средство для захвата трансляционного аппарата хозяина и играет дополнительную роль в уклонении от врожденного иммунитета хозяина путем предотвращения распознавания терминальных фосфатов РНК цитозольными рецепторами RIG-I и IFIT1. Инфекция чикунгуньи производит два вида вирусной РНК, которые кэпированы nsP1; полноразмерная 11,8 кбн положительно-полярная геномная РНК (гРНК) и субгеномная РНК (сгРНК) 4,3 кбн, которая транскрибируется со второй открытой рамки считывания на более поздних стадиях инфекции и кодирует только структурный полипротеин[26]. Интересно, что, несмотря на центральную роль кэпирования РНК в вирусной инфекции, исследование 2015 показало, что не все альфавирусные гРНК, упакованные в вирионы, кэпированы, и что некэпированные РНК могут играть важную роль в модуляции иммунного ответа хозяина на инфекцию[27].
Макрофаги, как фагоцитарные клетки врожденного иммунитета, служат первой линией защиты от вирусных инфекций, играя ключевую роль в воспалении и активации адаптивного иммунитета; однако при заражении вирусом чикунгунья (CHIKV) они могут выступать в качестве клеточных резервуаров, способствуя постоянному присутствию вируса и хроническому воспалению. Было установлено, что гликопротеины вируса чикунгунья (E1 и E2) не только облегчают проникновение, сборку и выход вируса, но и разрушают внутриклеточные барьеры, усиливая выработку и распространение вирионов в макрофагах человека (in vitro). По сравнению с вирусом О'Ненг-ненг (ONNV), вирус чикунгунья демонстрирует более высокую выработку вирионов в макрофагах, несмотря на их генетическое сходство. Ключевые факторы, определяющие образование вирионов вируса чикунгунья, были идентифицированы в домене E2 B, его β-ленточных дугах и домене E1 II. Кроме того, факторы хозяина, такие как комплексная субъединица сигнальной пептидазы 3 (SPCS3) и эукариотическая субъединица K фактора инициации трансляции 3 (eIF3k), взаимодействуют с вирусом чикунгунья E1 и функционируют как противовирусные рестрикционные факторы, ограничивающие репликацию вируса. Эти взаимодействия могут стать потенциальными мишенями для терапевтического вмешательства. Однако, поскольку модели макрофагов in vitro не в полной мере отражают сложность макрофагов in vivo, необходима дальнейшая проверка на млекопитающих-хозяевах, чтобы получить более полное представление о патогенезе, опосредованном макрофагами[28].
Лихорадка Чикунгунья
Вирус чикунгунья передается человеку, когда инфицированный комар прокусывает кожу и вирус попадает в кровоток. Патогенез лихорадки чикунгунья у людей плохо изучен, несмотря на описанные вспышки заболеваемости. Похоже, что in vitro вирус чикунгуньи способен размножаться в эпителиальных и эндотелиальных клетках человека, первичных фибробластах и макрофагах, происходящих из моноцитов. Вирусная репликация обладает высокой цитопатической активностью, но чувствительна к интерферону I и II типов. В исследованиях In vivo выяснилось, что вирус чикунгунья реплицируется в фибробластах, клетках-предшественниках скелетных мышц и миоволокнах[29].
Реакция организма на интерферон I типа играет важную роль в иммунном ответе организма на вирус чикунгунья. При заражении лихорадкой чикунгунья фибробласты хозяина вырабатывают альфа- и бета-интерфероны 1-го типа (IFN-α и IFN-β). В ходе исследований на мышах было установлено, что дефицит INF-1 у мышей, подвергшихся воздействию вируса, вызывает повышенную заболеваемость и смертность. Специфичные для чикунгуньи восходящие компоненты интерферонового пути 1-го типа, участвующие в реакции организма на инфекцию чикунгунья, до сих пор неизвестны. Тем не менее, исследования на мышах показывают, что IPS-1 является важным фактором, и что значимость IRF3 и IRF7 зависит от возраста. Исследования на мышах также показывают, что чикунгунья обходит защитные механизмы организма и противодействует реакции интерферона I типа, продуцируя NS2, неструктурный белок, который разрушает RBP1 и отключает способность клетки-хозяина транскрибировать ДНК. NS2 вмешивается в сигнальный путь JAK-STAT и предотвращает фосфорилирование STAT[30].
В острой фазе лихорадки чикунгунья вирус обычно присутствует в тех областях, где проявляются симптомы, особенно в скелетных мышцах и суставах. Предполагается, что в хронической фазе персистенция вируса (неспособность организма полностью избавиться от вируса), недостаточный клиренс антигена или и то, и другое вместе способствуют возникновению боли в суставах. Воспалительная реакция как на острой, так и на хронической стадиях заболевания частично является результатом взаимодействия вируса с моноцитами и макрофагами. Заболевание, вызванное вирусом Чикунгунья, у людей связано с повышенным уровнем специфических цитокинов и хемокинов в сыворотке крови. Высокие уровни специфических цитокинов были связаны с более тяжелым течением острого заболевания: интерлейкина-6 (IL-6), IL-1β, RANTES, белка-хемоаттрактанта моноцитов 1 (MCP-1), монокина, индуцируемого гамма-интерфероном (MIG), и белка 10, индуцируемого гамма-интерфероном (IP-10). Цитокины также могут способствовать развитию хронического заболевания, вызванного вирусом Чикунгунья, поскольку постоянная боль в суставах связана с повышенным уровнем IL-6 и гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF). У пациентов с хроническими симптомами наблюдалось незначительное повышение уровня С-реактивного белка, что свидетельствует о продолжающемся хроническом воспалении. Однако существует мало доказательств связи между хроническим заболеванием, вызванным вирусом Чикунгунья, и развитием аутоиммунных заболеваний[3][29].
Примечания
Ссылки
- Всемирная Организация Здравоохранения ВОЗ | Чикунгунья