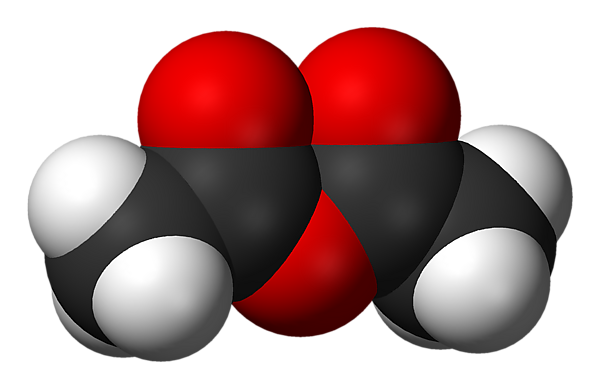
Уксусный ангидрид
У́ксусный ангидри́д (ангидри́д у́ксусной кислоты́) — бесцветная жидкость с резким запахом, растворимая в бензоле, диэтиловом эфире и других органических растворителях. Используется в промышленности и органическом синтезе.
Общие сведения
| Уксусный ангидрид[1][2][3][4] | |
|---|---|
| Общие | |
| Систематическое наименование |
уксусный ангидрид |
| Сокращения | Ac2O |
| Традиционные названия |
ангидрид уксусной кислоты, этановый ангидрид, ацетилацетат, ацетилоксид |
| Хим. формула | (CH3CO)2O |
| Рац. формула | C4H6O3 |
| Физические свойства | |
| Состояние | бесцветная прозрачная жидкость с острым запахом |
| Молярная масса | 102,09 г/моль |
| Плотность | 1,0820 г/см³ |
| Поверхностное натяжение | 0,03265 Н/м |
| Динамическая вязкость | 901 Па·с |
| Энергия ионизации | 965 кДж/моль |
| Удельная проводимость | 4,8·10–7 См/м |
| Термические свойства | |
| Температура | |
| • плавления | –73,1 °C |
| • кипения | 139,6 °C |
| • вспышки | 52,5—53 °C |
| • самовоспламенения | 316 °C |
| Пределы взрываемости | 2,7—10,3 % |
| Критическая точка | |
| • температура | 295,8 °C |
| • давление | 45,4 атм |
| Мол. теплоёмк. | 168,230 °C Дж/(моль·К) |
| Теплопроводность | 0,2209·10–3 Вт/(м·K) |
| Энтальпия | |
| • образования | –624,42ж, –576,1пар кДж/моль |
| • плавления | 10,5 кДж/моль |
| • кипения | 276,7 кДж/моль |
| • сублимации | 48,3 кДж/моль |
| Давление пара | 0,420 °C, 1,740 °C, 5,260 °C, 13,380 °C, 28,7100 °C, 53,3120 °C атм |
| Химические свойства | |
| Растворимость | |
| • в воде | 12 г в 100 г холодной воды |
| Диэлектрическая проницаемость | 20,5 |
| Оптические свойства | |
| Показатель преломления | 1,3906 |
| Структура | |
| Дипольный момент | 2,8 Д |
| Классификация | |
| Рег. номер CAS | 108-24-7 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 7918 |
| UNII | 2E48G1QI9Q |
| CompTox Dashboard EPA | DTXSID0024395 |
| Рег. номер EINECS | 203-564-8 |
| SMILES | |
| InChI | |
| RTECS | AK1925000 |
| ChEBI | 36610 |
| Номер ООН | 1715 |
| ChemSpider | 7630 |
| ECHA InfoCard | 100.003.241 |
| Безопасность | |
| Предельная концентрация | 21 мг/м3 |
| ЛД50 | 1,78—5 мг/кг |
| Фразы риска (R) | R10, R20/22, R34 |
| Фразы безопасности (S) | S26, S36/37/39, S45 |
| Краткие характер. опасности (H) |
H226, H302, H314, H332 |
| Меры предостор. (P) |
P280, P305+P351+P338, P310 |
| Пиктограммы СГС |
|
| NFPA 704 | |
Физические свойства
Уксусный ангидрид представляет собой бесцветную прозрачную подвижную жидкость с резким запахом. Он растворим в бензоле, диэтиловом эфире, этаноле, хлороформе, уксусной кислоте, тетрагидрофуране, ограниченно — в холодной воде. При растворении в воде и спиртах происходит медленное разложение, которое ускоряется при нагревании[1][5].
Химические свойства
Уксусный ангидрид часто применяется в реакциях ацилирования (в данном случае, ацетилирования), в которые вступает широкий ряд различных соединений[6].
- В частности, в реакцию с уксусным ангидридом вступают спирты, при этом выделяется уксусная кислота, а катализаторами выступают основания (например, ацетат натрия) и сильные кислоты.
- В реакции ацилирования вступают также амины, причём для них эта реакция протекает быстрее, чем для спиртов. Анилины также можно ацетилировать: обычно такая реакция применяется для защиты аминогруппы, соединённой с ароматическим циклом от окисления.
- Уксусный ангидрид используется для ацилирования ароматических углеводородов по реакции Фриделя — Крафтса, например, при реакции бензола с уксусным ангидридом в присутствии катализатора образуется ацетофенон.
- Реакции ацетилирования подвергаются также неорганические кислоты. Так, при взаимодействии уксусного ангидрида с азотной кислотой образуется ацетилнитрат — нитрующий реагент, находящий применение в тонком органическом синтезе. Также смешанные эфиры с уксусным ангидридом дают серная кислота, сульфоновые кислоты и соляная кислота.
- Ацетилированию могут подвергаться также оксиды с образованием соответствующих ацетатов. С уксусным ангидридом реагируют также различные соли, ацетилениды, алкоголяты.
- Пероксиды под действием уксусного ангидрида образуют надуксусную кислоту (пероксид водорода) либо перекись ацетила (CH3CO)2O2.
Другим важным свойством уксусного ангидрида является его способность отнимать воду в химических реакциях. Данное свойство широко используется в органическом синтезе, а также химической промышленности. Уксусный ангидрид вступает в реакцию Перкина и другие реакции карбонильных соединений[7].
Спектральные данные
- Масс-спектрометрия. Масса молекулярного иона уксусного ангидрида равна 102, однако в результате его фрагментации образуются также пики с m/z, равным 43 и 15[8].
- ЯМР-спектроскопия. Протоны уксусного ангидрида имеют в 1H ЯМР-спектр химический сдвиг, равный 2,219 м. д. (растворитель CDCl3). В спектре 13C ЯМР наблюдается два сигнала: при 22,07 м. д. для атомов углерода метильной группы и при 166,63 м. д. для атомов углерода карбонильной группы[8].
- УФ-спектроскопия. Максимум поглощения уксусного ангидрида составляет 217 нм[5].
Промышленные методы получения
Исторически первый метод синтеза уксусного ангидрида был основан на превращении ацетата натрия в ацетилхлорид под действием неорганического хлорида (обычно хлористого тионила, хлористого сульфурила или хлористого фосфорила). На второй стадии образовавшийся ацетилхлорид реагировал с избытком ацетата натрия с образованием уксусного ангидрида[7].
В настоящее время эти процессы не используются в промышленности. Основными методами получения являются реакция кетена с уксусной кислотой, окисление уксусного альдегида и карбонилирование метилацетата[7].
Уксусный ангидрид может быть получен жидкофазным окислением ацетальдегида на воздухе.
Использование
Примерно 80 % синтезируемого в промышленности уксусного ангидрида идёт на производство ацетата целлюлозы[9].
Остальная доля используется в органическом синтезе в качестве ацилирующего и водоотнимающего агента.
Правовой стутус
Является прекурсором в производстве наркотиков опиоидной группы, в связи с чем оборот уксусного ангидрида в РФ, Белоруссии и в некоторых других государствах законодательно ограничен[10].
Примечания
Литература
- Held H., Rengst A., Mayer D. Acetic Anhydride and Mixed Fatty Acid Anhydrides // Ullmann's Encyclopedia of Industrial Chemistry. — Wiley, 2000. — doi:10.1002/14356007.a01_065.
- Kim D. H. Acetic anhydride as a synthetic reagent (англ.) // J. Het. Chem. — 1976. — Vol. 13, no. 2. — P. 179—194. — doi:10.1002/jhet.5570130201.