Сульфурилхлорид
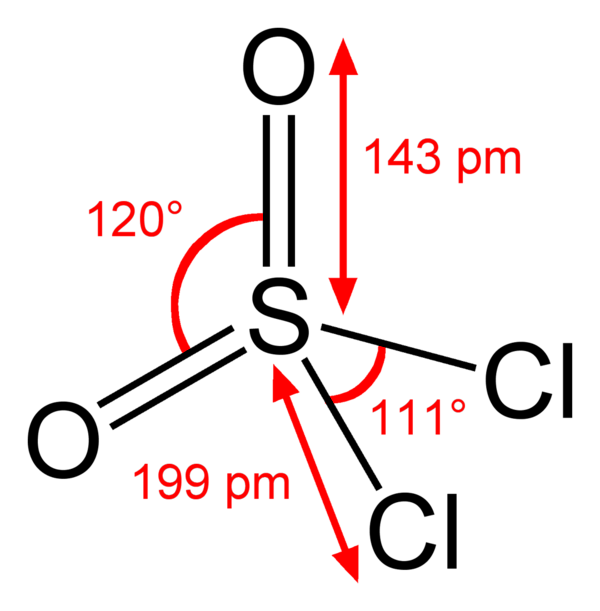
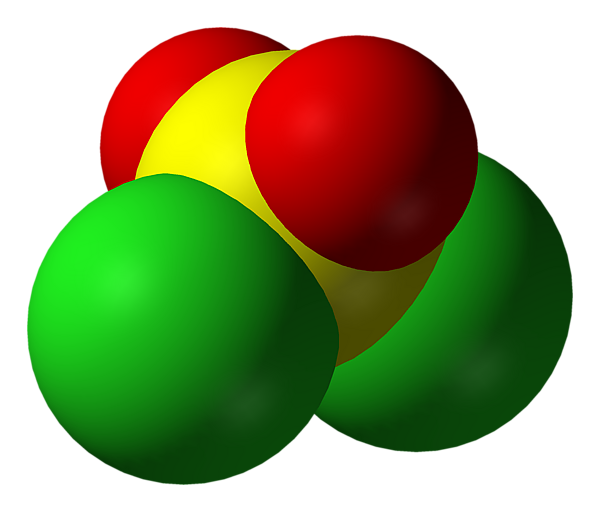
Сульфурилхлорид (хлористый сульфурил) SO2Cl2 — хлорангидрид серной кислоты.
Что важно знать
| Сульфурилхлорид | |
|---|---|
| Общие | |
| Систематическое наименование |
Хлористый сульфурил |
| Хим. формула | SO2Cl2 |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 134.965 г/моль |
| Плотность | 1.665 г/см³ |
| Поверхностное натяжение | 28,78 ± 0,01[1] |
| Термические свойства | |
| Температура | |
| • плавления | −54,7 °C |
| • кипения | 69,2 °C |
| Энтальпия | |
| • образования | −391,2 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | гидролизуется |
| Классификация | |
| Рег. номер CAS | [7791-25-5] |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 24648 |
| UNII | JD26K0R3J1 |
| CompTox Dashboard EPA | DTXSID6029707 |
| Рег. номер EINECS | 232-245-6 |
| SMILES | |
| InChI | |
| ChEBI | 29291 |
| ChemSpider | 23050 |
| ECHA InfoCard | 100.029.314 |
| Безопасность | |
| NFPA 704 | |
Свойства
Бесцветная, резко пахнущая жидкость, хорошо растворимая в хлороформе и уксусной кислоте, в избытке воды растворяется с частично протекающим гидролизом. Дымит на воздухе, гидролизуется по реакции:
Гидролиз идёт слабо в холодной воде, в горячей воде протекает быстро.
При хранении желтеет, поскольку распадается на SO2 и зеленовато-жёлтый хлор.
Получение
Получают взаимодействием SO2 с Cl2 в присутствии катализаторов (активированный уголь, камфора).
Применение
Сульфурилхлорид используется как растворитель для ряда органических и неорганических соединений.
Применяют в синтезе органических веществ (с ним активно проходит хлорирование[2]), вступает в реакции сульфохлорирования тиофенов через образование комплекса с ДМФА[3].
Пропусканием аммиака через раствор в петролейном эфире сульфурилхлорида и тионилхлорида получают хлорид α-сульфанура.
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.