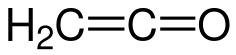Кетен
Кетен (карбометилен, этенон) — H2C=C=O, бесцветный газ с резким запахом. Простейший член гомологического ряда кетенов.
Что важно знать
Кетен
| |
|---|---|
Общие
| |
| Хим. формула | C₂H₂O |
Физические свойства
| |
| Молярная масса | 42,037 г/моль |
| Плотность | 1,93 г/см³ |
Термические свойства
| |
| Т. плав. | −150,5 ℃ |
| Т. кип. | −56,1 ℃ |
| Мол. теплоёмк. | 51,75 Дж/(моль·К) |
| Давление пара | > 1 atm (20°C) |
Классификация
| |
| Номер CAS | 463-51-4 |
| PubChem | 10038 |
| ChemSpider | 9643 |
| Номер EINECS | 207-336-9 |
| RTECS | OA7700000 |
| ChEBI | 48003 |
C=C=O
| |
InChI=1S/C2H2O/c1-2-3/h1H2
| |
| Приводятся данные для стандартных условий (25 ℃, 100 кПа), если не указано иное. | |
Строение и синтез
Первоначально основным лабораторным методом синтеза кетена являлся пиролиз ацетона в специальном аппарате — «кетеновой лампе» с выходами от 25-29 % в случае внешнего нагрева[1] до 80-90 % в кетеновых лампах со внутренним электрическим нагревом[2]. Этот метод также используется для синтеза некоторых гомологов кетена, например, метилкетена из метилэтилкетона[3].
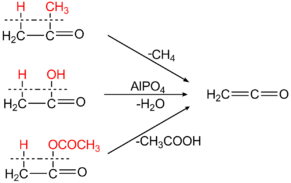
Кетен также может быть синтезирован пиролизом уксусного ангидрида или уксусной кислоты:
Кетен также образуется при действии цинка на раствор бромацетилбромида в эфире[4]:
- BrCH2COBr + Zn CH2=C=O + ZnBr2
Отщепление галогеноводорода сильными основаниями от ацеталей галогенуксусных альдегидов является препаративным методом синтеза диалкилкеталей кетена[5]:
- BrCH2CH(OEt)2 CH2=C(OEt)2 + HBr
В настоящее время благодаря доступности промышленно синтезируемого дикетена кетен обычно получают его пиролизом[2].
Промышленный синтез и применение
Кетен является крупнотоннажным продуктом промышленного органического синтеза (мощности США и Западной Европы в 1995 г. — 550 тыс. тонн), большая часть используется для производства уксусного ангидрида ацилированием уксусной кислоты[6]. В промышленности кетен получают пиролизом уксусной кислоты в присутствии триэтилфосфата или пиролизом ацетона над глинозёмом.
Кетен также используется в промышленном синтезе в реакциях [2+2]-циклоприсоединения к альдегидам.
Циклоприсоединение кетена к хлоралю с образованием соответствующего трихлорметил-β-лактона и последующим его гидролизом используется как метод синтеза яблочной кислоты, в модификации процесса, использующей в качестве хиральных индукторов на стадии [2+2]-циклоприсоединения хинина или хинидина позволяет провести реакцию стереоселективно с образованием (S)-(-)-яблочной кислоты, при этом достигает 96 %, оптическая чистота — 95 %[7].
Кетен также используется для производства капролактама (процесс Techni-Chem). На первой стадии этого процесса кетеном ацилируют циклогексанон с образованием циклогексенилацетата, который затем нитруют с отщеплением уксусной кислоты, получая 2-нитроциклогексанон. 2-Нитроциклогексанон затем подвергается гидролизу с образованием ε-нитрокапроновой кислоты, которую восстанавливают до ε-аминокапроновой кислоты; последнюю дегидратируют в капролактам при 300 °C и давлении 100 бар. Главным преимуществом Techni-Chem процесса является минимизация образования побочных продуктов, отщепляющаяся при нитровании циклогексенилацетата может быть пиролизована в кетен[8].
Реакционная способность и производные
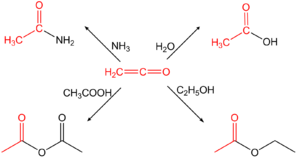
Кетен, формально являющийся внутренним ангидридом уксусной кислоты, очень реакционноспособен и является сильным ацилирующим агентом, легко присоединяющимся к нуклеофильным молекулам с образованием ацетильных производных:
- , где Х — Hal, OH, OR, OCOR, NH2, NHR, SH, SR и т. д.
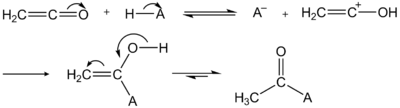
Реакция идет через образование енольного аддукта, который затем таутомеризуется в ацетильное производное:
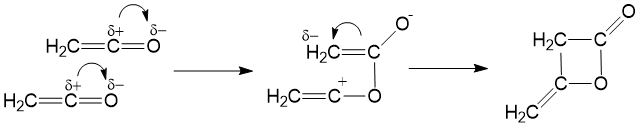
Кетен вступает в реакции [2+2]-циклоприсоединения, сам кетен димеризуется по этому механизму в дикетен при температуре выше −80 °C:
С алкенами кетен реагирует с образованием циклобутенонов.
Токсичность
Кетен — прозрачный газ с резким запахом, вызывающий раздражение глаз и дыхательных путей, чем напоминает фосген. При длительном воздействии возможен отёк лёгких.
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2 (Даф-Мед). — 671 с. — ISBN 5-82270-035-5.
- О. Я. Нейланд. Органическая химия. — М.: Высшая школа, 1990. — 751 с. — 35 000 экз. — ISBN 5-06-001471-1.