Метилацетат
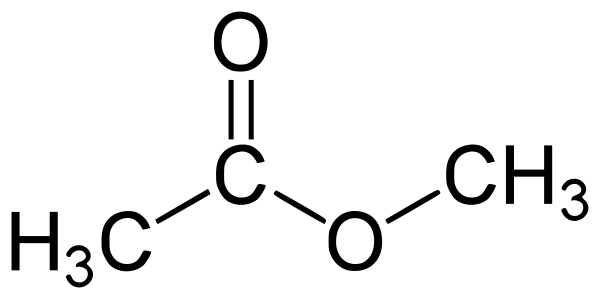
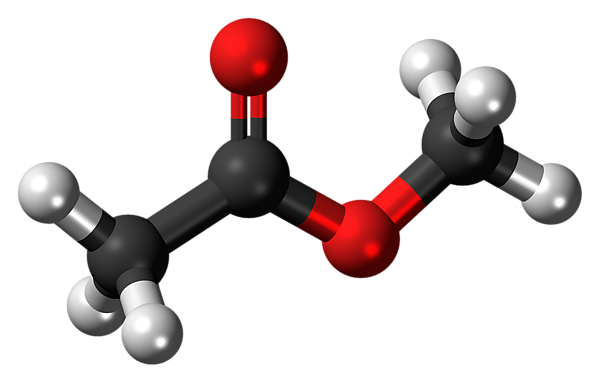
Метилацета́т (метиловый эфир уксусной кислоты, метиловый эфир этановой кислоты, уксуснометиловый эфир, MeOAc) CH3COOCH3 — органическое вещество класса сложных эфиров.
Встречается в природе, большей частью в эфирных маслах растений (например, до 8,9 % в различных видах мяты[2][3], до 28,2 % в лабазнике[4], до 44 % в жасмине[5]), и в пищевых продуктах (например, в коньяках многолетней выдержки[6]).
Общие сведения
| Метилацетат | |
|---|---|
| Общие | |
| Систематическое наименование |
метиловый эфир этановой кислоты |
| Сокращения | MeOAc |
| Традиционные названия |
метиловый эфир уксусной кислоты, уксуснометиловый эфир |
| Хим. формула | C3H6O2 |
| Рац. формула | CH3COOCH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 74.08 г/моль |
| Плотность | 0.9330 г/см³ |
| Динамическая вязкость | 0.362 Па·с |
| Энергия ионизации | 10,27 ± 0,01[1] |
| Удельное электрическое сопротивление | 0,52 Ом·м |
| Термические свойства | |
| Температура | |
| • плавления | -98.1 °C |
| • кипения | 57.1 °C |
| • вспышки | -9.4 °C |
| • воспламенения | -10 °C |
| • самовоспламенения | 470 °C |
| Пределы взрываемости | 3,15 — 15,60 % |
| Критическая точка | 233.70 |
| Мол. теплоёмк. | 156.19 Дж/(моль·К) |
| Давление пара | 0,2224 атм |
| Химические свойства | |
| Растворимость | |
| • в воде | 31,9 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1.3619 |
| Структура | |
| Дипольный момент | 1.72±0.09 Д |
| Классификация | |
| Рег. номер CAS | 79-20-9 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 6584 |
| UNII | W684QT396F |
| CompTox Dashboard EPA | DTXSID4021767 |
| Рег. номер EINECS | 201-185-2 |
| SMILES | |
| InChI | |
| RTECS | AI9100000 |
| ChEBI | 77700 |
| Номер ООН | 1231 |
| ChemSpider | 6335 |
| ECHA InfoCard | 100.001.078 |
| Безопасность | |
| Предельная концентрация | 100 мг/м³ |
| Токсичность | низкая |
| Фразы риска (R) | R11, R36, R66, R67 |
| Фразы безопасности (S) | S16, S26, S29, S33 |
| Пиктограммы СГС |
|
| NFPA 704 | |
Физические свойства
Бесцветная прозрачная жидкость с фруктовым запахом[7].
Хорошо смешивается с органическими растворителями[7]. По растворяющей способности аналогичен ацетону и применяется в ряде случаев как его заменитель. Смешивается в любых соотношениях с этанолом и этиловым эфиром, хорошо растворим в ацетоне и хлороформе, растворим в бензоле[8].
Некоторые свойства отличаются по разным источникам: плотность 0,9330[7] и 0,9244[8][9]г/см3; показатель преломления 1,3619[7] и 1,3593[8]; динамическая вязкость 0,362[7] и 0,381[8].
Растворимость в воде 31,9 %[8], образует с водой азеотропную смесь (температура кипения 56,4 °C, 96,7 % метилацетата)[7]. Образует азеотропные смеси с метанолом (температура кипения 54 °C, 81 % метилацетата) и ацетоном (температура кипения 56,1 °C, 45 % метилацетата)[10].
Образует аддукты: метилацетат•SbCl5, метилацетат•HSbCl6 и метилацетат•BF3, плавящиеся, соответственно, при 87-88, 81-82 и 65,5 °С.
Взрывоопасные концентрации в смеси с воздухом 3,15 — 15,60 %[9].
Химические свойства
По химическим свойствам метилацетат представляет собой типичный сложный эфир алифатической монокарбоновой кислоты.
Легко гидролизуется (омыляется) на исходные спирт и кислоту водой (обратимо) или щелочами (необратимо, так как образующаяся карбоновая кислота превращается в соль)[11][12]:
Восстановление метилацетата приводит к образованию двух спиртов[13] (этанол и метанол):
Под действием аммиака метилацетат превращается в ацетамид и метанол[14]:
Получение
Метилацетат получают:
- этерификацией уксусной кислоты метанолом в жидкой фазе в присутствии серной кислоты (или при пропускании смеси паров указанных жидкостей над нагретыми катализаторами: FeCl3, AlCl3)[7]:
- из уксусного ангидрида и метанола[7] (реакция протекает в жидкой фазе в отсутствии катализатора и является практически необратимой[15]):
- ,
- по реакции Байера-Виллигера воздействием перкарбоновой кислоты на ацетон в присутствии кислот Льюиса как катализатора (например, BF₃):
- ,
Применение
Метилацетат применяют, в основном, в качестве растворителя в производстве лакокрасочных материалов и как компонент многих промышленных и бытовых растворителей. Является составной частью (7-75 %) лесохимических растворителей[16][9].
Используется при производстве клеев, композиционных лаков, шпатлёвок, магнитных лент, автокосметики, эфиров целлюлозы, поливинилацетата, полиметилметакрилата, растительных и животных жиров, многих синтетических смол[16][9].
Применяется как экстрагент в аналитической химии, в том числе для отделения LiCl от хлоридов других щелочных металлов[17].
Метилацетат является ценным компонентом для промышленного синтеза, в том числе — из него карбонилированием получают уксусный ангидрид (процесс Реппе)[18][19]:
Используется в пищевой промышленности в качестве ароматизатора[17][20] и экстрактивного растворителя в процессе декофеинизирования чая и кофе[21]. В качестве ароматизатора и растворителя также входит в состав ряда косметических средств.
Токсичность, охрана труда
Слабо раздражает слизистые оболочки глаз и дыхательных путей (при концентрации 15 мг/л химически чистого метилацетата для ощущения раздражения требуется 5-минутная экспозиция). В высоких концентрациях оказывает лёгкое наркотическое воздействие, — в основном, за счёт действия самого сложного эфира, и, в меньшей степени, — за счёт образующегося из него спирта[9].
При пероральном введении ЛД50 = 2,9 г/кг (белые крысы), 2,4 г/кг (мыши и кролики), 3,6 г/кг (морские свинки)[9].
ПДК в атмосферном воздухе населённых мест 0,07 мг/м³[22].
По данным Роспотребнадзора, ПДК в воздухе рабочей зоны равна 100 мг/м3 (максимально-разовая)[23]. Однако по данным ряда исследований, порог восприятия запаха этого вещества может быть гораздо выше этой ПДК. Например, среднее значение порога в исследовании[24] было 900 мг/м3; в[25] 5250 мг/м3; а в[26] 8628 мг/м3. Поэтому можно ожидать, что использование широко распространённых фильтрующих СИЗОД в сочетании с «заменой фильтров по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками СИЗОД) приведёт к чрезмерному воздействию паров метилацетата на, по крайней мере, часть работников — из-за несвоевременной замены противогазных фильтров. Для защиты от метилацетата следует использовать значительно более эффективные изменение технологии и средства коллективной защиты.
Примечания
Литература
- Редкол.: Кнунянц И. Л. и др. Химическая энциклопедия, том 3. — М.: Советская энциклопедия, 1992. — 639 с. — ISBN 5-85270-039-8.
- Kirk-Othmer Encyclopedia, 3 td., v. 4, N.Y., 1978, p. 142—143
- Held H., Rengst A., Mayer D. Acetic Anhydride and Mixed Fatty Acid Anhydrides // Ullmann's Encyclopedia of Industrial Chemistry. — Wiley, 2000. — doi:10.1002/14356007.a01_065.
- Лазарев Н. В.. Вредные вещества в промышленности. том II. — Л.: Химия, 1976. — 624 с.
- Рабинович В. А., Хавин З. Я. Краткий химический справочник. — Л.: Химия, 1977. — 376 с.
- «NIOSH Pocket Guide to Chemical Hazards. Methyl acetate» (англ.). Национальный институт охраны труда (NIOSH). Дата обращения: 28 февраля 2016.
- Метилацетат. Паспорт безопасности. Дата обращения: 28 февраля 2016.