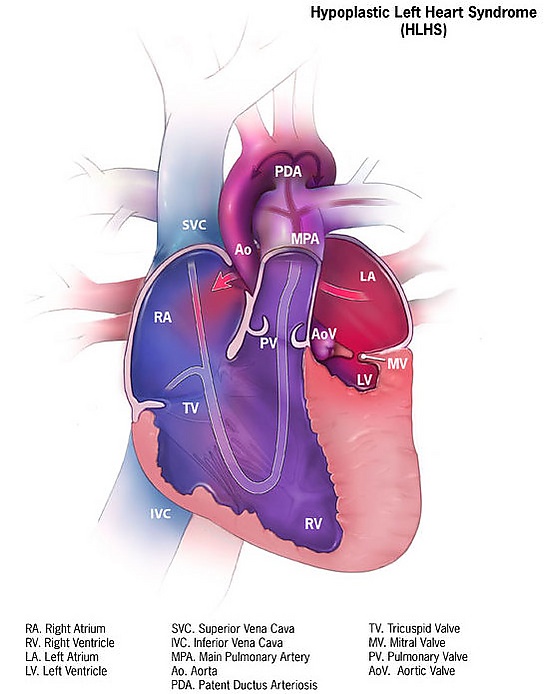
Синдром гипоплазии левых отделов сердца
Синдро́м гипоплази́и ле́вых отде́лов се́рдца (гипоплазия левых отделов сердца, англ. Hypoplastic left heart syndrome) — клинический синдром, который характеризуется наличием таких врождённых пороков сердца, как умеренная или выраженная гипоплазия или атрезия митрального клапана, левого желудочка, аортального клапана и различной степени гипоплазия восходящей аорты[3]. Основной функциональной особенностью синдрома является неспособность левых отделов сердца поддерживать адекватный системный сердечный выброс сразу после рождения, что делает состояние критическим и угрожающим жизни новорождённого. Если нормальное закрытие открытого артериального протока не предотвращается инфузией простагландина, то в течение первых нескольких дней жизни развивается кардиогенный шок и смерть[4]. Этиология синдрома считается многофакторной: роль играют генетические мутации (например, в генах NKX2‑5 и GJA1) и дефекты, влияющие на кровоток в сердце[5]. По данным различных источников, синдром гипоплазии левых отделов сердца составляет 1,4 до 9 % всех врождённых пороков сердца[3].
Диагноз обычно ставят внутриутробно с помощью эхокардиографии плода или вскоре после рождения при неотложной эхокардиографии[4]. Лечение направлено на поддержание жизнеспособности и последующую хирургическую коррекцию. Стандартная схема включает трёхэтапное паллиативное вмешательство: операцию Норвуда в первые дни жизни, операцию Гленна в возрасте 3—6 месяцев и операцию Фонтена в возрасте 2—4 лет. В некоторых случаях рассматривается трансплантация сердца[6].
Общие сведения
История
Синдром гипоплазии левых отделов сердца впервые был описан в 1814 году английским врачом Дж. Р. Фарре[5]. В 1952 году М. Лев представил более подробное морфологическое описание данного порока[6]. В 1958 году Дж. А. Нунан и А. С. Надас выделили его в отдельный синдром и ввели термин «гипоплазия левых отделов сердца» для обозначения комплекса врождённых аномалий, характеризующихся недоразвитием структур левой половины сердца, часто в сочетании с атрезией аортального и митрального клапанов[5][6].
Первые попытки хирургической коррекции предпринимались с 1961 года, однако длительное время они оставались безуспешными. Значительный прогресс в лечении стал возможен благодаря развитию анестезиологии, интенсивной терапии и кардиохирургии во второй половине XX века. В 1981 году В. Норвуд выполнил первую успешную хирургическую коррекцию у новорождённого с гипоплазией левых отделов сердца, что стало основой для разработки современных этапных методов лечения[5].
Классификация
Общепризнанной классификации синдрома гипоплазии левых отделов сердца не существует. В практике используется классификация, основанная на морфологии клапанов левых отделов сердца. Выделяют пять анатомических подтипов синдрома гипоплазии левых отделов сердца[3]:
- аортальный и митральный стеноз;
- аортальная и митральная атрезия;
- аортальная атрезия и митральный стеноз;
- аортальный стеноз и митральная атрезия;
- комплекс гипоплазии левых отделов сердца.
Этиология
Этиология синдрома гипоплазии левых отделов сердца остаётся окончательно не установленной и рассматривается как многофакторная, включающая сложное взаимодействие генетических, эмбриональных и внешнесредовых факторов[3].
Существенную роль в развитии синдрома гипоплазии левых отделов сердца играют генетические факторы. У части пациентов выявляются мутации в генах, регулирующих кардиогенез, в частности в гене NKX2-5, кодирующем транскрипционный фактор, необходимый для нормального формирования сердца. Описана гетерозиготная миссенс-мутация R25C, встречающаяся приблизительно у 5—7 % пациентов, которая нарушает регуляцию экспрессии генов-мишеней и может приводить к формированию врождённых пороков сердца, включая синдром гипоплазии левых отделов сердца. Также выявлены изменения в гене GJA1, кодирующем коннексин-43 — основной белок щелевых контактов кардиомиоцитов, обеспечивающий межклеточную электрическую и метаболическую связь. Нарушение функции данного белка способно влиять как на эмбриональное формирование миокарда, так и на его функциональную организацию[5].
Кроме того, в патогенез вовлечены и другие гены, включая HAND1, NOTCH1, ZIC3, MYH6, MCTP2 и ряд других, что подтверждает полигенный характер заболевания[7]. Существует небольшой риск рецидива при последующих беременностях, который оценивается в 2—4 % и возрастает до 25 % в семьях, где двое детей больны[8]. Считается, что это связано с генетическими мутациями с неполной пенетрантностью и вариабельной экспрессивностью генетических нарушений[9].
Синдром гипоплазии левых отделов сердца нередко сочетается с хромосомными аномалиями и генетическими синдромами. Наиболее часто он ассоциирован с синдром Шерешевского — Тёрнера, а также с синдром Патау, синдром Эдвардса и частичной трисомией 9-й хромосомы. Описаны сочетания с синдром Якобсена, синдром Холт — Орама, синдром Смита — Лемли — Опитца, синдром Нунан, а также с ассоциацией CHARGE. В целом генетические синдромы выявляются примерно у 10—25 % пациентов, что подчёркивает значимость хромосомных и моногенных нарушений в развитии данного порока[3][10].
Существенное значение имеют и эмбриональные механизмы. В большинстве случаев выявляется первичное поражение аортального и/или митрального клапанов в виде стеноза или атрезии, что приводит к нарушению внутрисердечной гемодинамики. Также описаны аномальное формирование и смещение первичной межпредсердной перегородки влево и нарушения формирования овального окна, включая его рестрикцию или атрезию, что ограничивает приток крови к левым отделам сердца и препятствует их нормальному развитию[3].
Несмотря на то что во многих случаях синдром гипоплазии левых отделов сердца возникает спорадически[8], предполагается роль ряда факторов риска, связанных как с состоянием матери, так и с воздействием окружающей среды.
К материнским факторам относятся сахарный диабет, ожирение, дефицит фолиевой кислоты, пожилой возраст матери, а также возможные метаболические нарушения во время беременности. Эти состояния могут оказывать влияние на процессы эмбриогенеза и повышать вероятность формирования врождённых пороков сердца[6][7].
Среди факторов окружающей среды рассматриваются внутриутробные инфекции, включая вирусные заболевания, воздействие тератогенов, а также влияние загрязнителей окружающей среды, таких как полициклические ароматические углеводороды (например, бензпирен), агрохимикаты и загрязнение грунтовых вод. Наблюдаемая сезонная и географическая вариабельность распространённости гипоплазии левых отделов сердца также косвенно указывает на возможное участие внешних факторов[7].
Патогенез
Патогенез синдрома гипоплазии левых отделов сердца представляет собой сложный многоэтапный процесс, включающий нарушения эмбрионального формирования сердечных структур и последующие гемодинамические изменения, развивающиеся как во внутриутробном, так и в постнатальном периодах. Ключевым звеном является нарушение развития левых отделов сердца на ранних этапах эмбриогенеза, преимущественно в период с 4-й по 8-ю неделю гестации. В основе лежит первичное поражение клапанного аппарата, прежде всего аортального и митрального клапанов, либо изменения внутрисердечной гемодинамики, приводящие к снижению кровотока через левый желудочек. В большинстве случаев выявляются стеноз или атрезия аортального и/или митрального клапанов различной степени выраженности. При митральном стенозе или атрезии уменьшается приток крови в левый желудочек, тогда как при аортальном стенозе возрастает сопротивление выбросу крови из него. Это приводит к уменьшению объёмной и механической нагрузки на левый желудочек, снижению его перфузии и, как следствие, к задержке его роста и дифференцировки[6].
Недостаточная гемодинамическая нагрузка на миокард сопровождается снижением пролиферации кардиомиоцитов и нарушением формирования нормальной архитектоники левого желудочка. В результате он остаётся резко уменьшенным в размерах и функционально несостоятельным. Параллельно уменьшается кровоток в восходящей аорте и дуге аорты, что приводит к их гипоплазии; в тяжёлых случаях восходящая аорта имеет минимальный диаметр и функционирует преимущественно как канал для ретроградного кровотока[6][7].
Дополнительным механизмом является нарушение формирования межпредсердного сообщения. Рестрикция или атрезия овального окна приводит к повышению давления в левом предсердии, затруднению оттока крови из лёгочных вен и формированию венозного застоя в малом круге кровообращения. Это, в свою очередь, усугубляет нарушения лёгочной гемодинамики и дополнительно ограничивает приток крови к левому желудочку. Также описано аномальное смещение первичной межпредсердной перегородки влево, что способствует уменьшению наполнения левых отделов сердца[3].
Во внутриутробном периоде гемодинамика частично компенсируется за счёт особенностей фетального кровообращения. Основной объём крови проходит через правые отделы сердца, из правого желудочка кровь поступает в лёгочную артерию и далее через открытый артериальный проток — в аорту. При этом системный кровоток в значительной степени обеспечивается через артериальный проток, а кровоснабжение коронарных и брахиоцефальных артерий осуществляется ретроградно через дугу и восходящую аорту. Эти условия позволяют поддерживать жизнедеятельность плода, однако одновременно способствуют сохранению сниженного кровотока через левые отделы и их дальнейшей гипоплазии. После рождения происходит резкая перестройка кровообращения, которая у пациентов с данным пороком приводит к критическим нарушениям. Левый желудочек не способен обеспечивать системный кровоток, и его функция фактически выключается из системной циркуляции. Единственным функционально активным насосом становится правый желудочек, который обеспечивает кровоснабжение как лёгочного, так и системного кругов кровообращения. Лёгочная венозная кровь, поступающая в левое предсердие, не может адекватно перейти в левый желудочек и через межпредсердное сообщение направляется в правое предсердие, где смешивается с венозной кровью. В результате формируется смешанный кровоток с пониженной оксигенацией, поступающий в системное русло. Кровоснабжение органов и тканей осуществляется за счёт выброса правого желудочка в лёгочную артерию с последующим поступлением крови в аорту через открытый артериальный проток. Таким образом, системное кровообращение становится зависимым от проходимости артериального протока и состояния межпредсердного сообщения[7].
Существенное значение имеет соотношение лёгочного и системного сосудистого сопротивления. После рождения физиологическое снижение лёгочного сосудистого сопротивления приводит к увеличению лёгочного кровотока и относительному уменьшению системной перфузии, что может вызывать гипоперфузию жизненно важных органов, метаболический ацидоз и органную дисфункцию. В противоположной ситуации, при повышенном лёгочном сопротивлении, увеличивается системный кровоток, однако усиливается гипоксемия[6][7].
Закрытие артериального протока приводит к резкому прекращению системного кровотока, тяжёлой гипоперфузии, ишемии органов и развитию кардиогенного шока. Перфузия коронарных артерий и головного мозга осуществляется за счёт ретроградного кровотока через дугу аорты, что делает их крайне чувствительными к изменениям гемодинамики[6].
Хроническая перегрузка правого желудочка приводит к его дилатации и гипертрофии, однако без хирургической коррекции он не способен длительно поддерживать адекватную гемодинамику[6][7].
Эпидемиология
Синдром гипоплазии левых отделов сердца относится к редким врождённым порокам сердца и составляет в среднем от 1,4 до 9 % всех врождённых пороков сердца[3]. В неонатальном периоде синдром гипоплазии левых отделов сердца рассматривается как один из наиболее частых пороков, сопровождающихся одножелудочковой гемодинамикой, и занимает одно из ведущих мест среди критических врождённых пороков сердца, требующих неотложного вмешательства[6].
Распространённость синдрома гипоплазии левых отделов сердца среди живорождённых составляет приблизительно 0,16—0,36 на 1000 новорождённых[3].
Заболевание чаще встречается у лиц мужского пола, доля которых составляет приблизительно 55—70 %[7], при соотношении мальчиков и девочек около 1,5:1[6].
Синдром гипоплазии левых отделов сердца является одной из ведущих причин смертности новорождённых от врождённых пороков сердца. По данным наблюдений, без хирургического лечения большинство пациентов погибает в первые месяцы жизни — до 25 % летальных исходов приходится на первую неделю после рождения[3]. В структуре смертности от врождённых пороков сердца в неонатальном периоде синдром гипоплазии левых отделов сердца может составлять до 20—25 % случаев[7].
В большинстве случаев заболевание возникает спорадически, однако примерно у 10—25 % пациентов выявляются ассоциированные хромосомные аномалии или генетические синдромы[3].
По данным Национальной сети профилактики врождённых дефектов, врождённые дефекты встречаются примерно у трёх процентов детей, родившихся живыми в Соединённых Штатах. Среди этих дефектов синдром гипоплазии левых отделов сердца встречается в среднем у одного из 4344 новорождённых, что составляет в общей сложности около 960 новорождённых каждый год в Соединённых Штатах[11][12][13].
Диагностика
Клинические проявления синдрома гипоплазии левых отделов сердца в неонатальном периоде во многом определяются состоянием фетальных коммуникаций — открытого артериального протока и межпредсердного сообщения, а также соотношением лёгочного и системного сосудистого сопротивления. В первые часы и даже дни после рождения новорождённые могут выглядеть относительно стабильными, поскольку системный кровоток поддерживается за счёт функционирования артериального протока, а адекватное смешение крови обеспечивается через овальное окно[7].
По мере физиологического закрытия артериального протока, которое обычно происходит в течение первых 24—48 часов жизни, развивается быстро прогрессирующее ухудшение состояния. Клиническая картина формируется остро и характеризуется признаками тяжёлой сердечно-сосудистой недостаточности и кардиогенного шока. У ребёнка появляются бледность или серовато-синюшная окраска кожных покровов, нередко сочетающаяся с акроцианозом/цианозом, усиливающимся при беспокойстве, прохладная липкая кожа, выраженная вялость и снижение активности. Отмечаются нарушения дыхания в виде тахипноэ, одышки и признаков дыхательной недостаточности. Характерны трудности кормления или полный отказ от него[3][4].
Нарушение системной перфузии проявляется слабостью или отсутствием периферического пульса, похолоданием конечностей, снижением артериального давления и признаками централизации кровообращения[3]. Быстро нарастают проявления метаболического ацидоза, олигурии или анурии, что отражает гипоперфузию жизненно важных органов, включая почки, печень и кишечник. В ряде случаев формируются признаки полиорганной недостаточности[6][4].
Особое значение имеет состояние межпредсердного сообщения. Примерно у 5—6 % новорождённых наблюдается его рестрикция или атрезия, что приводит к резкому затруднению оттока крови из левого предсердия. В этих условиях быстро развивается застой в лёгочных венах, посткапиллярная лёгочная гипертензия и интерстициальный отёк лёгких. Такие пациенты характеризуются крайне низким уровнем оксигенации крови, выраженной дыхательной недостаточностью и требуют неотложного вмешательства, направленного на декомпрессию левого предсердия[3][7].
При физикальном обследовании выявляются тахикардия, тахипноэ, признаки дыхательной недостаточности и цианоз различной степени выраженности. Пальпаторно часто определяется увеличение печени, отражающее венозный застой. Периферическая перфузия снижена, конечности холодные, пульс слабый или нитевидный. Аускультативная картина может быть скудной: характерен умеренный систолический шум по левому краю грудины, обусловленный кровотоком через открытый артериальный проток, при этом второй тон сердца обычно одиночный и может быть усилен. В ряде случаев шумы могут отсутствовать, что связано с особенностями гемодинамики[3][7].
При отсутствии своевременной медицинской помощи состояние новорождённых быстро прогрессирует от начальных признаков дыхательной и сердечной недостаточности к кардиогенному шоку и летальному исходу[7].
Синдром гипоплазии левых отделов сердца включает в себя различные комбинации шести следующих поражений и недоразвитий структур сердечно-сосудистой системы в сочетании с гипоплазией левого желудочка сердца[3]:
- порок митрального клапана (выраженная гипоплазия; стеноз; атрезия);
- фиброэластоз структур левых отделов;
- порок аортального клапана (выраженная гипоплазия; стеноз; атрезия);
- гипоплазия восходящей аорты;
- гипоплазия/перерыв дуги аорты;
- коарктация аорты.
Частота сопутствующих пороков сердца на фоне синдрома составляет около 25 % — наиболее часто это дефекты межжелудочковой и/или межпредсердной перегородки, поражение трёхстворчатого клапана и клапана лёгочной артерии, атрезия лёгочных вен, другие сочетания встречаются значительно реже
- Клинический анализ крови — проводится оценка уровня гемоглобина и гематокрита; выявление анемии или полицитемии, которые могут усугублять цианоз и сердечную недостаточность. Лейкоцитарная формула — контроль за инфекционными осложнениями[3].
- Клинический анализ мочи проводится для оценки почечной функции при критическом состоянии новорождённого[3].
- Биохимический анализ крови — проводится исследование концентрации калия, натрия, хлоридов, глюкозы, креатинина, общего белка, альбумина, мочевины, общего и связанного (конъюгированного) билирубина в крови, исследование уровня железа сыворотки крови, определение активности аспартатаминотрансферазы и аланинаминотрансферазы в крови для оценки почечной и печёночной функции в рамках первичного обследования, при поступлении в стационар, в том числе для оперативного лечения. Позволяет оценить системную перфузию, метаболический статус и выявить почечную или печёночную дисфункцию[3].
- Газовый состав крови и кислотно-основное состояние — определение pH, pCO₂, pO₂, BE, лактата. Оценка сбалансированности кровотока между малым и большим кругом кровообращения. Контроль метаболического ацидоза и гипоксемии, особенно при критическом состоянии[3].
- Коагулограмма — исследование АЧТВ, МНО, фибриноген — для исключения врождённых и приобретённых нарушений свёртываемости крови перед операцией[3].
- Групповые и серологические тесты перед операцией — определение группы крови (AB0), резус-фактора, антиэритроцитарных антител, HBsAg, антител к ВИЧ-1, ВИЧ-2, вирусу гепатита C, Treponema pallidum[3].
- Генетические исследования — кариотипирование детям с дисморфологическими признаками для исключения синдромов Шерешевского — Тёрнера, Ди Джорджи, Дауна и других[7].
- Ультразвуковое исследование плода — позволяет выявлять синдром гипоплазии левых отделов сердца уже с 16—20-й недели беременности. Однако порок выявляется во время беременности лишь у 18—60 % плодов с синдромом[5]:
- гипоплазия левого желудочка и восходящей аорты;
- аномалии митрального и аортального клапанов;
- оценка потоков через митральный и аортальный клапаны, открытый артериальный проток, межпредсердное сообщение.
- Эхокардиография — основной метод подтверждения синдрома гипоплазии левых отделов сердца у новорождённых. Позволяет выявить гипоплазию, аномальное строение, стеноз или атрезию митрального клапана; гипоплазию, стеноз или атрезию аортального клапана; гипоплазию восходящей аорты, дуги аорты и/или перешейка аорты; выявить или исключить наличие антеградного потока через митральный и аортальный клапаны; определить линейные размеры левого желудочка и степень выраженности фиброэластоза; размеры межпредсердного сообщения и открытого артериального протока; оценить кровоток в брюшной аорте, оценить функцию правого желудочка и трёхстворчатого клапана[3].
- Электрокардиография — проводится для оценки сердечного ритма и проводимости. Изменения на электрокардиограмме неспецифические и проявляются признаками перегрузки правых отделов сердца, а именно[3]:
- остроконечные, расширенные зубцы P во II, III, и AVF отведениях;
- отклонение электрической оси сердца вправо;
- признаки увеличения правого желудочка с появлением зубцов R в V1, или qR в правых грудных отведениях, зубцы rS в V5—V6.
- Рентгенография органов грудной клетки — проводится для исключения иных заболеваний сердца и крупных сосудов, а также внесердечной патологии (патологии других органов средостения, лёгких, плевры), состояния малого круга кровообращения и выявления лёгочного застоя, а также в случае оперативного лечения при необходимости в пред- и/или послеоперационном периоде. На обзорной рентгенограмме практически всегда отмечается полнокровие с интерстициальным или альвеолярным отёком лёгких (или без отёка). Также рентгенография грудной клетки позволяет выявить сопутствующие заболевания лёгких (пневмонию, мекониальную аспирацию, ателектазы и другие)[3].
- Компьютерная томография и магнитно-резонансная томография сердца и магистральных сосудов — проводятся в тех случаях, когда данных эхокардиографии недостаточно для верификации диагноза или они противоречивы. Магнитно-резонансная томография и компьютерная томография помогают уточнить морфологию порока, определить пространственное взаимоотношение структур сердца и крупных сосудов, а также важны для диагностики сопутствующих внутрисердечных/внесердечных аномалий развития. Также томографические методики применяются при пограничных размерах левых отделов сердца, что позволяет уточнить возможность выполнения операций двухжелудочковой коррекции и хирургическую тактику у данной группы пациентов[3].
- Нейросонография — проводится для исключения аномалий головного мозга у новорождённых с синдромом гипоплазии левых отделов сердца[3].
- Суточное мониторирование жизненно важных функций (частота сердечных сокращений, артериально давление, пульсоксиметрия) — контроль состояния пациента до и после операции[3].
Дифференциальная диагностика
Дифференциальная диагностика синдрома гипоплазии левых отделов сердца проводится со следующими заболеваниями:
- критический аортальный стеноз;
- коарктация аорты;
- синдром Шона;
- перерыв дуги аорты;
- общий аномальный лёгочный венозный возврат;
- атрезия лёгочной артерии с интактной межжелудочковой перегородкой;
- аномалия Эбштейна[6];
- врождённые пороки развития центральной нервной системы;
- диафрагмальная грыжа;
- некротический энтероколит;
- митральный стеноз;
- эндокардиальный фиброэластз;
- неонатальный сепсис[7].
Осложнения
Синдром гипоплазии левых отделов сердца, как вариант однокамерного кровообращения, сопровождается рядом пред- и послеоперационных осложнений[6].
К предоперационным осложнениям относятся кардиогенный шок при закрытии артериального протока, выраженный цианоз вследствие смешения крови, рестриктивное овальное окно с застоем в лёгочных венах и снижением сердечного выброса, аритмии, а также метаболические нарушения (ацидоз), сердечная, почечная и печёночная недостаточность. В тяжёлых случаях возможны некротический энтероколит, сепсис и летальный исход[6][7].
Послеоперационные осложнения зависят от этапа хирургического лечения. После операции Норвуда возможны тромбоз шунта, коронарный синдром «кражи», аритмии, дыхательная недостаточность, кровотечения, инфекции и почечная дисфункция. После операции Гленна отмечаются снижение лёгочного кровотока, аритмии и тромбоэмболические осложнения. После операции Фонтена характерны хроническая венозная гипертензия, предсердные аритмии, пластический бронхит, протеинтеряющая энтеропатия, поражение печени (вплоть до цирроза и гепатоцеллюлярной карциномы), а также тромбоэмболические осложнения[6].
В послеоперационном периоде также могут наблюдаться ацидоз, сердечная, почечная и печёночная недостаточность, тромбозы, некротический энтероколит, сепсис, перикардиальный и плевральный выпот, инсульт, повреждение диафрагмального или возвратного гортанного нерва, а также рекоарктация аорты и летальный исход. После трансплантации сердца возможны раннее отторжение трансплантата и развитие оппортунистических инфекций[7].
Отдельное значение имеет риск тромбозов: примерно у 20 % младенцев в межоперационном периоде (между первым и вторым этапами лечения) развивается тромбоз, что связано с длительностью искусственного кровообращения, продолжительным пребыванием в отделении интенсивной терапии и более низкой сатурацией кислорода при выписке[7].
Лечение
Родоразрешение рекомендуется проводить в специализированном стационаре не ниже III уровня, оснащённом отделением реанимации новорождённых и расположенном в непосредственной близости от кардиохирургического центра. Это необходимо для немедленной диагностики, стабилизации состояния и начала терапии[3].
Оптимальный срок родоразрешения — около 39 недель гестации. Возможны как естественные роды, так и плановое кесарево сечение. Выбор метода определяется акушерскими показаниями и необходимостью координации мультидисциплинарной помощи[3].
При наличии рестриктивного овального окна или интактной межпредсердной перегородки родоразрешение предпочтительно в кардиохирургическом центре, так как может потребоваться экстренное вмешательство (баллонная атриосептостомия, стентирование межпредсердной перегородки или проведение ЭКМО)м.
После рождения ребёнок подлежит немедленному переводу в отделение реанимации новорождённых с последующей транспортировкой в кардиохирургический стационар в первые 24—48 часов жизни[3].
Консервативная терапия направлена на поддержание адекватного системного кровотока и стабилизацию гемодинамики до хирургического вмешательства. Ключевым элементом является поддержание проходимости артериального протока с помощью инфузии простагландина E1. Всем пациентам обеспечивается сосудистый доступ и проводится мониторинг жизненно важных функций[3].
Важной задачей является баланс между лёгочным и системным кровотоком. Для предотвращения избыточного лёгочного кровотока избегают гипероксии, алкалоза и гипокапнии; оксигенотерапия обычно не требуется при сатурации 75—85 %. При необходимости проводится искусственная вентиляция лёгких с контролем газового состава крови[3].
Проводится коррекция метаболического ацидоза, поддержание нормотермии и адекватного объёма циркулирующей крови. При развитии сердечной недостаточности применяются инотропные препараты (добутамин, допамин, милринон), вазодилататоры (например, нитропруссид натрия), а также диуретики[3].
При рестриктивном межпредсердном сообщении показано экстренное выполнение баллонной атриосептостомии. В отдельных случаях может потребоваться антибактериальная терапия и тромбопрофилактика[3].
Основным методом лечения является этапная паллиативная хирургическая коррекция, направленная на формирование одножелудочковой гемодинамики[6][3][4]:
1. Операция Норвуда (1-й этап) — выполняется в первую неделю жизни и направлен на обеспечение системного кровотока за счёт правого желудочка с созданием контролируемого лёгочного кровообращения. В ходе вмешательства основная лёгочная артерия пересекается, дистальная культя закрывается лоскутом, а гипопластическая аорта и проксимальная часть лёгочной артерии объединяются, формируя неоаорту. Артериальный проток перевязывают, так как неоаорта теперь обеспечивает системное кровообращение. Лёгочный кровоток восстанавливается с помощью правостороннего модифицированного шунта Блэлока-Тауссига или кондуита от правого желудочка к лёгочной артерии по модификации Сано. При необходимости создаётся или расширяется соединение в межпредсердной перегородке, чтобы облегчить отток крови и снизить давление в правом предсердии. У пациентов высокого риска, например недоношенных детей или детей с низкой массой и мультисистемной дисфункцией, может применяться гибридный подход, включающий стентирование артериального протока и бандажирование лёгочных артерий, что позволяет контролировать поток крови и уменьшить хирургический риск.
2. Операция Гленна (2-й этап) — проводится в возрасте 3—6 месяцев и и направлен на снижение нагрузки на единственный желудочек. При двунаправленном кавопульмональном анастомозе верхняя полая вена соединяется с правой лёгочной артерией, что позволяет примерно половине венозной крови верхней половины тела обходить правое предсердие и поступать непосредственно в лёгкие для оксигенации. Вариант процедуры — геми-Фонтен — предусматривает соединение верхней полой вены с лёгочной артерией без полной её изоляции от правого предсердия. После этой операции нагрузка на желудочек снижается, а подготовка к финальному этапу становится безопаснее.
3. Операция Фонтена (3-й этап) — выполняется в возрасте 18—36 месяцев (2—4 лет) ии завершает последовательное разделение большого и малого кругов кровообращения. Поток крови из нижней полой вены перенаправляется к кавопульмональному анастомозу, соединяющему верхнюю полую вену и лёгочную артерию, что позволяет полностью обеспечить пассивный лёгочный кровоток. Перенаправление может выполняться через межпредсердную перегородку или с использованием экстракардиального трансплантата. После завершения операции Фонтена единственный желудочек работает исключительно на системное кровообращение, а насыщение крови кислородом стабилизируется, создавая условия для нормального роста и развития ребёнка.
Альтернативой у пациентов высокого риска может быть гибридный подход, который сочетает интервенционные и хирургические методы и позволяет временно стабилизировать кровообращение без проведения полной реконструкции сердца. При этом стентирование артериального протока обеспечивает поддержание системного кровотока, а бандажирование лёгочных артерий ограничивает избыточный поток крови в лёгкие и снижает нагрузку на правый желудочек. Гибридный метод используется у недоношенных детей, пациентов с низкой массой тела или с тяжёлыми сопутствующими состояниями и создаёт условия для роста ребёнка и подготовки к последующим этапам паллиативной коррекции. После завершения всех этапов хирургического лечения формируется эффективная одножелудочковая гемодинамика, позволяющая единственному желудочку перекачивать системную кровь, обеспечивая стабильное насыщение крови кислородом и поддерживая нормальный рост и развитие ребёнка[6][7].
В тяжёлых случаях с выраженной дисфункцией правого желудочка или клапанного аппарата рассматривается трансплантация сердца[6].
Прогноз
Прогноз при синдроме гипоплазии левых отделов сердца зависит от своевременности и этапности хирургического лечения. Без вмешательства значительная часть новорождённых погибает в раннем неонатальном периоде. До завершения поэтапной паллиативной коррекции смертность может достигать 70 %, тогда как после её выполнения снижается до примерно 1—5 %. По данным крупных регистров, госпитальная летальность составляет около 15 % после операции Норвуда, 1,8 % после операции Гленна и около 1 % после операции Фонтена. Даже при успешном хирургическом лечении пациенты подвержены риску нарушений нейропсихического развития. Часто отмечаются задержка развития, когнитивные нарушения (снижение внимания, памяти, скорости обработки информации), а также трудности обучения и поведенческие проблемы. Эти изменения связаны с хронической гипоксией, особенностями внутриутробного кровообращения и влиянием хирургических вмешательств[6][7].
Диспансерное наблюдение
После выполнения каждого этапа гемодинамической коррекции пациенты должны находиться под регулярным наблюдением врача-детского кардиолога с целью своевременного выявления гемодинамических нарушений, требующих медикаментозной или повторной хирургической коррекции[3].
В межоперационном периоде наблюдение осуществляется как на амбулаторном уровне, так и в специализированных центрах. По месту жительства необходимы регулярные осмотры врача-педиатра не реже одного раза в две недели, а также более частое наблюдение детским кардиологом: в первые два месяца жизни — не реже одного раза в неделю, далее — не реже одного раза в месяц. Такое динамическое наблюдение позволяет своевременно оценивать состояние ребёнка, выявлять признаки сердечной недостаточности, нарушения перфузии и другие осложнения[3].
После каждого этапа хирургического лечения пациенты подлежат обязательному обследованию в специализированном кардиохирургическом стационаре не реже одного раза в три месяца в межэтапный период и в течение первого года после выполнения операции Fontan. В дальнейшем, спустя год после завершения этапа Fontan, рекомендуется пожизненное наблюдение в специализированном центре с частотой не реже одного раза в год, оптимально — два раза в год[3].
В рамках диспансерного наблюдения при каждом обследовании проводится эхокардиография[3].
Учитывая высокий риск неврологических нарушений, всем пациентам с синдромом гипоплазии левых отделов сердца также показано регулярное наблюдение у врача-невролога по месту жительства, что позволяет своевременно выявлять и корректировать последствия гипоксии и возможные нарушения развития[3].
Профилактика
Специфических мер профилактики не разработано. Пренатальная ультразвуковая диагностика позволяет снизить смертность детей с синдромом гипоплазии левых отделов сердца[5].
Примечания
Ссылки
- HLHS Information Page Questions to ask medical professionals and insurance company, plus resources
- Hypoplastic Left Heart Syndrome information from Seattle Children’s Hospital Heart Center
- Card-AG, The Cardiologycal Working Group of the University Pediatric Clinic Munster
- Hypoplastic Left Heart Syndrome, American Heart Association
- Overview at Cincinnati Children’s Hospital Medical Center
- Overview at University of Michigan Congenital Heart Center
- Cardiac Center at The Children’s Hospital of Philadelphia
- Hypoplastic left heart syndrome information for parents.
- Little Hearts Matter, a charity providing support and information on HLHS and other single ventricle heart defects
- Baby Hearts Press
- www.congenitalheartdefects.com
- 120+ stories of children born with Hypoplastic Left Heart Syndrome hosted by the The Congenital Heart Information Network.
- HLHS email support groups/discussion list hosted by the The Congenital Heart Information Network (membership required).
- Little Hearts, Inc. — Providing hope with stories of children with HLHS and other CHDs. Email support group (membership required)
- HeartLine, a charity for children with heart conditions and their families
- Designer Heart, A Congenital Heart Defect Network.
- It’s My Heart, a non-profit organization created to provide support to and advocating for those affected by Acquired and Congenital Heart Defects.