Хлорацетальдегид
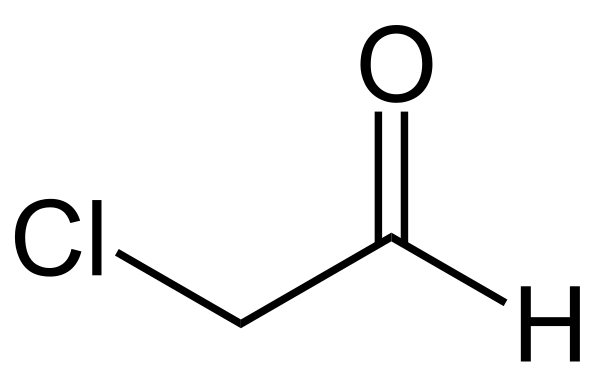
Хлорацетальдегид (монохлорацетальдегид, хлорэтаналь, хлоруксусный альдегид) — хлорорганическое соединение класса альдегидов с одной карбонильной группой с формулой ClCH2CHO.
Обычно встречается не в безводной форме, а в виде полуацеталя.
Что важно знать
| Хлорацетальдегид | |
|---|---|
| Общие | |
| Систематическое наименование |
Хлорэтаналь |
| Традиционные названия | хлоруксусный альдегид, 2-хлорацетальдегид, 2-хлор-1-этаналь, монохлорацетальдегид |
| Хим. формула | C2H3ClO |
| Рац. формула | ClCH2CHO |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 78,5 г/моль |
| Плотность | 1,117 г/см³ |
| Энергия ионизации | 10,61 ± 0,01[1] |
| Термические свойства | |
| Температура | |
| • плавления | -16,3 °C |
| • кипения | 85 - 85,5 °C |
| Давление пара | 100 ± 1[1] |
| Классификация | |
| Рег. номер CAS | 107-20-0 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 33 |
| UNII | CF069F5D9C |
| CompTox Dashboard EPA | DTXSID4020292 |
| Рег. номер EINECS | 203-472-8 |
| SMILES | |
| InChI | |
| RTECS | AB2450000 |
| ChEBI | 27871 |
| ChemSpider | 21106502 |
| ECHA InfoCard | 100.003.158 |
Физические свойства
Бесцветная жидкость с резким запахом.
Получение
Хлорацетальдегид был впервые получен из винилхлорида и хлорноватистой кислоты в присутствии закиси ртути[2]. Позднее для получения хлорацетальдегида было применено разложение хлорированных ацеталей щавелевой кислотой, а впоследствии осуществлён синтез из винилхлорида и хлорной воды (получается гидратированный хлорацетальдегид):
Но из-за склонности хлорацетальдегида к быстрой полимеризации данные методы оказались неподходящими для его ни лабораторного, ни промышленного получения.
Затем были разработаны методы синтеза хлорацетальдегида из винилацетата[3] и хлорированием ацетальдегида[4].
Безводный хлорацетальдегид получают из гидрата азеотропной перегонкой с хлороформом, толуолом или тетрахлорметаном.
Применение
Хлорацетальдегид используется в синтезе 2-аминотиазола. Также применяется для облегчения удаления коры с деревьев.
Токсичность
Примечания
Источники
- Р. П. Ластовский, Е. А. Божевольнов, А. В. Бромберг и др. «Методы получения химических реактивов и препаратов». Выпуск 21. — М.: "НИИТЭХИМ", 1970.
- Лазарев Н. В. Вредные вещества в промышленности. том I. — Л.: Химия, 1976. — 592 с.
- Институт промышленной безопасности, охраны труда и социального партнёрства. Хлорацетальдегид (40% раствор)
- Хлорацетальдегид