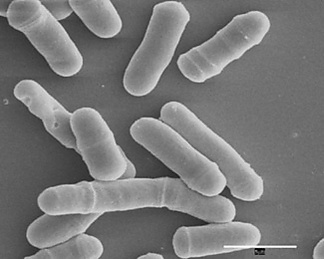
Schizosaccharomyces pombe
Schizosaccharomyces pombe (лат.) — вид дрожжей. Одноклеточный представитель царства грибов, относится к классу Schizosaccharomycetes (делящиеся дрожжи). Клетки имеют палочковидную форму и размеры 3-4 мкм в диаметре и 7-14 мкм в длину. Клетки растут только вдоль своей длинной оси и делятся пополам, сохраняя таким образом свою форму. Используется как модельный организм в молекулярной биологии и цитологии.
Общие сведения
| Schizosaccharomyces pombe | |
|---|---|
| Научная классификация | |
|
Домен: Царство: Подцарство: Отдел: Подотдел: Класс: Схизосахаромицеты (Schizosaccharomycetes O.E.Erikss. & Winka, 1997) Порядок: Schizosaccharomycetales O.E.Erikss. et al., 1993 Род: Вид: Schizosaccharomyces pombe |
|
| Международное научное название | |
| Schizosaccharomyces pombe Lindner, 1893 | |
| Синонимы | |
|
История происхождения
S. pombe были выделены в чистую культуру в 1893 году Линднером из восточноафриканской бузы. Название происходит от слова «пиво» на языке суахили — pombe[2]. Впервые были использованы как модельный организм для изучения клеточного цикла Мердоком Мичизоном в 1950-х. Пол Нерс, Леланд Хартвелл и Тимоти Хант получили в 2001 году Нобелевскую премию по физиологии и медицине за работы по регуляции клеточного цикла, выполненную на S. pombe.
Последовательность нуклеотидов в геноме S. pombe была расшифрована в 2002 году консорциумом во главе с институтом Сенгера. S. pombe стали шестым эукариотическим организмом, геном которого был полностью секвенирован. Это позволило идентифицировать многие гены, гомологичные человеческим, в том числе связанным с болезнями (включая диабет и муковисцидоз). В 2006 году при помощи зелёного флуоресцентного белка как молекулярной метки была установлена внутриклеточная локализация всех белков в S. pombe. На S. pombe также ведётся изучение изменений клеточного цикла, связанных с повреждением ДНК.
Значимые исследования
2007 год Исследования этого года внесли вклад в понимание механизмов репарации ДНК и клеточного деления. Была определена ключевая роль белка Ctp1 в процессе гомологичной рекомбинации[3] и показана функция белка Dss1p в привлечении факторов репарации к местам повреждения ДНК[4]. Кроме того, с помощью электронной микроскопии была детально изучена структура актомиозинового сократительного кольца, ответственного за цитокинез[5].
2009 год Были достигнуты успехи в изучении клеточного старения: разработан новый метод анализа хронологической продолжительности жизни (CLS) и продемонстрировано, что ограничение калорий (глюкозы) её значительно продлевает[6]. Также была установлена роль белкового комплекса TORC1 в контроле вступления клетки в митоз в ответ на питательный стресс[7].
2010 год Знаковым событием стало создание международным консорциумом полногеномной коллекции делеционных мутантов, покрывающей 98,4% всех генов S. pombe. Этот ресурс значительно упростил функциональный анализ генов и позволил провести масштабное сравнение с пекарскими дрожжами, выявив, что у S. pombe больше жизненно важных генов[8].
2011 год В журнале Science была опубликована работа по сравнительной геномике четырёх видов делящихся дрожжей, которая выявила неожиданное разнообразие в структуре центромер[9]. Другое исследование охарактеризовало белковый комплекс, связывающий репликацию ДНК с наследованием эпигенетических меток (модификаций гистонов)[10]. Также лаборатория Пола Нерса показала, что ширина клетки определяется градиентом концентрации белка Cdc42[11].
2012 год Был проведён полногеномный скрининг, который позволил идентифицировать новые гены, вовлечённые в реакцию клетки на повреждение ДНК[12]. Кроме того, для исследователей были созданы новые молекулярно-генетические инструменты, в том числе система для точного вызова двуцепочечных разрывов ДНК в заданном месте генома[13] и система для быстрого контроля экспрессии генов[14].
2013 год Группа под руководством Пола Нерса опубликовала первый для эукариот полногеномный каталог генов, удаление которых нарушает клеточный цикл или форму клетки. Было идентифицировано 513 таких генов, 276 из которых ранее не были связаны с этими функциями[15][16]. Также была выявлена ключевая роль белкового комплекса TORC2 в поддержании целостности генома во время синтеза ДНК[17].
2014 год Анализ штамма с четырьмя хромосомами (вместо обычных трёх) показал, что сборка кинетохора — ключевой структуры для расхождения хромосом — может происходить автономно, независимо от окружающего его гетерохроматина[18]. Другое исследование прояснило, как сигнальный путь ответа на повреждение ДНК способствует репарации, координируя два процесса: обработку концов разрыва и синтез нуклеотидов для его «заделки»[19].
2015 год В журнале Nature Genetics была опубликована знаковая работа по изучению геномного и фенотипического разнообразия вида. Учёные секвенировали геномы 161 природного изолята S. pombe со всего мира, что позволило создать подробную карту генетического разнообразия[20]. Анализ позволил проследить историю глобального распространения вида, которое, по оценкам, началось около 340 года до н.э[21]..
2016 год Масштабный скрининг геномной библиотеки делеций выявил 229 мутантов, чувствительных к ДНК-повреждающим агентам, и открыл новые гены, участвующие в ответе на повреждения, включая гены, связанные с архитектурой хроматина и функционированием микротрубочек[22]. В области биотехнологии был создан рекомбинантный штамм, способный эффективно производить L-молочную кислоту[23].
2017 год С помощью микроскопии сверхвысокого разрешения была картирована наноразмерная архитектура сократительного кольца, показавшая его слоистую организацию[5]. В области изучения старения было продемонстрировано, что в благоприятных условиях у S. pombe отсутствует репликативное старение (потеря способности к делению со временем)[24]. Также был создан практически полный каталог генов, важных для мейоза[25] и разработана первая геном-масштабная метаболическая модель (pomGEM)[26].
2018 год Проведён комплексный анализ активности сайтов начала транскрипции в ответ на различные стрессовые условия, что позволило выявить альтернативные промоторы, активируемые в зависимости от внешних сигналов[27]. Полногеномный скрининг позволил обнаружить 20 новых факторов, необходимых для процесса переключения типа спаривания[28]. Кроме того, количественный анализ протеома в ходе мейоза выявил глобальный сдвиг от анаболических процессов к катаболическим[29].
2019 год Было обнаружено, что ограничение определённых аминокислот (лейцина, лизина или аргинина) продлевает хронологическую продолжительность жизни неделящихся клеток[30]. Другое важное открытие касалось эволюции: у S. pombe была выявлена «асимметричная» система распознавания феромонов. Гибкость одной из пар феромон-рецептор способствует постепенной эволюции и может приводить к репродуктивной изоляции и видообразованию[31].
2020 год В области изучения репарации ДНК была продемонстрирована важная роль гистоновой ацетилтрансферазы KAT5 (Mst1) в привлечении белков репарации к местам повреждений[32] и разработан новый инструмент для визуализации ответа на геномный стресс в реальном времени[33]. Также был проведён транскриптомный анализ, показавший, как изменяется экспрессия генов в ответ на разную концентрацию глюкозы[34].
2021 год Были усовершенствованы методы изучения хронологического старения с использованием секвенирования штрих-кодов для большой библиотеки мутантов, что позволило идентифицировать новые гены, ассоциированные со старением[35][30]. Исследования фосфопротеома в ответ на питательные сигналы и активность комплекса TOR выявили высокую степень консервативности этих метаболических сетей между дрожжами и человеком[36].
2022 год Масштабное исследование транскрипционных факторов привело к открытию нового белкового комплекса, названного «Nattou complex», который регулирует экспрессию генов и их расположение внутри ядра[37]. Были раскрыты молекулярные механизмы действия «эгоистичных генов» семейства wtf, которые обеспечивают собственную передачу потомству, производя одновременно «яд» и «противоядие»[38]. Также было показано, что белок внутренней ядерной мембраны Lem2 координирует деградацию РНК на периферии ядра[39].
2023 год Было подтверждено, что S. pombe обладает необычайно высоким уровнем мейотических кроссоверов, что делает его эукариотическим организмом с самым высоким известным числом обменов участками на хромосому[40]. Исследования показали критическую роль гистонового шаперона HIRA в поддержании долговечности и обратимости состояния покоя (G0), предотвращая быстрый переход клеток в состояние необратимого старения[41]. Также было установлено, что в ответ на репликационный стресс в клетках активируется синтез ДНК в фазе G2, в который вовлечены множественные пути репарации[42].
2024 год Была описана новая функция белка Mis4 (ортолог человеческого NIPBL) в покоящихся клетках (фаза G0). Оказалось, что его работа в этот период является обязательным условием для правильного разделения дочерних ядер во время последующего митоза[43]. Кроме того, споры S. pombe стали использоваться как модель для изучения старения неделящихся клеток; было показано, что их жизнеспособность со временем снижается, особенно под воздействием стресса[44].
Сравнение
С почкующимися дрожжами Saccharomyces cerevisiae:
- Геном S. cerevisiae содержит ~ 5600 открытых рамок считывания, геном Sch. pombe содержит ~ 4800 открытых рамок считывания.
- S. cerevisiae имеет 16 хромосом, Sch. pombe имеет 3 хромосомы.
- S. cerevisiae — обычно диплоид, в то время как клетки Sch. pombe обычно гаплоидные.
- Клетки S. cerevisiae находятся главным образом в состоянии G1 (это значит, что переход G1-S надёжно контролируется), в то время как Sch. pombe находится обычно в состоянии G2 (следовательно, переход G2-M находится под надёжным контролем).
Примечания