ATM (белок)
ATM (англ. аtaxia telangiectasia mutated «мутантный при атаксии-телеангиэктазии белок») — серин/треониновая протеинкиназа, которая рекрутируется и активируется двунитевыми разрывами ДНК. Эта киназа фосфорилирует несколько ключевых белков, которые инициируют остановку клеточного цикла, запускают репарацию ДНК или апоптоз. Некоторые из этих белков, в том числе p53, Сhk2 и вариантный гистон H2AX являются опухолевыми супрессорами. Белок кодируется геном ATM.
Белок и кодирующий его ген назван по имени наследственного заболевания — атаксии-телеангиэктазии[1], вызываемой мутациями в гене ATM.
Что важно знать
Введение
На протяжении клеточного цикла ДНК контролируется на наличие повреждений. Повреждения ДНК возникают в результате ошибок при репликации, воздействия побочных продуктов метаболизма, токсичных препаратов, ионизирующего излучения и других факторов. При наличии повреждений ДНК клеточный цикл останавливается в так называемых контрольных точках. Клеточный цикл имеет две основных контрольных точки, G1/S и G2/M, на которых проверяется целостность генетического материала. ATM играет важную роль в задержке клеточного цикла после возникновения повреждений ДНК, особенно после двунитевых разрывов.[2] ATM вместе с другим белком NBS1 выступают в качестве белков, детектирующих двунитевые разрывы ДНК. Различные посредники, такие как Mre11 и MDC1, обретают пост-трансляционные модификации, которые создаются с помощью белков-детекторов. Эти модифицированные белки-посредники затем усиливают сигнал и передают нижестоящим эффекторам, таким как Сhk2 и p53.
Структура
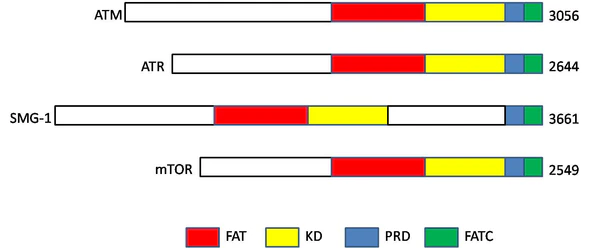
Ген ATM кодирует белок весом 350 кДа, состоящий из 3056 аминокислот.[3] ATM относится к надсемейству фосфатидилинозитоло 3-киназосвязанных киназ (PIKK). Надсемейство PIKK состоит из шести серин/ треониновых протеинкиназ, обладающих сходством с фосфатидилинозитол-3-киназой (PI3K). Этот семейство киназ включает, среди прочих: ATR, ДНК-PKcs (ДНК-зависимая протеинкиназа каталитической субъединицы) и МРМ (целевой рапамицин у млекопитающих). ATM состоит из пяти доменов, расположенных от N-конца к С-концу в следующем порядке: HEAT repeat domain, домен FRAP-ATM-TRRAP (FAT), домен киназы (KD), PIKK-регуляторный домен (PRD) и FAT-C-терминальный (FATC) домен. HEAT repeat непосредственно связывается с С-концом NBS1. Домен FAT взаимодействует с доменом киназы ATM, чтобы стабилизировать С-концевую область самой ATM. Домен KD возобновляет активность киназы, в то время как PRD и домен FATC её регулируют. Хотя ни одна структура для ATM окончательно не ясна, общая форма ATM очень похожа на ДНК-зависимая протеинкиназу ДНК-PKcs и состоит из головки и длинного плеча, для того, как полагают, чтобы обернуть его вокруг двухцепочечной ДНК после конформационного изменения. Весь N-концевой домен вместе с доменом FAT, по прогнозам, принимает вид α-спиральной структуры, которая была найдена с помощью анализа последовательности. Это α-спиральная структура, как полагают, образуют третичную структуру, которая имеет изогнутую трубчатую форму, например, как у белка хантингтин, который также содержит HEAT повторы. FATC является С-концевым доменом с длиной около 30 аминокислот. Он высококонсервативен и состоит из α-спирали с последующим резким поворотом, стабилизированным с помощью дисульфидной связи.[4]
Функция
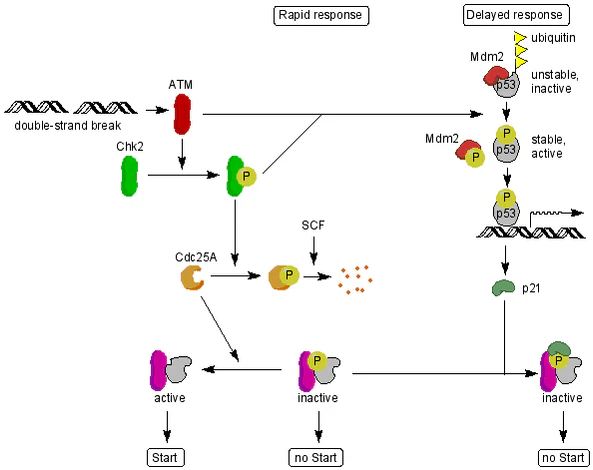
Комплекс из трёх белков Mre11, RAD50 и NBS1 (Xrs2 в дрожжах), у человека называется MRN комплексом, рекрутирует ATM при двунитевых разрывах ДНК и удерживает два конца вместе. ATM непосредственно взаимодействует с субъединицей NBS1 и фосфорилирует вариантный гистон H2AX по серину в 139 положении.[5] Это фосфорилирование генерирует сайт связывания для адаптерных белков, обладающих доменом BRCT . Эти адаптерные белки затем рекрутируют различные факторы, включая эффекторные протеинкиназы Сhk2 и опухолевые супрессоры p53. ATM-опосредованный ответ на повреждение ДНК состоит из быстрой и отсроченной реакции. Эффекторная киназа Chk2 фосфорилируется при помощи ATM и таким образом активируется. Активированная Chk2 фосфорилирует фосфатазу CDC25A, которая в результате не может дефосфорилировать CdK2-циклин, что приводит к остановке клеточного цикла. Если двунитевой разрыв ДНК не был быстро восстановлен, ATM дополнительно фосфорилирует MDM2 и р53 по серину в 115 положении.[6] p53 также фосфорилируется эффекторной киназой Сhk2 . Эти фосфорилирования приводят к стабилизации и активации p53 и последующей транскрипции многочисленных целевых генов p53, включая ингибитор Cdk р21. Это приводит к долгосрочной остановке клеточного цикла или даже апоптозу.[7]
Протеинкиназа АТМ также может быть вовлечена в гомеостаз митохондрий, как регулятор аутофагии митохондрий (митофагия), что приводит к удалению старых дисфункциональных митохондрий.[8]
Регуляция
В норме белок ATM присутствует в клетке в неактивной форме в виде димера, связь в котором между двумя молекулами ATM обеспечена нековалентными взаимодействиями. Первым шагом к активации ATM после появления в клетке двунитевого разрыва ДНК является аутофосфорилирование по сериновому остатку в положении 1981 (Ser1981). Это аутофосфорилирование провоцирует распад димеров ATM на два активных мономера[9]. Для полной активации ATM, помимо двунитевого разрыва ДНК, аутофоcфорилирования по Ser1981 и распада димера, необходим функциональный комплекс MRN и аутофосфорилирование по сериновым остаткам в положениях 367 и 1893 (Ser367 и Ser1893)[2].
Активации ATM с помощью комплекса MRN предшествует по меньшей мере, две стадии; рекрутирование ATM для DSB окончаний в качестве посредника контрольной точки повреждений ДНК — белка 1 (MDC1), который связывается с MRE11, а также последующей стимуляции активности киназы и C-окончания NBS1. Три домена FAT, PRD и FaTC вовлечены в регуляцию активности домена киназы KD. Домен FAT взаимодействует с доменом KD ATM, чтобы стабилизировать С-концевую область самой ATM. Домен FATC имеет решающее значение для активности киназы и очень чувствителен к мутагенезу. Это посредник белок-белковых взаимодействий, например, у гистонацетилтрансферазы Tip60 (HIV-1 Tat белок, взаимодействующий с 60 кДа), который ацетилирует ATM в остатке Lys3016. Ацетилирование происходит в С-концевой половине домена PRD и требуется для активации киназы АТМ и для её расщепления в мономеры. В то время как делеция всего домена PRD отменяет киназную активность ATM, конкретные небольшие делеции не показывают никакого эффекта.[4]
Роль при раке
Атаксия телеангиэктазия (AT) является редким заболеванием, характеризующимся дегенерацией мозжечка, иммунодефицитом, крайней чувствительностью клеток к облучению и предрасположенностью к раку. Пациенты с таким заболеванием имеют мутации в гене ATM, а также в генах, кодирующих белковый комплекс MRN.
Одной из особенностей протеинкиназы ATM является быстрое увеличение киназной активности в ответ на возникновение двунитевого разрыва ДНК[10][11]. Широта фенотипических проявлений атаксии телеангиэктазии обусловлено широким диапазоном субстратов протеинкиназы ATM, среди которых белки, участвующие в репарации ДНК, апоптозе, в регуляции клеточного цикла, генной регуляции, инициации трансляции и обслуживании теломер. Дисфункциональность ATM-киназы может иметь серьёзные последствия в виде неправильной репарации двунитевых разрывов ДНК, результатом чего может быть возникновение проонкогенных мутаций[12].
У больных, имеющих повышенный риск развития рака молочной железы, этот риск был приписан взаимодействию ATM и фосфорилирования BRCA1 и связанных с ним белков после повреждения ДНК.[13] Некоторые виды лейкозов и лимфом, в том числе мантийноклеточной лимфомы, T-ALL, атипичный хронический лимфолейкоз и T-PLL также связаны с дефектами ATM.[14]
Взаимодействия
Выявлено, что протеинкиназа ATM взаимодействует с:
Примечания
Литература
- Giaccia A.J., Kastan M.B. The complexity of p53 modulation: emerging patterns from divergent signals (англ.) // Genes Dev. : journal. — 1998. — Vol. 12, no. 19. — P. 2973—2983. — doi:10.1101/gad.12.19.2973. — PMID 9765199.
- Kastan M.B., Lim D.S. The many substrates and functions of ATM (англ.) // Nature Reviews Molecular Cell Biology : journal. — 2001. — Vol. 1, no. 3. — P. 179—186. — doi:10.1038/35043058. — PMID 11252893.
- Shiloh Y. ATM: from phenotype to functional genomics--and back (англ.) // Ernst Schering Res. Found. Workshop : journal. — 2002. — No. 36. — P. 51—70. — PMID 11859564.
- Redon C., Pilch D., Rogakou E., Sedelnikova O., Newrock K., Bonner W. Histone H2A variants H2AX and H2AZ (англ.) // Current Opinion in Genetics & Development. — Elsevier, 2002. — Vol. 12, no. 2. — P. 162—169. — doi:10.1016/S0959-437X(02)00282-4. — PMID 11893489.
- Tang Y. [ATM and Cancer] (неопр.) // Zhongguo Shi Yan Xue Ye Xue Za Zhi. — 2003. — Т. 10, № 1. — С. 77—80. — PMID 12513844.
- Shiloh Y. ATM and related protein kinases: safeguarding genome integrity (англ.) // Nature Reviews Cancer : journal. — 2003. — Vol. 3, no. 3. — P. 155—168. — doi:10.1038/nrc1011. — PMID 12612651.
- Gumy-Pause F., Wacker P., Sappino A.P. ATM gene and lymphoid malignancies (неопр.) // Leukemia. — 2004. — Т. 18, № 2. — С. 238—242. — doi:10.1038/sj.leu.2403221. — PMID 14628072.
- Kurz E.U., Lees-Miller S.P. DNA damage-induced activation of ATM and ATM-dependent signaling pathways (англ.) // DNA Repair (journal) : journal. — 2005. — Vol. 3, no. 8—9. — P. 889—900. — doi:10.1016/j.dnarep.2004.03.029. — PMID 15279774.
- Abraham R.T. The ATM-related kinase, hSMG-1, bridges genome and RNA surveillance pathways (англ.) // DNA Repair (journal) : journal. — 2005. — Vol. 3, no. 8—9. — P. 919—925. — doi:10.1016/j.dnarep.2004.04.003. — PMID 15279777.
- Lavin M.F., Scott S., Gueven N., Kozlov S., Peng C., Chen P. Functional consequences of sequence alterations in the ATM gene (англ.) // DNA Repair (journal) : journal. — 2005. — Vol. 3, no. 8—9. — P. 1197—1205. — doi:10.1016/j.dnarep.2004.03.011. — PMID 15279808.
- Meulmeester E., Pereg Y., Shiloh Y., Jochemsen A.G. ATM-mediated phosphorylations inhibit Mdmx/Mdm2 stabilization by HAUSP in favor of p53 activation (англ.) // Cell Cycle : journal. — 2006. — Vol. 4, no. 9. — P. 1166—1170. — doi:10.4161/cc.4.9.1981. — PMID 16082221.
- Ahmed M., Rahman N. ATM and breast cancer susceptibility (англ.) // Oncogene (журнал). — 2006. — Vol. 25, no. 43. — P. 5906—5911. — doi:10.1038/sj.onc.1209873. — PMID 16998505.
- Bermudez-Cabrera, H. C., Culbertson, S., Barkal, S., Holmes, B., Shen, M. W., Zhang, S., ... & Sherwood, R.I. Small molecule inhibition of ATM kinase increases CRISPR-Cas9 1-bp insertion frequency (англ.) // Nature communications : journal. — 2021. — Vol. 12, no. 1. — P. 5111. — doi:10.1038/s41467-021-25415-8. — PMID 34433825.
- Kang, H. T., Park, J. T., Choi, K., Kim, Y., Choi, H. J. C., Jung, C. W., ... & Park, S. C. (2017). Chemical screening identifies ATM as a target for alleviating senescence. Nature chemical biology, 13(6), 616-623. PMID 28346404 doi:10.1038/nchembio.2342