Яблочная кислота
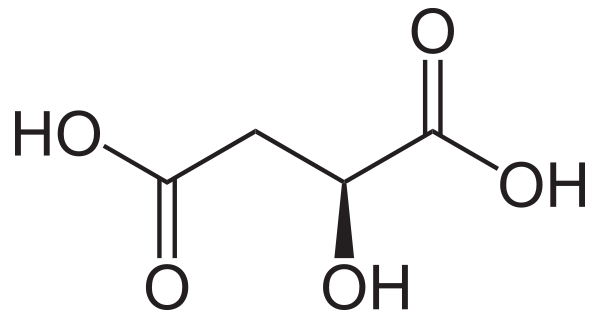
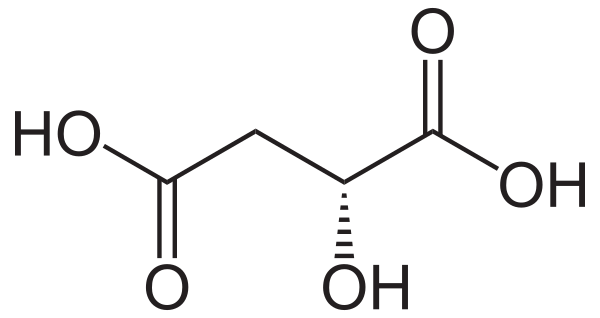
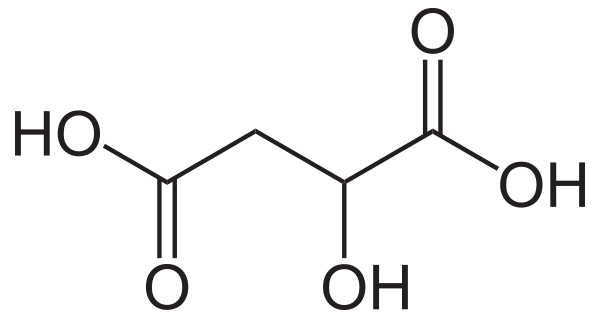
Я́блочная кислота́ (оксиянта́рная кислота́, химическая формула — C4H6O5 или НООС−СН2−СН(ОН)−СООН) — слабая органическая кислота, двухосновная предельная оксикислота. При стандартных условиях — кристаллическое вещество без цвета и запаха.
Соли и сложные эфиры яблочной кислоты называются мала́тами.
Что важно знать
| Яблочная кислота | |
|---|---|
| Общие | |
| Систематическое наименование |
Гидроксибутандио́вая кислота |
| Традиционные названия |
Яблочная кислота, оксиянтарная кислота |
| Хим. формула | C4H6O5 |
| Рац. формула | НООССН2СН(ОН)СООН |
| Физические свойства | |
| Молярная масса | 134,1 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 100 °C |
| Химические свойства | |
| Константа диссоциации кислоты |
3,46; 5,05 |
| Растворимость | |
| • в воде | 144 г/100 мл |
| • в этаноле | 35,9 г/100 мл |
| Классификация | |
| Рег. номер CAS | 6915-15-7 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 525 |
| UNII | 817L1N4CKP |
| CompTox Dashboard EPA | DTXSID0027640 |
| Рег. номер EINECS | 230-022-8 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E296 |
| ChEBI | 6650 |
| ChemSpider | 510 |
| ECHA InfoCard | 100.027.293 |
История
Впервые выделена шведским химиком Карлом Вильгельмом Шееле в 1785 году[1] из сока незрелых яблок.
В 1787 году Антуан Лавуазье предложил для вещества название acide malique, происходящее от латинского слова mālum — названия растений рода «Яблоня»[2][3].
Свойства
Яблочная кислота представляет собой бесцветные гигроскопичные кристаллы, хорошо растворимые в воде, этиловом спирте и диэтиловом эфире.
Существует в двух энантиомерно чистых формах и в виде рацемической смеси.
Нахождение в природе
Яблочная кислота содержится в незрелых яблоках, винограде, рябине, барбарисе, малине, апельсине, мандарине, лимоне[4] и др.
Чтобы вина не производили впечатление кислых, яблочная кислота должна под воздействием бактерий преобразоваться в молочную. Виноделы часто сознательно запускают этот процесс, именуемый яблочно-молочным брожением. Если винодел желает сохранить в вине яблочную кислоту, то такое брожение не проводят, а если оно началось — его останавливают (например, путем понижения температуры в винном погребе).
В растениях махорки и табака содержится в виде химического соединения с никотином. В природе преобладает l-форма яблочной кислоты.
В цитрусовых, выращенных в органическом сельском хозяйстве, содержится больше яблочной кислоты, чем во фруктах, выращенных в традиционном сельском хозяйстве[4].
Роль в метаболизме
Яблочная кислота является промежуточным продуктом цикла трикарбоновых кислот и глиоксилатного цикла. В цикле Кребса l-яблочная кислота образуется путём гидратации фумаровой кислоты и далее окисляется коферментом НАД+ в щавелевоуксусную кислоту.
Применение
Применяется как пищевая добавка (Е296) природного происхождения при приготовлении прохладительных напитков и кондитерских изделий.
Также применяется в медицине.
Примечания
Литература
- Горбов А. И. Яблочная кислота // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Нейланд О. Я. Органическая химия. — М.: Высшая школа, 1990. — 751 с. — 35 000 экз. — ISBN 5-06-001471-1.
- Зефиров Н. С. и др. т. 5 Три—Ятр // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1998. — 783 с. — ISBN 5-85270-310-9.