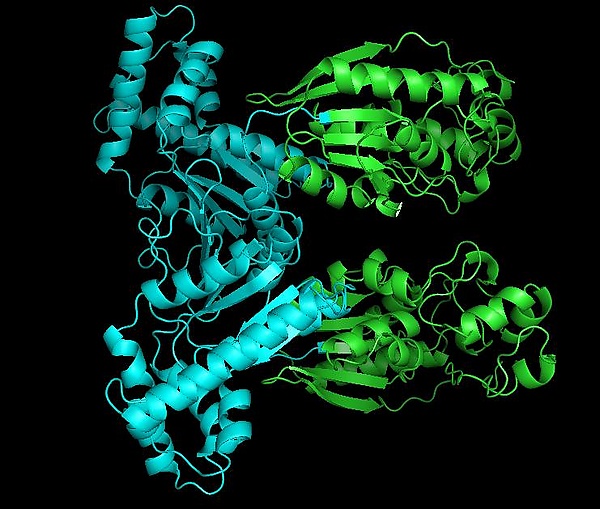
Фосфофруктокиназа-2
Фосфофруктокиназа-2 (ФФК-2) или фруктозо-2,6-бисфосфатаза (ФБФ-2) — бифункциональный фермент, регулирующий процессы гликолиза и глюконеогенеза в теле человека. Этот белок является димером, в котором каждый мономер, в зависимости от внешних условий, может действовать как киназа или фосфатаза. Регулируется глюкагоном и инсулином[1].
Общие сведения
| 6-фосфофрукто-2-киназа | |
|---|---|
| Идентификаторы | |
| Шифр КФ | 2.7.1.105 |
| Номер CAS | 78689-77-7 |
| Базы ферментов | |
| IntEnz | IntEnz view |
| BRENDA | BRENDA entry |
| ExPASy | NiceZyme view |
| MetaCyc | metabolic pathway |
| KEGG | KEGG entry |
| PRIAM | profile |
| PDB structures | RCSB PDB PDBe PDBj PDBsum |
| Gene Ontology | AmiGO • EGO |
| Поиск | |
| PMC | статьи |
| PubMed | статьи |
| NCBI | NCBI proteins |
| CAS | 78689-77-7 |
Структура
Каждый мономер данного белка разделён на два функциональных домена. Киназный домен расположен на N-конце[2]. Он состоит из шести-тяжевого бета-листа, в котором пять параллельных тяжей и один антипараллельный тяж, окружённый шестью альфа-спиралями[3]. Этот домен содержит нуклеотид-связывающую укладку (англ. nucleotide-binding fold) на C-конце первого β-тяжа[4], что объединяет его со структурой аденилаткиназы.
Фосфатазный домен расположен на C-конце[5]. Он схож с белками других семейств, таких как фосфоглицератмутазы и кислые фосфатазы[6] Этот домен имеет смешанную α/β-структуру, в которой присутствует шести-тяжевый центральный β-лист и дополнительный α-спиральный субдомен, предположительно покрывающий активный центр фермента молекулы[3]. Наконец, N-конечный регион модулирует активности фосфофруктокиназы-2 и фруктозо-2,6-бисфосфатазы и стабилизирует димерную форму фермента[6][7].
Механизм действия
Когда уровень глюкозы понижен, в кровь выпускается глюкагон, что активирует сигнальный каскад цАМФ-зависимого пути. В печени протеинкиназа A фосфорилирует Ser-32 этого бифункционального фермента (но этого не происходит в скелетных мышцах), что вызывает понижение киназной активности и стимулирует фосфатазную активность[8]. В результате происходит снижения уровня фруктозо-2,6-бисфосфата, которая в норме стимулирует активность фосфофруктокиназы-1, что и приводит к ослаблению гликолиза и стимуляции глюконеогенеза[9].
Когда концентрация глюкозы растёт, повышается и уровень фруктозо-6-фосфата. Фруктозо-6-фосфат стимулирует фосфопротеинфосфатазу-1, которая дефосфорилирует фосфофруктокиназу-2. В результате происходит активация её киназного домена, который катализирует образование Фр-2,6-Ф. Происходит стимуляция гликолиза и подавление глюконеогенеза.
Регуляция
Аллостерическая регуляция ФФК-2/ФБФ-2 схожа с таковой у ФФК-1[10]. Высокий уровень АМФ или неорганического фосфата означает, что в клетке не хватает энергии: такие условия стимулируют ФФК-2. С другой стороны, высокая концентрация фосфоенолпирувата (ФЕП) и цитрата означает, что в клетке много предшественников для биосинтеза АТФ, что ингибирует ФФК-2. В отличие от ФФК-1, активность ФФК-2 не зависит от концентрации АТФ.
Глюкагон подавляет киназную активность фермента, активируя протеинкиназу А, которая фосфорилирует фермент снижая киназную и стимулируя фосфатазную активность; через протеинкиназу А и ФФК-2/ФБФ-2 глюкагон снижает уровень фруктозо-2,6-бисфостфата, что приводит к подавлению гликолиза. Инсулин активирует обратный процесс, активируя протеинфосфатазу, которая дефосфорилирует ФФК-2/ФБФ-2, снижая её фосфатазную и усиливая киназную активность; в результате растёт концентрация фруктозо-2,6-бисфостфата, что активирует гликолиз.
Изоферменты
На сегодняшний день у млекопитающих обнаружено пять изоферментов, часть из них образуется в результате транскрипции отдельных генов, а часть — в результате альтернативного сплайсинга[11][12][13]. Все изоэнзимы радикально отличаются по своей регуляции: способ регуляции, описанный выше описан для самой изученной печёночной изоформы[3].
К генам человека, кодирующим белки с активностью фосфофруктокиназы-2 относятся:
Значение для медицины
Было показано, что у европейцев мутации в гене Pfkfb2, кодирующем белок ФФК-2/ФБФ-2, связаны с предрасположенностью к шизофрении[14]. Более того, было обнаружено, что регуляция активности ФФК-2 связана с работой сердца и механизмом, не допускающим развития гипоксии[15].
Примечания
Литература
- Д. Нельсон, М. Кокс. Основы биохимии Ленинджера: в 3 т. — М.: БИНОМ, 2014. — Т. 2. — С. 144—146. — 636 с. — ISBN 978-5-94774-366-1.