Полиметилсилоксана полигидрат
Полиметилсилоксана полигидрат (ПМСПГ; торговое наименование — «Энтеросгель») — или гидрогель метилкремниевой кислоты энтеросорбент[2], предназначенный для связывания в желудочно-кишечном тракте и выведения из организма токсических веществ различной природы, возбудителей заболеваний, метаболитов[3][4].
Представляет собой однородную пастообразную массу белого или почти белого цвета, без запаха и без вкуса.
Распространяется, в частности, под торговой маркой «Энтеросгель». Оказывает энтеросорбирующее и дезинтоксикационное действие, применяется при острых и хронических интоксикациях различного генеза.
Что важно знать
| Полиметилсилоксана полигидрат | |
|---|---|
| Состав | |
| Действующее вещество | |
| Гидрогель метилкремниевой кислоты | |
| Классификация | |
| Фармакол. группа | Адсорбирующие кишечные препараты[1] |
| АТХ | A07B |
| Лекарственные формы | |
| Гель для приготовления суспензии, паста для приёма внутрь | |
Общие сведения
Энтеросгель (ПМСПГ) или гидрогель метилкремниевой кислоты — полимерное гелевидное кремнийорганическое соединение[5]. Гель диспергирован в воде до частиц размером не более 300 мкм. Препарат представляет собой суспензию.
На основе электронно-микроскопических исследований установлено, что гелеобразующая матрица имеет глобулярное строение и состоит из ансамбля сросшихся глобул.
Глобулы, связываясь между собой силоксановыми связями, формируют поры.
Поры представляют собой пространства между глобулами. Поры заполнены водой. Размеры пор ограничены[6]. Наличие метильных групп на поверхности обеспечивают его гидрофобные свойства[7]. Частицы Энтеросгеля (ПМСПГ), как правило, образуют непрерывную сеть в суспензии для уменьшения взаимодействия гидрофобных групп SiCH3 с водой.
Эти частицы можно рассматривать как двумерные листы, а не трёхмерные твёрдые частицы.
Водные суспензии полиметилсилоксана полигидрата характеризуются высокой вязкостью[8].
Физико-химические свойства Энтеросгеля (ПМСПГ) определяет его поглотительные и защитные свойства:
- Прочная пористая структура гелеобразующей матрицы определяет поглотительные способности по механизму молекулярной адсорбции и позволяет преимущественно адсорбировать среднемолекулярные токсические вещества и метаболиты (например, билирубин, продукты распада белков)[9][10].
- Благодаря гелевидной консистенции:
- поглощает высокомолекулярные токсические вещества по механизму соосаждения в геле (например, бактериальные токсины)[11];
- проявляет защитные свойства, — эластичные гелевидные частички препарата образуют слой на поверхности слизистых оболочек. Этот слой предохраняет слизистые от воздействия различных повреждающих факторов, его защитные свойства проявляются универсально, — в кишечнике, и на поверхности слизистых других органов[12].
Поглощает токсические вещества, образующиеся в желудочно-кишечном тракте, а также токсические вещества, попавшие в желудочно-кишечный тракт из окружающей среды (например, этиловый спирт)[13]. Также предотвращается обратное всасывание токсических веществ и метаболитов, выделившихся в просвет кишечника из крови, а также поступивших в кишечник с желчью.
В эксперименте in vitro уменьшал продукцию стафилококкового энтеротоксина и ингибировал рост возбудителя Staphylococcus aureus[14].
Снижал образование малонового диальдегида и повышал интегральную антирадикальную активность при токсическом поражении печени в эксперименте in vivo[15].
Благодаря адсорбции в ЖКТ, способствует снижению уровня сахара и гликированного гемоглобина в крови, устранению липидного дистресс-синдрома, включая диабетическую дислипидемию, улучшает энергетические процессы в тканях печени в условиях экспериментального диабета[16].
Энтеросгель (ПМСПГ) прочно связывает и выводит патогенные бактерии[17] и ротавирусы[18][19].
Доказано положительное значение применения Энтеросгеля (ПМСПГ) в качестве основы для мазей при лечении гнойных ран. Применение сорбционного дренажа приводит к снижению нагрузки на лимфатическую систему и удалению фрагментов нежизнеспособных тканей[20].
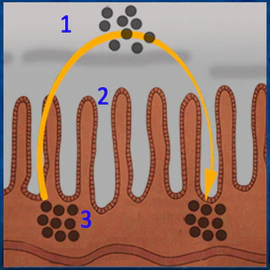
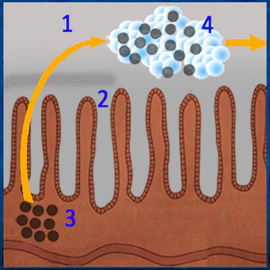
| Пояснения к рисункам 1. просвет кишечника 2. слизитая оболочка кишечника 3. метаболиты и токсические вещества 4. метаболиты и токсические вещества связаны энтеросгелем |
Обладающие повышенной вязкостью частички ПМСПГ покрывают участки слизистой и защищают её от повреждающего действия токсинов бактерий и различных активных химических соединений (напр. деконъюгатов солей жёлчных кислот, которые повреждают слизистую оболочку желудочно-кишечного тракта).
Необходимо отметить выраженную способность Энтеросгеля (ПМСПГ) к поглощению молекул липополисахарида. Крупные молекулы липополисахарида соосаждаются в геле и выводятся [11]. Суточная доза ПМСПГ (Энтеросгель паста) связывает 410 мг ЛПС[21].
Липополисахарид (ЛПС), обладающий чрезвычайно высокой биологической активностью, содержится в наружной стенке всех грамотрицательных бактерий и выделяется только при разрушении бактерии, а поэтому его также называют эндотоксином (приставка эндо- означает внутри-, внутри бактерии). Основным резервуаром грамотрицательной микрофлоры и липополисахарида является дистальный отдел кишечника. В норме в кровоток попадает небольшое количество эндотоксина, так как стенка кишечника выполняет барьерную функцию и ограничивает поступление эндотоксина в кровоток. Большая часть (94 %) поступившего в кровь эндотоксина подвергается детоксикации в печени. Но небольшая часть эндотоксина, минуя печень, попадает в системный кровоток, поддерживая физиологическую концентрацию эндотоксина в крови (физиологическая эндотоксинемия).
Процесс проникновения эндотоксина в кровоток может усиливаться при возникновении различных повреждениях слизистой кишечника и при дисбактериозах, которые сопровождаются транслокацией бактерий и продуктов их жизнедеятельности в тонкую кишку[22], а также в результате индуцированной антибиотиками гибели грамотрицательной микрофлоры и выброса большого количества эндотоксина[23].
Особо необходимо подчеркнуть, что различные стрессовые ситуации (тяжелый приступ стенокардии, ожог, травмы и т. д.) вызывают повреждение слизистой оболочки желудочно-кишечного тракта.
Эти повреждения происходят из-за перераспределения энергетических и структурных ресурсов организма, то есть передачи из систем не участвующих в адаптации к стрессовому фактору, в системы обеспечивающие адаптацию[24].
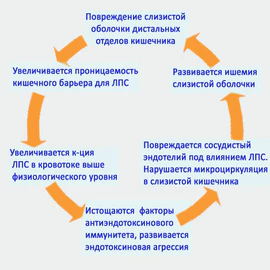
Увеличение концентрации эндотоксина в крови выше физиологической нормы приводит к патологическому состоянию — эндотоксиновой агрессии. Эндотоксиновая агрессия является универсальным фактором патогенеза заболеваний человека, развитие которого обусловлено избыточным поступлением в общий кровоток эндотоксина и недостаточностью эндотоксинсвязывающих систем (Таболин В. А., Яковлев М. Ю.)[25][26][27][28][29][30]. Избыток эндотоксина вызывает повреждение эндотелия[31] в микроциркуляторных сосудах слизистой оболочки кишечника и приводит к развитию ишемии слизистой оболочки. Это, в свою очередь, вызывает дальнейшее повреждение слизистой и ослабления кишечного барьера.
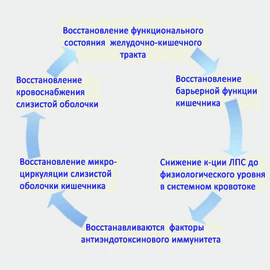
Снижение до физиологического уровня эндотоксина в крови предотвращает повреждение стенки сосудов и восстанавливает нарушенное кровоснабжение слизистой оболочки кишечника, устраняет ишемию слизистой оболочки. Последнее, в свою очередь, способствует её регенерации и восстановление барьерной функции слизистой оболочки кишечника.
Положительный эффект от применения Энтеросгеля (ПМСПГ) направлен в первую очередь на сохранение/восстановление энтерогематического барьера, на восстановление физиологического уровня эндотоксина и на разрыв порочного круга, развитие которого вызвано повреждением слизистой оболочки. Таким образом, развитие эндотоксиновой агрессии не происходит.
| Пояснения к рисункам Слева: В результате недостаточности кишечного барьера происходит увеличение концентрации ЛПС в кровотоке слизистой оболочки, что приводит к нарушению микроциркуляции и ишемии слизистой оболочки, её повреждению и дальнейшему развитию недостаточности кишечного барьера. Развивается эндотоксиновая агрессия.
|
Фармакологическое действие
- Фармакокинетика
Препарат не всасывается в желудочно-кишечном тракте, выводится в неизменённом виде в течение 12 часов[32].
- Фармакодинамика
В просвете желудочно-кишечного тракта препарат связывает и выводит из организма эндогенные и экзогенные токсические вещества различной природы, включая бактерии и бактериальные токсины, антигены, пищевые аллергены, лекарственные препараты и яды, соли тяжёлых металлов, алкоголь.
Препарат сорбирует также некоторые продукты обмена веществ организма, в том числе избыток билирубина, мочевины, холестерина и липидных комплексов, а также метаболиты, ответственные за развитие эндогенного токсикоза[33].
- Основные показания[34]
Эффективность и безопасность применения препарата по зарегистрированным показаниям мониторится в рамках Фармакомнадзора, согласно требованиям Евразийского Союза и Европейского Союза (GVP)[35][36].
Оцениваются результаты клинических рандомизированных исследований, включая двойные слепые плацебо-контролируемые, в России, СНГ, Европе и др. Завершено исследование в Великобритании RELIEVE IBS-D, которое получило множество национальных и международных премий[37] за использование самых передовых технологий[38], и даже вошло в руководство по проведению клинических исследований департамента здравоохранения Англии 2023 (буквально: "...what good research practice looks like (как выглядит хорошая исследовательская практика)"[39].
Энтеросгель включен в клинические рекомендации государственных и негосударственных медицинских организаций специалистов в странах СНГ и Европе[40].
Энтеросгель (ПМСПГ) в соответствии с инструкцией по медицинскому применению используется у взрослых[41], включая беременных и кормящих женщин[42] и детей для лечения[43] и профилактики[44]:
- острых и хронических интоксикаций различного происхождения[45] (например, алкоголь[46], ботулизм[47], грибы[48][49]), включая вирусные[50] и бактериальные[51]. Так, например, в исследовании в Хорватии в качестве дополнительного лечения у женщин, получавших радио- и химиотерапию по поводу онкологических заболеваний органов малого таза, позволил уменьшить симптомы интоксикации (тошноту, рвоту и проч.)[52].
- гипербилирубинемии (вирусные гепатиты[53])[54][55][56], в том числе у новорожденных при гемолитической болезни[57].
- хронической почечной недостаточности (гиперазотемии)[58][59].
- аллергических заболеваний, например, атопического дерматита [60][61].
- гастроэнтерологических заболеваний[62][63]. Так, рекомендован для лечения острой[64][65] и хронической диареи[66], дисбактериоза, дисбиоза[67], включая диареи неинфекционного происхождения[68] и антибиотик-ассоциированные[69][70], в том числе для лечения синдрома раздраженного кишечника с диареей[71], что нашло подтверждение и в фармакоэкономических исследованиях как в России, так и за рубежом, например, в Италии[72].
- в акушерстве[73][74] и гинекологии[75] при острых и хронических инфекционно-воспалительных заболеваниях, поскольку разрешен к применению у беременных женщин[76][77].
- хирургической патологии (также и в экспериментальных целях, за пределами инструкции)[78].
- в дерматологии [79][80][81], при инфекционных болезнях [82] (ВИЧ/СПИД[83]), в кардиологии[84], колопроктологии[85], комбустиологии[86], наркологии[87], неврологии [88], нефрологии [89][90], онкологии[91][92][93], оториноларингологии[94], офтальмологии[95], психиатрии[96], пульмонологии [97][98], радиационной медицине[99], реабилитации[100], реаниматологии[101][102], ревматологии [103], спортивной медицине [104][105], стоматологии [106], урологии [107], фтизиатрии [108], челюстно-лицевой хирургии[109], эндокринологии[110].
- Также используется для выведения тяжелых металлов[111][112][113], инкорпорированных радионуклидов, о чем свидетельствует клинический опыт после Чернобыльской катастрофы[114].
Использование в ветеринарной медицине
Полиметилсилоксана полигидрат (Энтеросгель[115], Энтерозоо[116]) широко используется в ветеринарной медицине[117], что подтверждает фармакологическую эффективность препарата, поскольку в ветеринарии не так явно прослеживаются плацебо и ноцебо эффекты. У животных приблизительно по тем же показаниям, что и в медицине, используется в следующих случаях:
- Подготовка к исследованиям, например УЗИ у котов[118].
- Инфекционные заболевания, например, при парвовирусной инфекции у собак[119], микотоксикозе у кур[120].
- Хроническая почечная недостаточность, например, у котов[121].
- Заболевания гастроэнтерологического тракта, например у телят[122], собак[123].
В промышленном животноводстве:
- Лечение инфекционно-воспалительных заболеваний, например, лечение абомазоэнтерита у телят [124], мастит у коров[125].
- У новорожденных для лечения диареи, например, поросят[126], преодоления критического периода новорожденности у телят[127], у цыплят[128], утят[129].
- Повышение продуктивности, укрепление здоровья животных, например, овец[130].
- Повышение производительности, например, повышения качества спермы у хряков[131].
- Выведение радионуклидов (цезия, стронция) из организма животных[132].
- Профилактика заболеваний и отравлений[133].
В эксперименте показал эффективность в лечении перитонита у крыс[134], язвенной болезни у собак[135].
История
Данный продукт был синтезирован в Украинской ССР в конце 1970-х — начале 1980-х годов И. Б. Слиняковой и И. М. Самодумовой в институте физической химии имени Л. В. Писаржевского[136] (Киев), где с 1960-х годов разрабатывались теоретические основы формирования пористой структуры кремнийорганических адсорбентов с регулируемой пористой структурой и заданной химической природой поверхности, а также проводились работы по синтезу кремнийорганических адсорбентов — пористых полимеров полиорганосилоксанов.
Промышленный выпуск препарата был налажен на Украине на малом предприятии «Креома» в начале 1991 года (рег. свидетельство 94/158/6)[137]. В 1996 году это предприятие было расформировано, а на его технологической базе создано ЗАО «ЭОФ „Креома-Фарм“»[137]. Украинское предприятие организовало в РФ дочернюю компанию — ЗАО «Силма», на котором по лицензии «Креома-Фарм» было запущено производство препарата в России[137]. В апреле 2017 года Кадничанский и Бадаев уступили по 30 % своей доли ЗАО «Силма» О. Жаркову, вице-президенту «Опоры России», который также сменил на посту генерального директора Э. Кадничанского[138].
Препарат производства ЗАО «Силма» был зарегистрирован в качестве лекарственного средства и производился и реализовывался на территории РФ на основании регистрационных свидетельств 94/158/6, Р N001123/01-2002 и Р N001123/02-2003|20|09|2017[139].
Благодаря активной рекламной кампании (в частности, в 2003 году даже был среди 20 наиболее рекламируемых в прессе препаратов на Украине[140]) препарат распространён в ряде стран Dhive-url=https://web.archive.org/web/20220126121320/https://pharmvestnik.ru/content/articles/Kakie-enterosorbenty-polzuutsya-sprosom-u-rossiyan.html%7Carchive-date=2022-01-26%7Caccessdate=%7Cdeadlink=no}}</ref>.
Изучение применения препарата проводилось совместно с медицинской службой Краснознамённого Киевского военного округа (полковник м/с, профессор Ф. Г. Новиков, полковник м/с Н. П. Безлюда)[141].
Препарат зарегистрирован в России и странах СНГ в качестве лекарственного средства[34], а в странах Европейского Союза, Сербии, Новой Зеландии|[142][143] по Классификации Европейской Комиссии— в качестве «медицинского изделия», так как продукт не всасывается в кровь и действует только в желудочно-кишечном тракте в качестве адсорбента[144](англ. medical device class IIa; CE 1023 — Certificate No. 110058 QS/NB)[145].
В 2016 году украинская фирма инициировала патентный спор с ООО «ТНК „Силма“», которое является производителем препарата под этим названием в РФ и поставляет продукцию во многие страны мира[139]. С октября 2006 года (дата подачи заявки в ЕАПО)[146] украинская фирма имеет евразийский патент на способ получения сорбента, действующий на территории Азербайджана, Армении, Белоруссии, Казахстана, Киргизии, Молдавии.
Молдавия денонсировала Евразийскую патентную конвенцию с 26 апреля 2012 года, однако признаёт евразийские патенты, выданные до этой даты[147] Таджикистана и Туркмении[146].
Патент действовал также на территории России, однако 5 мая 2017 года ФИПС признал патент недействительным на территории этой страны[146]. Украинская сторона считала, что препарат «Энтеросгель» производится «Силмой» с нарушением её прав. Ряд судов разных инстанций в РФ, в Казахстане, на Украине и в других странах признал претензии украинской стороны необоснованными[139][148][149][150].
См. также
Примечания
Литература
- Барбова А. И. Сорбция ротавирусов человека и животных энтеросгелем // Микробиологический журнал. — 1995. — Т. 57, № 5. — С. 52—57.
- Волохонский И.А., Самодумова И.М., Слинякова И.Б. Строение пористых полиметилсилоксанов-селективных поглотителей биомолекул из растворов. // Строение и реакционная способность кремнийорганических соединений. — Изд-во Иркутского университета, 1985. — С. 211—212.
- Григорьян А. Ю. и соавт. Проблема лечения ран. Экспериментальное обоснование местного применения препаратов на основе Энтеросгеля. — LAP LAMBERT Academic Publishing GmbH & Co.KG, Deutschland, 2012. — 123 с. — ISBN 978-3-659-13746-4.
- Козинец Г. П. , Боярская А. М., Осадчая О. И. Пасечко Н. В. Энтеросорбция при ожоговой болезни. — К.: Богдана, 2009. — 264 с.
- Николаев В. Г. Энтеросгель. — Богдана, 2010. — 159 с. — ISBN 978-966-425-006-8. Архивная копия от 4 марта 2016 на Wayback Machine
- Слинякова И. Б., Денисова Т. И. Кремнийорганические адсорбенты : получение, свойства, применение, АН УССР, Ин-т физ. химии им. Л. В. Писаржевского. Наук. думка — Киев,1988,страниц 190, isbn = 5-12-000224-2
- Суворова А. Н., Ткаченко Е. И., Успенский Ю. П. Дисбиоз кишечника. Руководство по диагностике и лечению.—3е изд., испр. и доп. — СПб. : ИнформМед, 2013. — 270 с., ил. — С. 230—233. ISBN 978-5-904192-14-3 (2-е издание)
- Shevchenko Y. N., Dushanin B. M., Yashinina N. I. New silicon compounds — porous organosilicon matrics for technology and medicine // Silicon for chemistry industry. — Sandefjord; Norway, 1996 — p. 114—166.
- Григорьев А. В. Желудочно–кишечный тракт как среда обитания бактерий. — СИЛМА, 2004. — 123 с. — ISBN 978-5-98403-006-9.
- Вышегуров Я. Х., Закирова Д. З. и др. Кишечный эндотоксин как облигатный фактор патогенеза эндогенных иридоциклидов и эндофтальмитов неясной этиологии. — ЗАО КДО-тест, Москва, 2006. — 123 с. — ISBN 5-8443-0038-4.
- Збірник наукових праць. Біосорбційні методи і препарати в профілактичній та лікувальній практиці. 1я НПК. — ЛОГОС, Киев, 1997. — 216 с.
- Journal of Colloid and Interface Science — № 308 (Comparative characterization of polymethylsiloxane hydrogel and silylated fumed silica and silica gel). — 2007.
- Меерсон Ф. 3., Пшенникова М. Г. Адаптация к стрессорным ситуациям и физическим нагрузкам. — Медицина, 1988. — 256 с. — ISBN 5-225-00115-7.
- Газенко О.Г., Меерсон Ф. 3., Пшенникова М. Г. Физиология адаптационных процессов. — Наука, 1986. — 636 с. — ISBN нет.
- Скрипкин Ю. К., Бутов Ю. С., Иванов О. Дерматовенерология. Национальное руководство. — ГЭОТАР-Медиа, 2013. — 1024 с. — ISBN 978-5-9704-2305-9.
- Лиходед В. Г., Ющук Н. Д., Яковлев М. Ю. Роль эндотоксина грамотрицательных бактерий в инфекционной и неинфекционной патологии // Архив патологии. — 1996. — № 2. — С. 8—12.
- Яковлев М. Ю. Элементы эндотоксиновой теории физиологии и патологии человека // Физиология человека. — 2003. — № 4. — С. 154—165.
- Таболин В. А. и др. Антифосфолипидный синдром у новорожденных детей от женщин с пороками сердца // Международный журнал иммунологии. — 1999. — № 12. — С. 160—161.
- Таболин В. А., Лазарева С. И., Яковлев М. Ю. Антифосфолипидный синдром: важная роль эндотоксиновой агрессии // Педиатрия. — 2001. — № 5. — С. 80–84.
- Таболин В. А., Яковлев М. Ю. и др. Современные подходы к лечению токсико-септических состояний у новорожденных // Педиатрия. — 2002. — № 1. — С. 31—35.
- Таболин В. А., Бельчик Ю. Ф. и др. Особенности гуморального звена антиэндотоксинового иммунитета у новорожденных и грудных детей с цианотическими врожденными пороками сердца, осложненными инфекционно-воспалительными заболеваниями // Аллергология и иммунология. — 2002. — № 1. — С. 153—158.
- Таболин В. А. и др. Патогенетические механизмы и клинические аспекты действия термостабильного эндотоксина кишечной микрофлоры // Русский медицинский журнал. — 2003. — № 2. — С. 126—128,том 11.
- Яковлев М. Ю., Лиходед В. Г,. Аниховская И. А. и др. Эндотоксининдуцированные повреждения эндотелия // Архив патологии. — 1996. — № 2. — С. 41—45.
- Helmut Brade. Endotoxin in Health and Disease. — Marcel Dekker, New York-Basel, 1999. — 962 с. — ISBN 0824719441.
- Mikhalovsky S., Khajibaev A. Biodefence (NATO Science for Peace and Security Series A Chemistry and Biology), Advanced Matherial and Methods for healths protection. — Springer, Netherlands, 2011. — 375 с. — ISBN 978-94-007-0219-6.