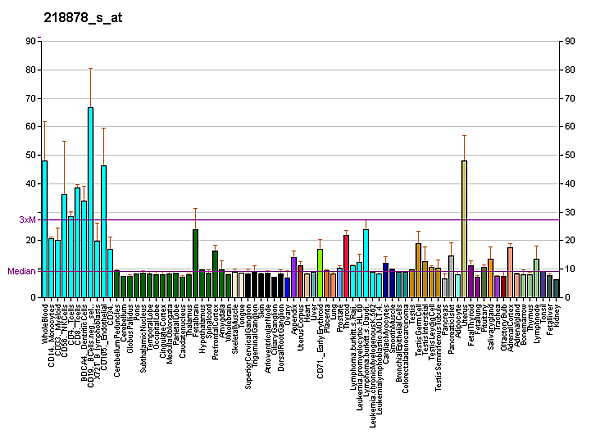
SIRT1
Сиртуин 1, также известный как деацетилаза сиртуин-1 зависимая от НАД, представляет собой белок, который у человека кодируется как геном SIRT1.[5][6]
SIRT1 представляет собой фермент, расположенный преимущественно в клеточном ядре, который деацетилирует факторы транскрипции, влияющие на клеточную регуляцию (реакция на стрессоры, долголетие).[7][8]
Общие сведения
Функции
Сиртуин 1 является членом семейства белков сиртуинов, гомологов гена Sir2 в S. cerevisiae. Представители семейства сиртуинов характеризуются наличием сиртуинового core-домена и делятся на четыре класса. Функции сиртуинов человека ещё не определены, однако известно, что белки сиртуинов дрожжей регулируют эпигенетический сайленсинг генов и подавляют рекомбинацию рДНК. Исследования показывают, что сиртуины человека могут функционировать как внутриклеточные регуляторные белки с активностью моноАДФ-рибозилтрансферазы. Белок, кодируемый этим геном, входит в класс I семейства сиртуинов.[9]
Sirtuin 1 понижен в клетках с высокой резистентностью к инсулину, а индуцирование его экспрессии повышает чувствительность к инсулину, что позволяет предположить, что эта молекула связана с улучшением чувствительности к инсулину.[10] Кроме того, было показано, что SIRT1 деацетилирует и влияет на активность обоих членов комплекса PGC1-alpha/ERR-alpha, которые являются важными метаболическими регулирующими транскрипционными факторами.[11][12][13][14][15][16] Было показано, что у млекопитающих SIRT1 деацетилирует и тем самым деактивирует белок p53.[17] SIRT1 также стимулирует аутофагию, предотвращая ацетилирование белков (через деацетилирование), необходимых для аутофагии, что было продемонстрировано в культивируемых клетках, эмбриональных и неонатальных тканях.[18] Эта функция обеспечивает связь между экспрессией сиртуинов и клеточным ответом на ограничение питательных веществ в результате ограничения калорийности.[19]
SIRT1 играет роль в активации клеток Т-хелперах 17, которые способствуют развитию аутоиммунных заболеваний; попытки активировать SIRT1 терапевтическим путём могут вызвать или усугубить аутоиммунные заболевания.[20] SIRT1, наряду с HDAC1 и промоторным комплексом AP-1 в дофаминергических средних колючих нейронах D1-типа, по-видимому, тесно вовлечён в патогенез зависимости.
SNP (rs10997875) в гене Sirt1 может играть роль в патофизиологии большого депрессивного расстройства. Также было установлено, что существует связь между геном Sirt1 (rs3758391) и депрессивными расстройствами. Кроме того, было показано, что экспрессия Sirt1 в периферической крови людей с депрессией значительно меньше, чем у здоровых людей.[21]
Селективные лигандные вещества
- Ламин А представляет собой белок, который был идентифицирован как прямой активатор сиртуина 1 во время исследования прогерии.[22]
- Утверждается, что ресвератрол является активатором Сиртуина 1[23], но этот эффект оспаривался на основании того факта, что первоначально использованный анализ активности с использованием нефизиологического субстратного пептида может давать искусственные результаты.[24][25] Ресвератрол увеличивает экспрессию SIRT1, что означает, что он увеличивает активность SIRT1, хотя и не обязательно путём прямой активации.[26] Однако позже было показано, что ресвератрол непосредственно активирует сиртуин 1 против немодифицированных пептидных субстратов.[27][28] Ресвератрол также усиливает связывание сиртуина 1 и ламина А.[22] В дополнение к по отношниею к ресвератролу было показано, что ряд других полифенолов растительного происхождения взаимодействует с SIRT1.[29]
- Также утверждалось, что SRT-1720 является активатором[23], но теперь это подвергается сомнению.[30]
- Метиленовый синий[31] за счёт увеличения соотношения НАД+/НАДН.
- Метформин активирует как PRKA, так и SIRT1.[32]
Хотя ни ресвератрол, ни SRT1720 напрямую не активируют SIRT1, ресвератрол и, вероятно, SRT1720 косвенно активируют SIRT1 путём активации AMP-активированной протеинкиназы (AMPK),[33] которая повышает уровень NAD+ (кофактор, необходимый для активности SIRT1).[34][35] Повышение уровня NAD+ является более прямым и надёжным способом активации SIRT1.
Взаимодействия
Было показано, что сиртуин 1 взаимодействует с HEY2,[36] PGC1-альфа,[37] ERR-альфа,[38] и AIRE.[39] Сообщалось, что микроРНК Mir-132 взаимодействует с мРНК сиртуина 1, снижая экспрессию белка. Это было связано с резистентностью к инсулину у тучных людей.[40]
Сообщалось, что человеческий Sirt1 имел 136 прямых взаимодействий в интерактомных исследованиях, связанных с различными процессами.[41]
И SIRT1, и PARP1 имеют примерно одинаковое сродство к NAD+, который необходим обоим ферментам для активности.[42] Но повреждение ДНК может увеличить уровень PARP1 более чем в 100 раз, оставляя мало NAD+ для SIRT1.[42]
Sir2
Sir2 (гомолог которого у млекопитающих известен как SIRT1) был первым найденным геном из семейства генов сиртуинов. Он был обнаружен в почкующихся дрожжах, и с тех пор члены этого высококонсервативного семейства были найдены почти во всех изученных организмах.[43] Предполагается, что сиртуины играют ключевую роль в реакции организма на стрессы (такие как тепло или голодание) и отвечают за продление жизни при ограничении калорий.[44][45]
Трёхбуквенный символ гена дрожжей Sir означает Silent Information Regulator, а цифра 2 указывает на то, что это был второй обнаруженный и охарактеризованный ген SIR.[46][47]
У круглых червей Caenorhabditis elegans Sir-2.1 используется для обозначения продукта гена, наиболее похожего на дрожжевой Sir2 по структуре и активности.[48][49]
Сиртуины действуют в первую очередь за счёт удаления ацетильных групп из остатков лизина в белках в присутствии НАД+; таким образом, они классифицируются как «НАД+-зависимые деацетилазы» и имеют номер ЕС 3.5.1.[50] Они присоединяют ацетильную группу белка к АДФ-рибозному компоненту НАД+ с образованием О-ацетил-АДФ-рибозы. HDAC-активность Sir2 приводит к более плотной упаковке хроматина и снижению транскрипции в локусе целевого гена. Активность сайленсинга Sir2 наиболее заметна в теломерных последовательностях, скрытых локусах MAT (локусы HM) и локусе рибосомной ДНК (rDNA) (RDN1), с которого транскрибируется рибосомная РНК .
Ограниченная сверхэкспрессия гена Sir2 приводит к увеличению продолжительности жизни примерно на 30 %[51], если продолжительность жизни измеряется количеством клеточных делений, которые материнская клетка может пройти до гибели клетки. Соответственно, удаление Sir2 приводит к сокращению продолжительности жизни на 50 %.[51] В частности, сайленсинговая активность Sir2 в комплексе с Sir3 и Sir4 в локусах HM предотвращает одновременную экспрессию обоих факторов спаривания, что может вызывать бесплодие и сокращение продолжительности жизни.[52] Кроме того, активность Sir2 в локусе рДНК коррелирует с уменьшением образования колец рДНК. Сайленсинг хроматина в результате активности Sir2 уменьшает гомологичную рекомбинацию между повторами рДНК, что является процессом, ведущим к образованию колец рДНК. Поскольку считается, что накопление этих колец рДНК является основным способом «старения» дрожжей, то действие Sir2 по предотвращению накопления этих колец рДНК является необходимым фактором продолжительности жизни дрожжей.[52]
Голодание дрожжевых клеток приводит к аналогичному увеличению продолжительности жизни, и действительно, голодание увеличивает доступное количество НАД+ и снижает никотинамид, оба из которых могут увеличить активность Sir2. Кроме того, удаление гена Sir2 устраняет продлевающий жизнь эффект ограничения калорий Эксперименты с нематодой Caenorhabditis elegans и плодовой мухой Drosophila melanogaster[53] подтверждают эти выводы. В 2006 году проводились опыты на мышах.[54]
Однако результаты других исследований ставят под сомнение вышеприведённую интерпретацию. Если измерять продолжительность жизни дрожжевой клетки как количество времени, которое она может прожить на стадии без деления, то глушение гена Sir2 действительно увеличивает продолжительность жизни.[55] Более того, ограничение калорий может существенно продлить репродуктивную продолжительность жизни дрожжей даже в отсутствие Sir2.[56]
Похоже, что в организмах более сложных, чем дрожжи, Sir2 действует путём деацетилирования нескольких других белков, помимо гистонов.
У плодовой мушки Drosophila melanogaster ген Sir2, по-видимому, не является существенным; потеря гена сиртуина имеет очень незначительные последствия. Однако мыши, у которых отсутствовал ген SIRT1 (биологический эквивалент sir2), при рождении были меньше нормы, часто рано умирали или становились бесплодными.[57]
Ингибирование SIRT1
Старение человека часто характеризуется хроническим вялотекущим уровнем воспаления[58], а провоспалительный транскрипционный фактор NF-κB является основным регулятором транскрипции генов, связанных с воспалением.[59] SIRT1 ингибирует экспрессию генов, регулируемых NF-κB, путём деацетилирования субъединицы RelA/p65 NF-κB по лизину 310.[60][61] Но NF-κB более сильно ингибирует SIRT1. NF-κB увеличивает уровни микроРНК miR-34a (которая ингибирует синтез никотинамидадениндинуклеотида NAD+) путём связывания с её промоторной областью[62], что приводит к снижению уровня SIRT1.
И фермент SIRT1, и поли-АДФ-рибозополимераза 1 (PARP1) требуют NAD+ для активации.[63] PARP1 является ферментом репарации ДНК, поэтому в условиях сильного повреждения ДНК уровни NAD+ могут быть снижены на 20-30 %, тем самым снижая активность SIRT1.[63]
Гомологическая рекомбинация
Белок SIRT1 активно способствует гомологичной рекомбинации (HR) в клетках человека и, вероятно, способствует рекомбинационной репарации разрывов ДНК.[64] SIRT1-опосредованный HR требует белка WRN.[64] Белок WRN участвует в репарации двухцепочечных разрывов с помощью HR.[65] Белок WRN представляет собой геликазу RecQ и в своей мутированной форме вызывает синдром Вернера, генетическое заболевание у людей, характеризующееся многочисленными признаками преждевременного старения. Эти результаты связывают функцию SIRT1 с HR, процессом репарации ДНК, который, вероятно, необходим для поддержания целостности генома во время старения.[64]
Использованная литература
Ссылки
- Блог Corante Дерека Лоу об исследованиях sir2 и SIRT1.