Синдром Кагами — Огата
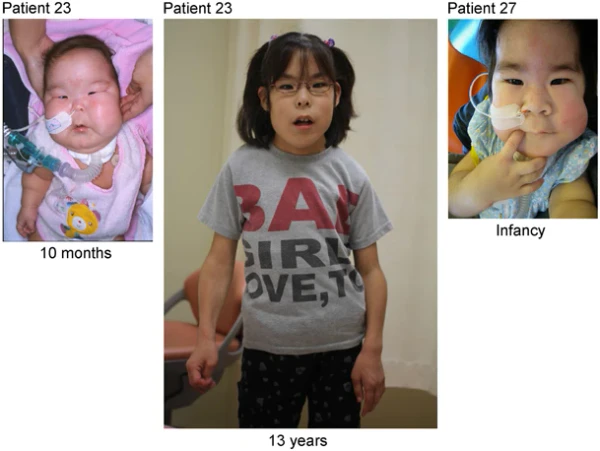
Синдром Кагами — Огата — это редкое генетическое заболевание, вызываемое мутациями в материнской 14 хромосоме или отцовской однородительской дисомией по 14 хромосоме (upd(14)pat)[1]. Его клиническая картина включает комплекс характерных признаков: узкую колоколообразную грудную клетку, укороченные рёбра с крючкообразной деформацией (по типу «вешалки для одежды»), а также дефекты передней брюшной стенки. К пренатальным маркерам относятся многоводие и увеличенная плацента[2]. Кроме того, у пациентов наблюдается специфический лицевой дисморфизм, такой как выступающий лоб, гирсутизм в лобной области, вогнутая переносица, микрогнатия и/или ретрогнатия, полные щёки, крыловидная складка на шее и выступающий фильтрум[3].
История
Впервые синдром был описан Вангом и его коллегами в 1991 году в ходе исследования, связанного с идентификацией отцовской однородительской дисомии хромосомы 14 (upd(14)pat), однако своё название он получил благодаря Масаё Кагами и Цутому Огата, которые подробно описали этот синдром[4].
Этиология
Существует три основных причины, которые могут вызывать данный синдром:
- Отцовская однородительская дисомия 14-й хромосомы (upd(14)pat) встречается в 55-70 % случаев синдрома. Обычно это возникает из-за нерасхождения хромосом во время мейоза в ооците, что приводит к его нуллисомии по 14-й хромосоме. При оплодотворении такого ооцита нормальным сперматозоидом образуется зигота с моносомией по 14-й хромосоме. Поскольку аутосомная моносомия нежизнеспособна, для восстановления диплоидного набора запускается механизм компенсации — оставшаяся одиночная хромосома дублируется. В результате возникает однородительская дисомия, при которой обе хромосомы унаследованы от отца. Это приводит к нарушению импринтинга и проблемам с экспрессией генов
- Эпимутация (гиперметилирование) на 14-й материнской хромосоме встречается в 10-20 % случаев. Эпимутация влияет не на ДНК, а на экспрессию генов посредством химических взаимодействий. В этом случае гены на 14-й материнской хромосоме метилируются и впоследствии деактивируются.
- Делеция 14q32.2 материнской хромосомы 14 встречается в 10-20 % случаев
Гены, мутация которых может привести к заболеванию, расположены в локусе 14q32.2. Это следующие гены: MEG3, RTL1, MEG8[5].
Патогенез
Основным патогенетическим механизмом синдрома Кагами-Огата является повышенная экспрессия гена RTL1. Это происходит из-за отсутствия функционального антисмыслового транскрипта RTL1as (RTL1 antisense) материнского происхождения, который в норме действует как транс-действующий репрессор экспрессии смыслового гена RTL1. В норме материнский аллель в локусе 14q32.2 содержит неметилированную межгенную дифференциально метилированную область MEG3/DLK1:IG-DMR и неметилированный MEG3:TSS-DMR. Это обеспечивает экспрессию RTL1as с материнского аллеля, который, в свою очередь, подавляет экспрессию отцовского аллеля RTL1[6].
К нарушению этого механизма приводят несколько типов генетических и эпигенетических аномалий:
1. Отцовская однородительская дисомия 14 (upd(14)pat)
При upd(14)pat эмбрион наследует две копии хромосомы 14 от отца и ни одной — от матери. Следовательно, в его геноме полностью отсутствует материнский аллель с неметилированными DMR-областями и функциональным RTL1as, что приводит к нерегулируемой сверхэкспрессии RTL1. Пожилой возраст матери является фактором риска возникновения моносомии, которая затем компенсируется до upd(14)pat.
2. Эпимутация (гиперметилирование)
Гиперметилирование обычно неметилированных материнских MEG3/DLK1:IG-DMR и MEG3:TSS-DMR приводит к эпигенетическому сайленсингу этих регионов. Это нарушает транскрипцию RTL1as и, как следствие, вызывает сверхэкспрессию RTL1.
3. Делеции материнского аллеля, затрагивающие MEG3/DLK1:IG-DMR и/или MEG3:TSS-DMR, приводят к отсутствию функционального RTL1as и, как результат, к сверхэкспрессии RTL1.
4. Делеции, затрагивающие только локус RTL1as на материнской хромосоме, приводят к прямой потере его экспрессии и, как следствие, к сверхэкспрессии RTL1 без изменения паттерна метилирования соседних DMR.
5. Транслокации, нарушающие целостность региона между промотором MEG3 и геном RTL1as, подавляют транскрипцию последнего, что в конечном итоге также ведёт к сверхэкспрессии RTL1[6].
Эпидемиология
Распространённость этого заболевания составляет менее 1 случая на 1 000 000 человек[7].
Диагностика
При проведении УЗИ с 25-й недели гестации характерными признаками являются многоводие и увеличение плаценты. Аномалии развития грудной клетки и передней брюшной стенки визуализируются примерно у 40 % плодов[6].
Существует ряд признаков, на основе которых можно предположить наличие синдрома Кагами — Огата. Специфическими признаками являются узкая колоколообразная грудная клетка укороченные рёбра с крючкообразной деформацией (по типу «вешалки для одежды»), полные щёки и выступающая надбровная дуга. Для синдрома также характерны:
- задержка в развитии
- умственная отсталость
- проблемы с кормлением из-за дисфагии
- дефекты брюшной стенки (омфалоцеле и диастаз прямых мышц живота)
- контрактуры суставов
- кифосколиоз
- вальгусная деформация тазобедренного сустава
- ларингомаляция
- аномалии сердечно-сосудистой системы
- гепатобластома
- выступающий лоб, гирсутизм в лобной области, вогнутая переносица, микрогнатия и/или ретрогнатия, полные щёки, крыловидная складка на шее и выступающий фильтрум[3][6]
Молекулярно-генетическое тестирование — подтверждает недостаточную экспрессию антисмыслового транскрипта RTL1as материнского происхождения[6].
Рентгенография грудной клетки — измеряют угол рёбер (среднее значение углов между центром шестого рёбра сзади и горизонтальной осью с обеих сторон). Если угол больше 25°, следует заподозрить синдром Кагами-Огата[8].
Дифференциальная диагностика
- Синдром Беквита — Видемана;
- Синдром Жена;
- Синдром Симпсона — Голаби — Бемеля, тип 1[6].
Осложнения
Лечение
Заболевание неизлечимо. Лечение носит только симптоматический характер[6].
Прогноз
Прогноз при таком синдроме неблагоприятный, так как около 30 % пациентов умирают вскоре после рождения или в течение 1 года жизни[9].