Анаммокс
Анаммо́кс (сокр. от англ. anaerobic ammonium oxidation — анаэробное окисление аммония) — один из ключевых микробных процессов в круговороте азота[1]. Бактерии, осуществляющие этот процесс, были открыты в 1999 году, и в своё время описание этого процесса стало большим сюрпризом для научного сообщества[2]. Уравнение процесса:
- NH4+ + NO2− → N2 + 2H2O.
Этот процесс происходит во многих природных сообществах.
Общая характеристика процесса
В ходе анаммокса нитрит-ион и ион аммония превращаются непосредственно в молекулярный азот[3]:
- NH4+ + NO2− → N2 + 2H2O.
В масштабах планеты этот процесс даёт начало 30—50 % молекулярного азота, образующегося в океанах. В ходе анаммокса утилизируются соединения фиксированного азота в усваиваемой растениями форме и переводятся в неусваиваемую молекулярную форму, поэтому этот процесс ограничивает первичную продуктивность океана[4].
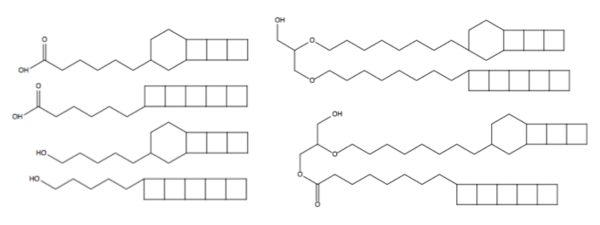
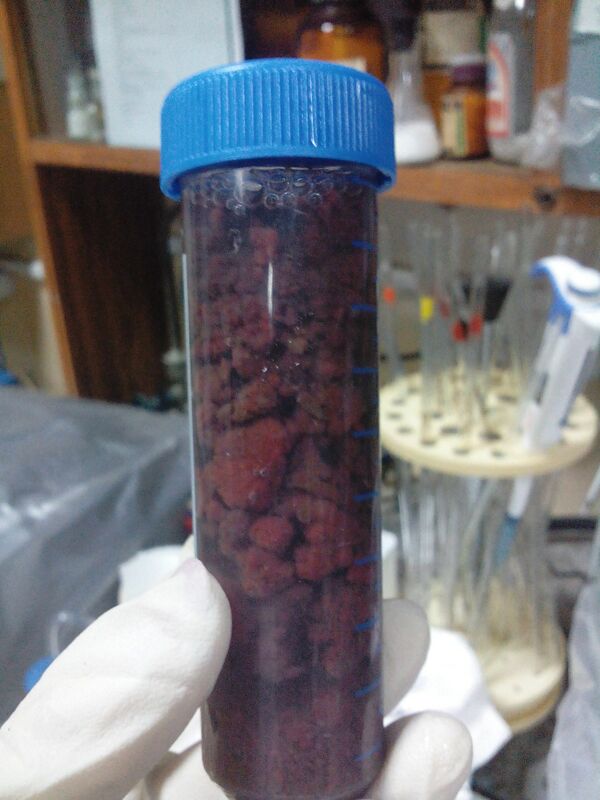
Бактерии, осуществляющие анаммокс, относятся к типу планктомицетов. На данный момент анаммокс описан у представителей 5 родов бактерий: Brocadia, Kuenenia, Anammoxoglobus, Jettenia (все пресноводные виды), а также Scalindua (морские представители)[6]. Для бактерий, осуществляющих анаммокс, характерно несколько отличительных черт: в их клетках всегда содержится единственная аннамоксосома — окружённый мембраной компартмент, в котором и происходит процесс анаммокса. Кроме того, их мембраны содержат особые ладдерановые липиды, обнаруженные лишь у этих организмов[7]. Особый интерес представляет образование гидразина как промежуточного соединения (это вещество используется как ракетное топливо и ядовито для большинства организмов)[8]. Наконец, эти бактерии отличаются поразительно низкой скоростью роста: время удвоения численности составляет 7—22 дней[5]. Они способны осуществлять превращения субстратов анаммокса даже при очень низкой их концентрации (менее микромолярных); иными словами, они отличаются очень высоким сродством к аммонию и нитриту[9][10]. Клетки, осуществляющие анаммокс, содержат очень много белков типа цитохрома с, которые составляют до 30 % всех клеточных белков. К их числу относятся и ферменты, осуществляющие ключевые катаболические реакции анаммокса; они придают клеткам характерный красный цвет[11]. Изначально считалось, что анаммокс происходит только при температурах 20—43 °C[9], однако в недавнее время анаммокс был описан в горячих источниках при температурах 36—52 °C[12] и в гидротермальных источниках вдоль Срединно-Атлантического хребта при температурах 60–85 °C[13].
История
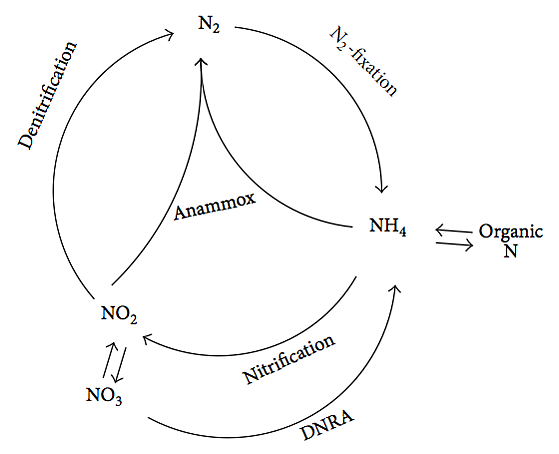
В 1932 году появились сообщения об образовании азота в ходе неизвестного процесса при брожении, которое происходило в иловых отложениях в озере Мендота (штат Висконсин, США)[14]. Более чем через 40 лет назад Ричардс заметил, что большая часть аммония, которая должна была бы образоваться при реминерализации органических остатков, пропадала[15]. Поскольку никаких биологических путей для осуществления таких превращений известно не было, поначалу биологическое анаэробное окисление получило мало внимания[1]. Тридцать лет назад при помощи термодинамических расчётов было предсказано существование двух хемолитоавтотрофных организмов, способных окислять аммиак до азота[16]. Долгое время, впрочем, считали, что биологическое окисление аммиака невозможно, поскольку многие предшествующие попытки найти биологическую основу этих реакций не увенчались успехом. В 1990-х годах наблюдения Арнольда Мадлера (англ. Arnold Mulder) подтвердили заключение Ричардса[17]. Эти учёные наблюдали, что в лишённой кислорода среде, содержащей бактерии, ионы аммония исчезают с видимым образованием азота. Этот процесс получил название анаммокс, и стало понятно, что он имеет огромное значение для разложения невостребованного аммония. Об открытии анаммокса было публично объявлено на Пятом биотехнологическом европейском конгрессе[18]. В середине 1990-х было сообщено об открытии анаммокса в реакторе с кипящим слоем (англ. fluidized bed reactor)[19]. В нём наибольшая скорость анаммокса составила 0,4 кг N/м3/d. Было показано, что для поглощения 1 моля аммония был необходимы 0,6 моля нитрата, в результате чего образовывалось 0,8 моля газообразного N2. В том же году была определена биологическая природа анаммокса[20]. Эксперименты с применением радиоактивных изотопов показали, что при использовании 15NH4+ и 14NO3− доминирующим продуктом был 14-15N2, который составлял 98,2 % всего меченного N2. Стало понятно, что в качестве агента, окисляющего аммиак, в анаммоксе использовался нитрит, а не нитрат. На основании предшествующих исследований Strous и коллеги, используя баланс взаимодействующих масс, рассчитали стехиометрию анаммокса[21], и их результаты получили широкую известность в других группах учёных. Позднее было определено, что бактерии, осуществляющие анаммокс, относятся к типу планктомицетов[2], и первый известный осуществляющий анаммокс организм получил название Candidatus Brocadia anammoxidans[22]. До 2002 года считалось, что анаммокс играет лишь небольшую роль в круговороте азота в природных экосистемах[23]. Однако в 2002 году установили, что анаммокс играет важную роль в биологическом цикле азота, на его долю приходится от 24 до 67 % общей продукции азота в осадочном слое континентальных шельфов[24]. Из-за этого представление об общем виде круговорота азота в природе несколько изменилось, как показано на рисунке.
Возможный механизм реакции
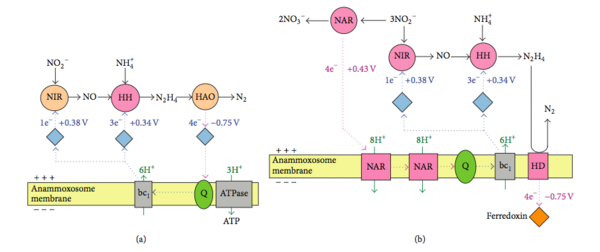
Согласно экспериментам с 15N, проведённым в 1997 году, в ходе анаммокса аммоний биологически окисляется до гидроксиламина, а в качестве возможного акцептора электронов выступает нитрит[25]. Считается, что электронные эквиваленты, необходимые для восстановления нитрита до гидроксиламина, образуются при превращении гидразина в молекулярный азот[26]. Предложено два возможных механизма этих реакций[26]. Согласно первому механизму, мембраносвязанный ферментный комплекс осуществляет превращение аммония и гидроксиламина в гидразин, который в периплазме окисляется до азота. В этот же момент цитоплазматическая сторона того же самого комплекса, который окисляет гидразин, и осуществляет внутренний перенос электронов. Второй механизм утверждает следующее. Аммоний и гидроксиламин превращает в гидразин мембраносвязанный ферментный комплекс, после чего гидразин окисляется до молекулярного азота в периплазматическом пространстве, а высвобожденные электроны через электронтранспортную цепь доставляются в цитоплазму к ферменту, восстанавливающему нитрит до гидроксиламина. Ещё нет ясности относительно того, происходит ли восстановление нитрита и окисление гидроксиламина в разных сайтах одного и того же фермента, или же эти реакции осуществляются двумя различными ферментными системами, соединёнными электронтранспортной цепью[26]. Микроорганизмы редко используют гидразин как промежуточное соединение в метаболизме азота[8]. Возможно, в нитрогеназной реакции именно он является связанным с ферментом промежуточным соединением[27].
Hooper и коллеги предположили, что, возможно, в анаммоксе принимают участие оксид азота NO и нитроксил HNO: NO или HNO конденсируется с аммонием под действием фермента, родственного ферментам семейства аммониймонооксигеназ[28]. Выделяющийся гидразин или имин может впоследствии превратиться в молекулярный азот под действием гидроксиламиноксидазы, а образующиеся восстановительные эквиваленты необходимы для реакции между NO или HNO с аммонием или же для восстановления нитрита до NO. Геномный анализ вида Candidatus Kuenenia stuttgartiensis показал, что у этого организма промежуточным соединением является не гидроксиламмоний, а NO; таким образом, у него имеет место близкий, но слегка отличающийся метаболический механизм[29]. Однако эта гипотеза не противоречит тому, что важным промежуточным соединением анаммокса является гидразин. С гидразином работают два фермента, уникальных для бактерий, осуществляющих анаммокс: гидразингидролаза (hh) и гидразиндегидрогеназа (hd). Hh образует гидразин из нитрита и аммония, а hd переносит электроны с гидразина на ферредоксин. Были определены несколько генов, которые участвуют в биосинтезе жирных кислот и S-аденозилметионина, которые содержат каталитические домены и домены, имеющие электрон-транспортную цепь[29].
Аэрация и добавление органических субстратов (обычно метанола) показало, что две стадии анаммокса, во-первых, являются чрезвычайно энергозатратными процессами, во-вторых, связаны с образованием излишков илистых отложений и, в-третьих, дают начало большим объёмам парниковых газов, таких как СО2, N2O и NO, поглощающий озон. Поскольку анаммокс-бактерии непосредственно превращают аммоний и нитрит в N2 в анаэробных условиях, этот процесс не нуждается в аэрации и добавлении других доноров электронов. Тем не менее, кислород необходим для образования нитрита бактериями, окисляющими аммоний. Однако в системах анаммокса с частичной нитрификацией потребность в кислороде значительно снижена, потому что только половина аммония окисляется до нитрита вместо полного превращения в нитрат[30].
Разнообразие видов
К настоящему моменту описано 10 видов, представители которых могут осуществлять анаммокс, причём семь из них могут быть выращены в лабораторной культуре[5]. Все они пока имеют таксономический статус Candidatus, поскольку ни один из них не удалось получить в чистой культуре. Известные виды распределены по 5 родам: Kuenenia (Kuenenia stuttgartiensis)[29], Brocadia (три вида: B. anammoxidans, B. fulgida и B. sinica)[2][31][32], Anammoxoglobus (A. propionicus)[33], Jettenia (J. asiatica[34][35]) и Scalindua (S. brodae, S. sorokinii, S. wagneri и S. profunda)[36][37][38]. Представители первых четырёх видов были выделены из осадков, покрывающих растения, использующиеся для очищения сточных вод. K. stuttgartiensis, B. anammoxidans, B. fulgida и A. propionicus были выделены из одной и той же посевной культуры. Scalindua населяет преимущественно морские воды, однако встречается также в пресноводных экосистемах и на растениях, очищающих сточные воды[36][39][40][41]. Эти 10 видов, судя по всему, представляют лишь малую долю биоразнообразия видов, осуществляющих анаммокс. Например, в базе данных GenBank в настоящее время содержится более 2000 генов 16S рРНК, выделенных из бактерий, осуществляющих анаммокс. Они принадлежат различным видам, подвидам и штаммам, которые сумели найти свою собственную видовую нишу среди различных сред обитания, населяемых бактериями, проводящими анаммокс. Видовое микроразнообразие особенно выражено у морского рода Scalindua[37][42][43][44][45][46].
Доля совпадения последовательностей 16S рРНК у анаммокс-бактерий составляет от 87 до 99 %, и филогенетические данные заставляют отнести их к филуму Planctomycetes[47], который образует суперфилум PVC вместе с филумами Verrucomicrobia и Chlamydiae[48]. В пределах Planctomycetes анаммокс-бактерии формируют рано отделившуюся монофилетическую кладу. Их филогенетические особенности вместе со специфическими клеточными, физиологическими и молекулярными свойствами заставляют выделить анаммокс-бактерии в порядок Brocadiales[49].
Применение
Анаммокс применяется для удаления аммония из сточных вод при их очистке и включает два раздельных процесса. Первый из них заключается в частичной нитрификации половины аммония до нитрита бактериями, окисляющими аммиак.
- 2NH4+ + 3O2 → 2NO2− + 4H+ + 2H2O
Далее остатки аммония и нитрит в ходе анаммокса, осуществляемого второй группой бактерий, превращаются в нитрат и молекулярный азот (выход около 15 %, не показано):
- NH4+ + NO2− → N2 + 2H2O
Оба процесса могут происходить в одном и том же реакторе, где бактерии двух разных групп формируют компактные гранулы[50][51].
Для получения гранулярной биомассы или биоплёнки из бактерий, осуществляющих анаммокс, необходимы специальные реакторы, причём в оптимальных условиях необходимый объём культуры может быть достигнут за 20 дней. Для выращивания анаммокс-бактерий подходят такие системы, как реактор переменного действия (англ. sequencing batch reactors, SBR), движущийся реактор с кипящим слоем (англ. moving bed reactor) и реакторы типа gas-lift-loop. Первый крупномасштабный реактор, предназначенный для выращивания анаммокс-бактерий, был построен в Нидерландах в 2002 году[52].
Анаммокс — торговое наименование технологии удаления аммиака, основанной на его анаэробном окислении и разработанной Делфтским техническим университетом[53].
Примечания
Литература
- Нетрусов А. И., Котова И. Б. Микробиология. — 4-е изд., перераб. и доп.. — М.: Издательский центр «Академия», 2012. — С. 179. — 384 с. — ISBN 978-5-7695-7979-0.