Список структурных типов
В этой статье перечислены основные структурные типы, характерные для неорганических веществ.
Структурный тип — это категория для классификации кристаллических структур, объединяющая вещества с одинаковой пространственной группой симметрии и одинаковым размещением атомов по эквивалентным позициям (орбитам Уайкоффа), независимо от конкретных химических элементов и абсолютных межатомных расстояний[1].
Классификация и номенклатура
В кристаллографии и химии твёрдого тела не существует единой номенклатуры ИЮПАК для обозначения структурных типов. 1 января 2026 года официально стартовал проект ИЮПАК (2025-014-2-800) по пересмотру «Красной книги», который, в частности, охватит номенклатуру протяжённых структур[2].
Для описания и именования кристаллических структур используются несколько взаимодополняющих систем:
- Название по прототипу — структурному типу присваивается название вещества-представителя, для которого эта структура была впервые подробно описана (например, тип каменной соли, флюорита или перовскита).
- Система Штруктурберихт (нем. Strukturbericht) — обозначение, состоящее из буквы, указывающей на стехиометрию, и порядкового номера. Согласно рекомендациям ИЮПАК 2005 года, использование этой системы считается неприемлемым (устаревшим), вместо неё рекомендуется применять символы Пирсона.
- Символ Пирсона — краткое обозначение, описывающее решётку Браве и количество атомов в элементарной ячейке. Символ формируется из трёх частей: строчная буква обозначает сингонию, заглавная буква — тип центрировки решётки Браве, а число указывает общее количество атомов в элементарной ячейке.
- Пространственная группа — наиболее полное описание симметрии кристаллической решётки.
Простые вещества
| Название | Обозначение | Вид | Символ Пирсона | Пр. гр. | Описание | КЧ | Примеры |
|---|---|---|---|---|---|---|---|
| Cu (ГЦК) | A1 | 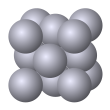
|
cF4 | Fm3m (225) | Кубическая гранецентрированная структура Браве (трёхслойная плотнейшая упаковка) | 12 | Cu, Al, Ni, Pd, Ag, Pt, Au, Pb |
| α-Fe (ОЦК) | A2 | 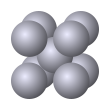
|
cI2 | Im3m (229) | Кубическая объёмноцентрированная структура Браве | 8 | Fe, Na, K, V, Cr, Nb, Mo, Ba |
| Mg (ГПУ) | A3 | 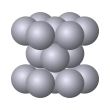
|
hP2 | P63/mmc (194) | Гексагональная (двухслойная) плотнейшая упаковка | 12 | Mg, Be, Te, Co, Zn, Y, Re, Os, C (лонсдейлит) |
| α-La | A3' | 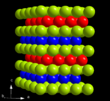
|
hP4 | P63/mmc (194) | Четырёхслойная плотнейшая упаковка | 12 | La, Pr, Nd, Pm |
| Алмаз | A4 | cF8 | Fd3m (227) | Ажурная структура из четырёхкоординированных атомов | 4 | C (алмаз), Si, Ge, α-Sn | |
| β-Sn | A5 | tI8 | I41/amd (141) | Искажённая A4 | 4+2 | β-Sn | |
| In | A6 | 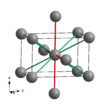
|
tI2 | I4/mmm (141) | Искажённая A2 | 8 | In, Pa |
| α-As | A7 | 
|
hR2 | R-3m (166) | Гофрированные слои | 3 | α-As, Sb, Bi, C (ромбоэдрический β-графит), β-O2 |
| γ-Se | A8 | hP3 | P3121 (152) | Цепочечная | 2 | γ-Se, Te | |
| Графит | A9 | 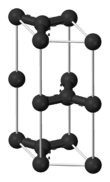
|
hP4 | P63/mmc (194) | Слоистая | 3 | C (графит) |
| α-Hg | A10 | hP1 | R-3m (166) | Искажённая A1 | 6+6 | α-Hg, близка β-Po (Ai) | |
| α-Ga | A11 | 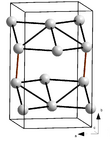
|
oC8 | Cmca (64) | 3+3+3 | α-Ga, формально I2, Cl2, Br2 (А14) и P (чёрный) (A17) | |
| α-S | A16 | oF128 | Fddd (70) | Из молекул S8 | 2 | α-S | |
| α-Po | Ah | 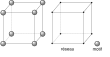
|
cP1 | Pm3m (221) | Кубическая примитивная структура Браве | 6 | α-Po |
| Двумерный аллотроп углерода | — | — | — | — | Двумерный кристаллический лист, сочетающий гексагональные, 4-, 6- и 8-членные кольца[3] | — | C |
| Циклоуглерод C48 | — | — | — | — | Молекулярное кольцо из 48 атомов с чередующимися одинарными и тройными связями[4] | 2 | C |
Бинарные соединения
| Название | Обозначение | Символ Пирсона | Пр. гр. | Описание | КЧ(A) | КЧ(B) | Примеры |
|---|---|---|---|---|---|---|---|
| NaCl | B1 | cF8 | Fm3m (225) | ГЦК (Гранецентрированная кубическая структура) упаковка B, A заполняют все октаэдрические пустоты | 6 | 6 | NaCl, KBr, LiF, ZrO, MgO, BaS, PbS, UC |
| CsCl | B2 | cP2 | Pm3m (221) | Простая кубическая упаковка B, A заполняют все пустоты | 8 | 8 | CsCl, CsBr, CsI, RbCl, AlCo, AgZn, BeCu, RuAl |
| Сфалерит | B3 | cF8 | F-43m (216) | ГЦК упаковка B, A заполняют 1/2 тетраэдрических пустот | 4 | 4 | ZnS (сфалерит), AgI, AlP, BAs, CdS, CuF, GaAs, SiC |
| Вюрцит | B4 | hP4 | P63mc (186) | ГП упаковка B, A заполняют 1/2 тетраэдрических пустот | 4 | 4 | ZnS (вюрцит), ZnO, SiC, AlN, CdSe |
| NiAs | B81 | hP4 | P63mmc (194) | ГП упаковка B, A заполняют все октаэдрические пустоты | 6 | 6 | NiAs, CoTe, CrSe, FeS, NiSn, PtB, VP, ZrTe |
| HgS | B9 | hP6 | P3221 (154) | Искажённая производная от B1, атомы образуют бесконечные спиральные цепи[5] | 2 | 2 | HgS, HgO |
| PbO | B10 | tP4 | P4/nmm (129) | Слоистая структура, атомы свинца в вершинах квадратной пирамиды[6] | 4 | 4 | PbO, BiIn, FeSe, FeS, SnO |
| γ-CuTi | B11 | tP4 | P4/nmm (129) | 9 | 9 | γ-CuTi, AuCu, AlRe | |
| BN | B12 | hP4 | P63mmc (194) | Слоистая графитоподобная структура | 3 | 3 | BN |
| NiS | B13 | hR6 | R3m (160) | Группы из трёх полуоктаэдров формируют пустотелые каналы тригонального сечения[7] | 8 | 8 | NiS, β-FeS |
| GeS | B16 | oP8 | Pnma (62) | Слоистая, искажённая B1 | 3 | 3 | GeS, GeSe, SnS, SnSe |
| CuS | B18 | hP12 | P63mmc (194) | 4 | 4 | CuS, CuSe | |
| AuCd | B19 | oP4 | Pmma (51) | 10 | 12 | AuCd, AuTi, CdMg, IrMo, IrW, MoRh, NbRh, PdTi |
Для бинарных соединений типа AB2 выделяют два основных структурных типа: флюорит и рутил[8][9].
| Название | Сингония | Описание | КЧ(A) | КЧ(B) |
|---|---|---|---|---|
| Структурный тип флюорита (CaF2) | Кубическая | Катионы образуют гранецентрированную решётку[8] | 8 | 4[8] |
| Структурный тип рутила (TiO2) | Тетрагональная[9] | Структура состоит из цепочек октаэдров[10] | 6 | 3[11] |
| Структурный тип кристобалита (SiO2) | Кубическая (β), тетрагональная (α)[12][13] | Высокотемпературная кубическая форма (β-кристобалит, Fd3m) и низкотемпературная тетрагональная (α-кристобалит, P41212); каркасная структура из тетраэдров SiO4[12][13] | 4[12] | 2[12] |
Тройные и более сложные соединения
Структурный тип перовскита характерен для соединений с общей формулой ABX3. В идеализированной кубической структуре (пространственная группа Pm3m) катионы A располагаются в вершинах куба (координационное число 12), катионы B находятся в центре куба (координационное число 6, октаэдрическое окружение), а анионы X занимают центры граней. При понижении температуры структура часто претерпевает искажения с понижением симметрии.
Структурный тип шпинели характерен для соединений с общей формулой AB2X4, кристаллизующихся в кубической сингонии (пространственная группа Fd3m). Анионы в этой структуре образуют плотную кубическую упаковку, а катионы занимают часть тетраэдрических и октаэдрических пустот. В зависимости от распределения катионов выделяют два основных варианта структуры:
- В нормальной шпинели двухвалентные катионы A занимают тетраэдрические пустоты, а трёхвалентные катионы B — октаэдрические.
- В обращённой шпинели половина катионов B находится в тетраэдрических позициях, тогда как катионы A и оставшаяся половина катионов B делят между собой октаэдрические позиции.