Сульфид железа(II)
Сульфи́д желе́за(II) — сложное неорганическое вещество с химической формулой FeS класса неорганических сульфидов .
Общие сведения
| Сульфид железа(II) | |
|---|---|
| Общие | |
| Систематическое наименование |
Сульфид железа(II) |
| Хим. формула | FeS |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 87,910 г/моль |
| Плотность | 4,84 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1194 °C |
| Классификация | |
| Рег. номер CAS | 1317-37-9 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 14828 |
| UNII | TH5J4TUX6S |
| CompTox Dashboard EPA | DTXSID5061665 |
| Рег. номер EINECS | 215-268-6 |
| SMILES | |
| InChI | |
| ChemSpider | 8466211 |
| ECHA InfoCard | 100.013.881 |
Описание и структура
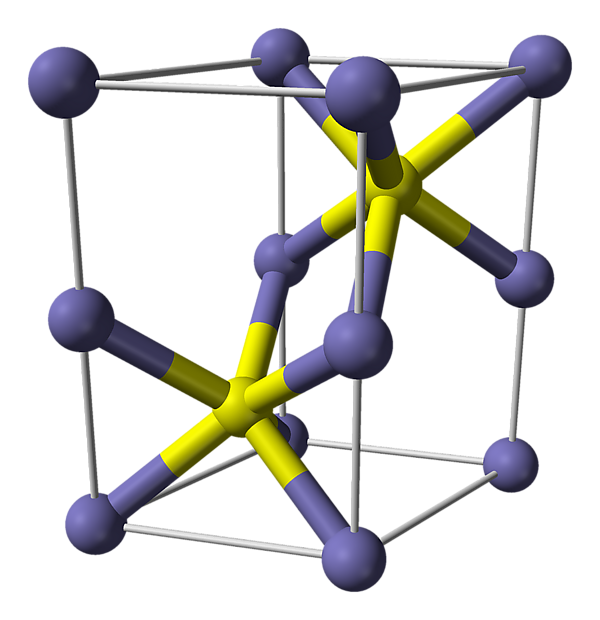
Сульфид железа(II) — бескислородная соль. Кристаллы чёрного цвета с металлическим блеском и гексагональной кристаллической решёткой[1], тугоплавкий, разлагается при нагревании в вакууме. Во влажном состоянии чувствителен к кислороду воздуха. Нерастворим в воде. Не выпадает в осадок при насыщении растворов солей железа(II) сероводородом. Разлагается кислотами. Применяется как сырье в производстве чугуна, твердый источник сероводорода. Не притягивается магнитом[2].
Получение
1. Взаимодействие железа с серой[3]:
Реакция начинается при нагревании смеси железа с серой в пламени горелки, далее может протекать и без подогрева, с выделением теплоты[2].
2. Взаимодействие оксида железа(III) с водородом и сероводородом:
Химические свойства
Применение
Сульфид железа(II) служит обычным исходным продуктом при получении сероводорода в лабораторных условиях. Гидросульфид железа [Fe(SH)2] и/или отвечающая ему основная соль [Fe(SH)OH] является важнейшей составной частью некоторых лечебных грязей.
Примечания
Литература
- Лидин Р. А. «Справочник школьника. Химия» М.: Астрель, 2003.
- Некрасов Б.В. Основы общей химии. — 3-е издание. — Москва: Химия, 1973. — Т. 2. — С. 363. — 688 с.
Ссылки
![]() На РУВИКИ.Медиа есть медиафайлы по теме Сульфид железа(II)
На РУВИКИ.Медиа есть медиафайлы по теме Сульфид железа(II)