ERN1
Сериновая/треониновая протеинкиназа/эндорибонуклеаза Инозитол-требующий фермент 1 α (IRE1α) — это фермент, который у человека кодируется геном ERN1[5][6].
Что важно знать
Функция
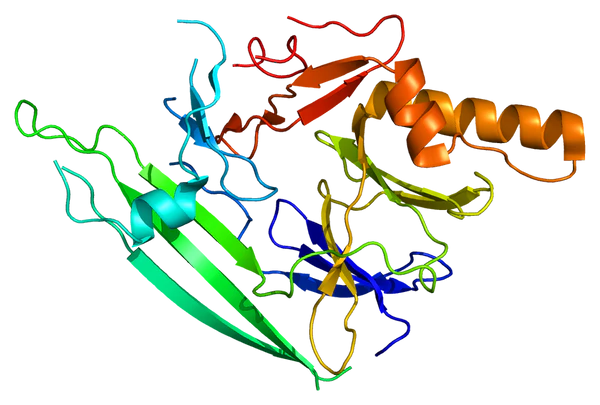
Белок, кодируемый у человека геном ERN1 — это белок, участвующий в каскаде внутриклеточной передачи сигнала от эндоплазматического ретикулума клетки к её ядру. Он является человеческим гомологом белка IRE1 дрожжей. Он обладает встроенной двоякой ферментативной активностью — он является одновременно и сериновой/треониновой протеинкиназой, и эндорибонуклеазой[6].
Одна из основных функций этого белка заключается в изменении экспрессии ряда генов в ответ на стрессовые сигналы, поступающие от эндоплазматического ретикулума (прежде всего — в ответ на накопление в эндоплазматическом ретикулуме несвёрнутых или неправильно свёрнутых белков)[6].
У гена, кодирующего этот белок, обнаружены два альтернативных варианта его сплайсинга, кодирующие две разные изоформы этого белка[6].
Клиническое значение
Поскольку белок IRE1α (он же белок ERN1) является одним из основных сенсоров накопления несвёрнутых или неправильно свёрнутых белков в клетке, а также одним из первых звеньев в каскаде, запускающем генерацию внутриклеточного ответа на накопление в клетке несвёрнутых или неправильно свёрнутых белков, то существуют предположения, что нарушение функции этого белка может играть роль в этиологии и/или в механизмах патогенеза различных нейродегенеративных заболеваний, при которых происходит избыточное накопление в клетке токсичных для неё патологических белков, таких, как бета-амилоид, альфа-синуклеин[7].
В частности, предполагается, что нарушение внутриклеточной передачи сигнала через каскад IRE1α играет роль в патогенезе болезни Альцгеймера[8], болезни Паркинсона[9] и бокового амиотрофического склероза[10][11].
Взаимодействия с другими белками клетки
Белок IRE1α активно взаимодействует с белками теплового шока, в частности, с 90-килодальтонным цитоплазматическим белком Hsp90α (Heat Shock Protein 90 alpha) а также Hsp70 (BiP, он же GRP-78) [12]. При этом взаимодействие с белком Hsp90α стабилизирует белок IRE1α[13]. Когда концентрация несвёрнутых белков не превышена, люминальный домен IRE1 связан с белком-шапероном BiP. Увеличение концентрации несвёрнутых белков может привести к диссоциации комплекса IRE1:BiP вследствие конкуренции за BiP между ними и IRE1 (так как BiP, будучи шапероном, может связываться с несвернутыми белками). После распада комплекса IRE1:BiP молекулы IRE1 олигомеризуются, аутофосфорилируются и становятся активными эндорибонуклеазами, причем для эндорибонуклеазной активности IRE1 должен находиться по крайнем мере в димерной форме.