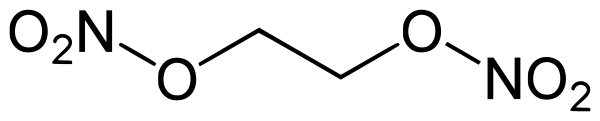
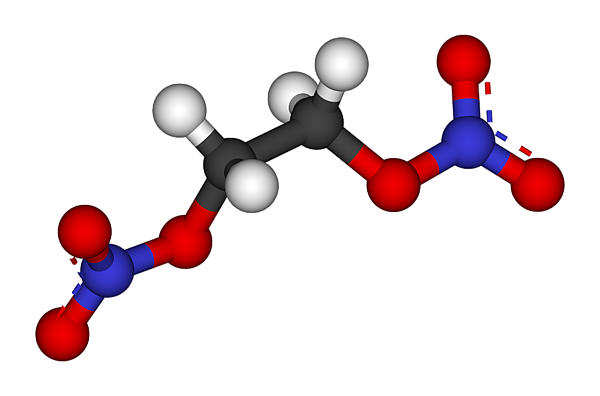
Этиленгликольдинитрат
Этиленгликольдинитра́т (динитроэтиленгликоль, нитрогликоль, сокр. ЭГДН) — органическое соединение с формулой C2H4O6N2 ((CH2ONO2)2), сложный эфир азотной кислоты и двухатомного спирта этиленгликоля, представляет собой маслянистую жидкость. ЭГДН — мощное взрывчатое вещество (ВВ). Изредка встречаются иные наименования: динитрогликоль, гликольдинитрат. Пары весьма токсичны при вдыхании, может проникать через неповреждённую кожу. При попадании в организм вызывает отравления вплоть до летального исхода. Весьма чувствителен к удару, трению, нагреванию. Летуч.
Общие сведения
| Этиленгликольдинитрат | |
|---|---|
| Общие | |
| Систематическое наименование |
1,2-динитроксиэтан |
| Сокращения | ЭГДН, НГЛ |
| Традиционные названия | этиленгликольдинитрат, нитрогликоль |
| Хим. формула | C2H4N2O6 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 152,063 ± 0,0041 г/моль |
| Плотность | 1,49 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | -22,3 °C |
| • кипения | 387 ± 1[1] |
| • разложения | 114 °C |
| • вспышки | 419 ± 0[1] |
| • самовоспламенения | 217 °C |
| Давление пара | 0,05 ± 0,01[1] |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,56 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,4452 |
| Классификация | |
| Рег. номер CAS | 628-96-6 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 40818 |
| UNII | 9CZ6PE9E3J |
| CompTox Dashboard EPA | DTXSID6027264 |
| Рег. номер EINECS | 211-063-0 |
| SMILES | |
| InChI | |
| RTECS | KW5600000 |
| ChemSpider | 37281 |
| ECHA InfoCard | 100.010.058 |
| Безопасность | |
| ЛД50 |
540 мг/кг (мыши, перорально), 460 мг/кг (крысы, перорально), 3800 мг/кг (крысы, подкожно) |
| Токсичность | токсичен, особенно при вдыхании |
| NFPA 704 | |
Физико-химические свойства
Прозрачная маслообразная довольно летучая жидкость. Плотность при 20 °C 1,489 г/см³, температура затвердевания −21,7 °C. Малогигроскопичен, растворим в этаноле, метаноле, диэтиловом эфире, нитробензоле, ацетоне и многих других растворителях. Растворимость в воде 0,5 % при 25 °C. Вязкость при 20 °C — 0,421 сПа·с. Летучесть значительно выше, чем у нитроглицерина (2,2 мг/(см2·ч) — в 20 раз больше (по другим данным — в 8 раз и в 13 раз по Штетбахеру). Легко желатинирует коллоксилин при обычной температуре и сравнительно быстро, в то время как для желатинизации нитроглицерина требуется нагревание. При нагревании со щелочами ЭГДН омыляется. Образует с нитроглицерином эвтектические смеси с очень низкой температурой плавления.
Восприимчивость к нагреванию и внешним воздействиям
t пл. −22.5°С. t кип. 197,5°С. В вакууме ЭГДН кипит без разложения при 95°С и может быть легко перегнан с водяным паром.
Отношение к нагреванию: При осторожном нагревании небольших количеств, ЭГДН можно довести до испарения без взрыва или вспышки. Быстро нагретый на металлической пластинке вспыхивает с лёгким взрывом. Нагретый до 150 °C начинает выделять жёлтые пары — Оксиды азота. При нагревании до 170 °C, в небольших количествах быстро разлагается с лёгкой вспышкой, в больших количествах взрывается.
Химическая стойкость: ЭГДН значительно более стойкий, нежели нитроглицерин. При температуре 72 °C он выдерживает пробу Абеля в течение часа (НГЦ в течение 10-15 мин). Кажущаяся изначально более низкая стойкость ЭГДН объясняется небольшой диссоциацией его паров.
Чувствительность к удару: ~20 см (по другим данным 7-10 см) для груза 2 кг (нитроглицерин — 4 см, ТЭН — 17 см).
Восприимчивость к детонации: ЭГДН намного легче детонирует чем нитроглицерин. Его расширение (при водной забивке), сравнительно с другими гомологичными эфирами в бомбе Трауцля представлено ниже:
| Капсюли с ГР | ЭГДН | Нитроглицерин | Метилнитрат |
|---|---|---|---|
| № 1 (0,3 г.) | 465 мл (71 %) | 190 мл (32 %) | 520 мл (84 %) |
| № 3 (0,54 г.) | |||
| 225 мл (38 %) | |||
| № 6 (1,0 г.) | |||
| 460 мл (78 %) | |||
| № 8 (2,0 г.) | 650 мл (100 %) | 590 мл (100 %) | 620 мл (100 %) |
*В этих опытах не учитывалась разница в действиях самих капсюлей, так как она незначительна.
Из таблицы можно видеть что ЭГДН детонирует значительно легче и полнее даже от самого маленького капсюля. Предположительно это заключается в более низкой вязкости. Высокая скорость детонации возможна при диаметре заряда более 2.7 мм.
Взрывчатые свойства
- Теплота взрыва: 6,8 МДж/кг.
- Теплота образования: −358,2 ккал/кг.
- Энтальпия образования: −381,6 ккал/кг.
- Температура взрыва: 4503 К (примерно 4230 °C).
- Скорость детонации: 7200 м/с. По другим данным 8300 м/c — в стальной трубе диаметром 35 мм. Может детонировать в низкоскоростном режиме (1500—2000 м/с).
- Бризантность: 129 % (61,9 г. песка) от тротила (песочная проба), по Гессу 115 % (18,9 мм) от тротила.
- Фугасность в Pb-блоке: ЭГДН обладает очень высокой работоспособностью: 620 мл при песочной забивке (650 мл при водной).
- Работоспособность в баллистической мортире: 127—137 % от тротила.
- Объём продуктов взрыва: 737 л/кг, (НГЦ 713 л/кг, тол 730 л/кг).
- Критический диаметр: 2 мм, притом детонация низкоскоростная и распространяется не более чем на 100 диаметров (20 см)
Получение
Впервые получен Генри в 1870 году. Основные способы получения:
- этерификация этиленгликоля
- нитрование этилена
Для получения нитрогликоля применяется этиленгликоль марки «динамитный», которого берут 20 весовых частей на 100 весовых частей нитрующей смеси состава 50 % азотной кислоты крепостью 90…98 % и 50 % серной кислоты крепостью 90-98 %.
Нитрация этиленгликоля ведётся на оборудовании и по технологии (температурные и прочие условия) для получения нитроглицерина (см.).
Сепарация нитрогликоля производится так же, как сепарация нитроглицерина с той разницей, что отсепарированный нитрогликоль принимают в ёмкость с 2-х кратным количеством холодной воды, причём вследствие меньшей по сравнению с нитроглицерином вязкости нитрогликоля сепарация проходит быстрее чем у нитроглицерина.
Промывка нитрогликоля производится так же, как и нитроглицерина, с тем отличием, что используют только холодные промывные жидкости вследствие большой летучести нитрогликоля. Промывную жидкость на каждую промывку берут в количестве равном количеству нитрогликоля по объёму. Промытый нитрогликоль фильтруют через фильтр.
Получение нитрогликоля представляет большую опасность. Но меньшую чем производство нитроглицерина.
Применение
Впервые был получен Генри в 1870 году. В 1914 году был применён в Германии в качестве антифриза к динамиту. Во время Второй мировой войны вследствие нехватки глицерина использовался как заменитель нитроглицерина в бездымных порохах. Нитрогликолевые пороха имели малые сроки хранения из-за летучести ЭГДН, однако в условиях военного времени это было оправдано. Пороха на ЭГДН горят приблизительно в 2 раза медленнее чем на нитроглицерине. Применяется в смесях с нитроглицерином в производстве незамерзающих динамитов для применения при низких температурах (обычно в соотношении 50:50).
Взрывчатые вещества (ВВ) с применением этиленглигольдинитрата: GOMA 2 ECO; он также нашёл широкое применение во многих нитроглицериновых (нитрогликолевых) ВВ: желатиндинамитах, гремучем студне, угленитах, детонитах, как добавка в АСВВ и пр.
В январе 2003 года на Раушской набережной около здания ГУП Мосгортранс произошёл теракт с применением этого вещества.
Токсичность ЭГДН
При остром отравлении — головная боль, гипотония, тахикардия, тошнота, рвота. Описаны десятки случаев внезапной смерти сравнительно молодых и здоровых рабочих, длительно соприкасавшихся с ЭГДН и нитроглицерином в производстве взрывчатых веществ. ЭГДН более летуч, чем нитроглицерин, и быстрее всасывается через кожу; считают поэтому, что ему принадлежит главная роль. Гибель обычно наступала через 30—60 ч после прекращения работы (в воскресенье или в понедельник утром) при явлениях стенокардии и острой сердечной недостаточности[2].
У рабочих, занятых изготовлением ЭГДН, был выявлен ряд других неврологических нарушений: бессонница, брадикардия, депрессия, обмороки, не зависящие от сосудистой недостаточности[2]. Существует мнение, что под влиянием действия ЭГДН нарушается синаптическая передача и процессы обмена в головном мозге — в промежуточном его отделе[3].
ЭГДН легко проникает через кожу. Всасывание через кожу способствует развитию отравления ЭГДН у рабочих и даже является его главной причиной. У рабочих, пользовавшихся защитными резиновыми перчатками, находили на коже кистей рук 0,1—1 мг ЭГДН[4]. Минимальная доза, вызывающая боль у человека при нанесении на кожу, 1,8—3,5 мл 1 % спиртового раствора ЭГДН[5]. ПДК в рабочей зоне не установлена, рекомендуется 3 мг/м3[2].
При попадании ЭГДН внутрь с пищей или питьём моментально возникает сильнейшая головная боль, обморочное состояние и через несколько минут смерть от остановки сердца.
Минимальная летальная доза (мЛД) = 0,5 мл при приёме внутрь.
Примечания
Ссылки
- http://chemistry-chemists.com/N2_2013/P1/pirosprawka2012.pdf Архивная копия от 12 июля 2017 на Wayback Machine
- https://exploders.info/articles/0/33.html Архивная копия от 15 октября 2016 на Wayback Machine
- https://exploders.info/books/14.html Архивная копия от 31 июля 2016 на Wayback Machine
- http://chemistry-chemists.com/N6_2011/P16/ChemistryAndChemists_6_2011-P16-5.html Архивная копия от 11 июля 2017 на Wayback Machine
- https://exploders.info/sprawka/90.html Архивная копия от 2 ноября 2016 на Wayback Machine
- http://pirochem.net/index.php?id1=3&category=azgotov-prim-vv&author=shtetbaher-a&book=1936 Архивная копия от 12 июля 2017 на Wayback Machine
- https://exploders.info/books/14.html Архивная копия от 31 июля 2016 на Wayback Machine
- https://exploders.info/books/18.html Архивная копия от 31 июля 2016 на Wayback Machine