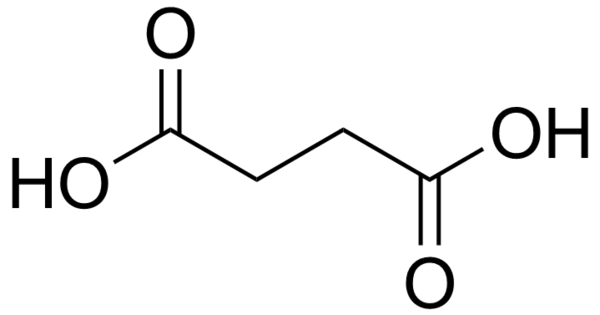
Янтарная кислота
Янта́рная кислота́, бутандиóвая кислота— cлабая органическая кислота, двухосновная карбоновая кислота, химическая формула — C4H6O4 или НООС−СН2−СН2−СООН. При стандартных условиях сухая янтарная кислота — бесцветное кристаллическое вещество без запаха. Соли и эфиры янтарной кислоты называются сукцина́тами (от лат. succinum — «янта́рь»). Янтарную кислоту используют в качестве биологически активной добавки (БАД) в виде препаратов (таблеток, инъекций, ингаляций), в составе косметических средств (масках, скрабах), как биоактиватор для роста растений[2].
Что важно знать
| Янтарная кислота | |
|---|---|
| Общие | |
| Систематическое наименование |
этан-1,2-дикарбоновая кислота |
| Традиционные названия |
Янтарная кислота Бутандиóвая кислота |
| Хим. формула | C4H6O4 |
| Рац. формула | НООС−СН2−СН2−СООН |
| Физические свойства | |
| Молярная масса | 118.09 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 183[1] |
| Классификация | |
| Рег. номер CAS | 110-15-6 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 1110 |
| UNII | AB6MNQ6J6L |
| CompTox Dashboard EPA | DTXSID6023602 |
| Рег. номер EINECS | 203-740-4 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E363 |
| ChEBI | 15741 |
| ChemSpider | 1078 |
| ECHA InfoCard | 100.003.402 |
История
Упоминания о лечебных свойствах янтаря встречаются в трудах Гиппократа в 460—370 г.г. до н.э[3].. Впервые янтарная кислота была получена в XVII веке путём перегонки янтаря. Соли и эфиры янтарной кислоты получили название сукцинаты, происходящее от слова лат. succinum («янтарь»)[2].
Свойства
Янтарная кислота представляет собой бесцветные кристаллы без запаха. Вкус — слабокислый со слегка солоновато-горьким привкусом[4], напоминающим лимонную кислоту. Янтарная кислота, также известна как бутандиовая. Она является слабой органической кислотой. Её химическая формула — C4H6O4 или НООС−СН2−СН2−СООН[2].
Температура плавления 183 °C. Температура кипения 235 °C. Выше 235 °C отщепляет Н2О и переходит в янтарный ангидрид. Янтарная кислота легко возгоняется при 130—140 °С. Растворимость в воде (в 100 г воды): 6,8 г (при 20 °С), 121 г (при 100 °С). Также растворяется в этиловом спирте: 9,9 г (5 °С); в диэтиловом эфире — 1,2 г (15 °С). Нерастворима кислота в бензоле, бензине и хлороформе. Константы диссоциации таковы: Ка1 = 7,4⋅10−5, Ка2 = 4,5⋅10−6[5].
Метиленовые группы янтарной кислоты обладают высокой реакционной способностью, что связано с влиянием карбоксильных групп. При бромировании янтарная кислота даёт дибромянтарную кислоту HOOC−(CHBr)2−COOH. Диэфиры янтарной кислоты конденсируются с кетонами (конденсация Штоббе) и с альдегидами.
С аммиаком и аминами янтарная кислота образует сукцинимид и его N-замещённые аналоги (R−H, алкильная или арильная группа). Моно- и диамиды янтарной кислоты, получаемые с ароматическими и гетероциклическими аминами, применяют для синтеза некоторых красителей, инсектицидов и лекарственных веществ.
Янтарная кислота и её ангидрид легко вступают в реакцию Фриделя — Крафтса с ароматическими соединениями (так называемое сукцинилирование), образуя производные 4-арил-4-кетомасляной кислоты.
Получение
Янтарную кислоту получают при производстве адипиновой кислоты, где она является побочным продуктом[6]. Другой способ промышленного получения — из смеси кислот, образующихся при окислении углеводородов от бутана до декана (алканов С4-С10). Также в промышленности её извлекают из отходов янтаря[7].
Янтарная кислота может быть получена окислением фурфурола пероксидом водорода или в два этапа — гидрирование малеинового ангидрида с последующей гидратацией[7].
В промышленности янтарную кислоту получают главным образом гидрированием малеинового ангидрида.
Где содержится
Биохимическая роль
Янтарная кислота участвует в процессе клеточного дыхания кислорододышащих организмов — в цикле трикарбоновых кислот.
Летальные дозы (LD50): орально — 2,26 г/кг (крысы), внутривенно — 1,4 г/кг (мыши)[8].
Содержится
Янтарная кислота вырабатывается в митохондриях человека, животных, растений и, как и все органические кислоты, сгорая, образует АТФ — энергетического топлива для всех видов синтеза в клетке[3]. Янтарная кислота также содержится в буром угле, природных смолах и янтаре[7].
Применение
Янтарную кислоту используют для получения алкидных смол, сукцинатов, фотоматериалов, красителей и лекарственных веществ[7].
Янтарная кислота используется в аналитической химии, а также в химическом синтезе для получения пластмасс, смол и лекарственных препаратов.
В пищевой промышленности янтарная кислота известна под индексом E363, используется в качестве регулятора кислотности (подкислителя)[4].
Янтарную кислоту используют при выращивании растений для нормализации микрофлоры почвы, стимулирования роста растений. Предпосевная обработка семян увеличивает всхожесть сельскохозяйственных культур и повышает приживаемость рассады. Полив под корень раствором янтарной кислоты растений стимулирует рост корневой системы, опрыскивание — цветение[6]. Приживаемость черенков увеличивается, если перед укоренением их подержать в растворе янтарной кислоты[9]. Янтарная кислота выступает в роли биостимулятора, усиливающего действие удобрений. Её воздействие на растения схоже с влиянием витаминов на организм человека. Выпускается в форме таблеток или порошка и продаётся в специализированных магазинах[10].
Янтарная кислота стимулирует рост цыплят, ускоряет рост бактерий[11].
Некоторые эфиры янтарной кислоты используют в пищевой и парфюмерной промышленности[7]:
- диэтилсукцинат — ароматизатор для пищевых продуктов и парфюмерных композиций, он придаёт запах цветов и обладает свойствами пластификатора;
- моноамиды и диамиды янтарной кислоты с ароматическими и гетероциклическими аминами применяют в производстве красителей и инсектицидов.
Препараты янтарной кислоты в клинической практике в СССР начали использовать с 1972 года. В настоящее время препараты, содержащие сукцинат, применяют в кардиологии, неврологии, эндокринологии, токсикологии, наркологии, педиатрии, восстановительной медицине, хирургии, пульмонологии, гематологии, дерматологии и гинекологии. Широкое использование обусловлено участием сукцината в процессах тканевого дыхания и окислительного фосфорилирования в митохондриях[12]. В лекарственных препаратах янтарная кислота применяется в качестве активного вещества как средство, улучшающее метаболизм. Увеличивает энергообеспечение, уменьшающее гипоксию тканей[13][3]. Янтарная кислота снижает токсическое действие таких лекарственных веществ как барбитураты и анксиолитики[6].
Используется в косметологии в составе кремов для удаления пигментных пятен, очищения пор, снижения жирности кожи и уменьшения воспаления. Инъекции смеси сукцината и гиалуроновой кислоты применяются в омолаживающей процедуре редермализации[14].
Примечания
Литература
- Балуева, Г. А. Кислота из янтаря // Химия и Жизнь : журн. — 1983. — № 11. — С. 58–61.
- Горбов А. И. Янтарная кислота и её гомологи // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Евглевский Алексей Алексеевич, Рыжкова Галина Федоровна, Евглевская Елена Павловна, Ванина Наталья Владимировна, Михайлова Ирина Ивановна, Денисова Алена Владимировна, Ерыженская Надежда Федоровна. Биологическая роль и метаболическая активность янтарной кислоты // Вестник Курской государственной сельскохозяйственной академии. — 2013. — № 9.
- Зацепина Илона Валериевна. БИОМЕТРИЧЕСКИЕ ПОКАЗАТЕЛИ ЗЕЛЕНЫХ ЧЕРЕНКОВ СОРТОВ ГРУШИ, УКОРЕНИВШИХСЯ С ПОМОЩЬЮ РАЗЛИЧНЫХ СТИМУЛЯТОРОВ РОСТА РАСТЕНИЙ // Известия Великолукской государственной сельскохозяйственной академии. — 2022. — № 2 (39).
- Магдесиева Н. Н. Янтарная кислота // Химическая энциклопедия : в 5 т. / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1998. — Т. 5: Триптофан — Ятрохимия. — 783 с. — 10 000 экз. — ISBN 5-85270-310-9.
- Рабинович, В. А. Краткий химический справочник / В. А. Рабинович, З. Я. Хавин. — 2-е изд., испр. и доп. — Л. : Химия, 1978. — С. 201–202, 240. — 392 с. : 114 табл., 19 рис. — 230 000 экз. — УДК 54(031)(G).
- Смирнов А.В., Нестерова О.Б., Голубев Р.В. Янтарная кислота и её применение в медицине. Часть II. Применение янтарной кислоты в медицине // Нефрология. — 2014. — № 4.