Биосинтез гема
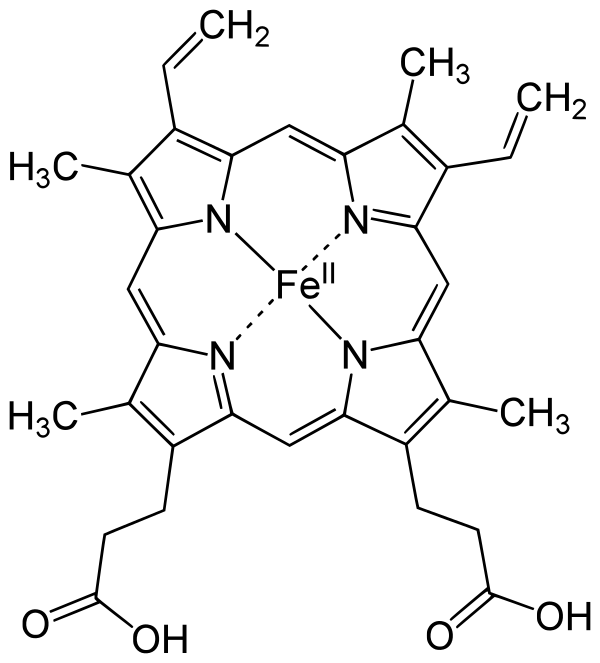
Биосинтез гема — метаболический многоступенчатый процесс образования молекул гема из его предшественников. Гем представляет собой плоский железосодержащий макроциклический комплекс, основу которого составляет четыре пиррольных кольца (тетрапиррол), объединённые между собой метениловыми мостиками (=СH-) и координированные двухвалентным железом (Fe2+). Гем имеет несколько типов, они отличаются как структурно, так и функционально. Но наиболее распространённым типом гема, является — гем Б[1].
Для позвоночных и некоторых видов прокариот (α-протеобактерий) биосинтез гема физиологически важный процесс, так как гем включается в состав многих белков и ферментов (в качестве простетической группы), которые участвуют в газообмене и переносе кислорода (гемоглобин — в эритроцитах и миоглобин — в мышцах), катализе, окислительном фосфорилировании, биотрансформации метаболитов и ксенобиотиков и защите от патогенов (каталаза, пероксидаза, цитохромы, NO-cинтаза, циклооксигеназы, миелопероксидаза и т.д.)[2][3]. Реакции синтеза гема у позвоночных протекает, как в митохондриях, так и цитозоле клеток, у прокариот только в цитозоле. Практически все клетки тела позвоночных, включая и человека (кроме зрелых эритроцитов), способны синтезировать гем, однако, интенсивно этот процесс наблюдается в клетках эритропоэтической ткани красного костного мозга (проэритробластах, эритробластах, ретикулоцитах) и гепатоцитах печени.
Реакции
Синтез гема включает в себя 8 последовательных реакций, протекающие как в митохондриях (1, 6, 7 и 8-я реакции), так и в цитозоле (2, 3, 4 и 5 реакции). Начало и конец синтеза локализованы в одном компартменте — митохондрии, что позволяет эффективнее регулировать данный процесс.
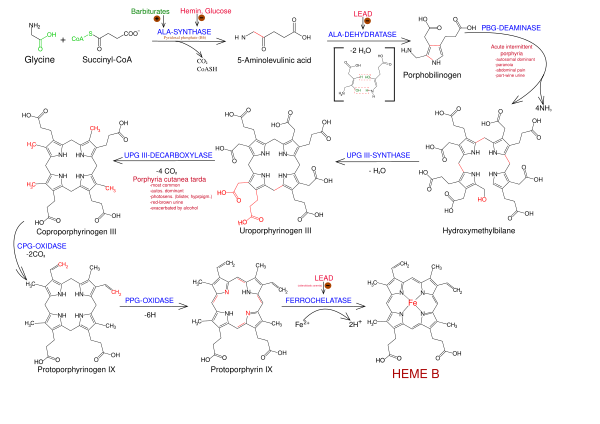
Путь биосинтеза гема Б и его модуляторы. Также показаны основные дефициты ферментов.
Первая реакция в синтезе молекул гема начинается в матриксе митохондрии. Глицин и сукцинил-КоА являются главными предшественниками в образовании гема. Под действием фермента АЛК-синтазы (КФ 2.3.1.37) происходит конденсация глицина с сукцинил-КоА, в результате которой образуется аминолевулинат (АЛК), углекислый газ и кофермент А. Схема реакции:
- сукцинил-КоА + глицин δ-аминолевулиновая кислота + КоА + CO2.
В качестве кофермента используется молекула пиридоксаль-5'-фосфата (PLP).
Данная реакция является ключевой в синтезе гема и протекает достаточно медленно по отношению к последующим (скоростьлимитирующая). Реакция регулируется аллостерически гемом, также он влияет на транскрипцию АЛК-синтазы, прекращая её синтез. Свободные ионы двухвалентного железа (Fe2+) положительно влияют на синтез АЛК-синтазы. Барбитураты усиливают индукцию АЛК-синтазы в гепатоцитах, а гемин и глюкоза аллостерически ингибируют[4]. Образовавшийся в ходе реакции аминолевулинат из матрикса митохондрии поступает в цитозоль.
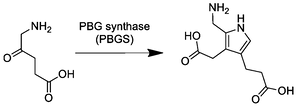
Вторая реакция в процессе синтеза гема характеризуется несимметричной конденсацией двух молекул аминолевулината (АЛК) и одновременно с этим происходящая циклизация, с образованием молекулы порфобилиногена. Реакцию катализирует фермент порфобилиногенсинтаза или АЛК-дегидратаза (КФ 4.2.1.24) по следующему уравнению:
- 2 5-аминолевулинат порфобилиноген + 2 H2O.
Эта реакция является первой общей стадией биосинтеза всех природных тетрапирролов. Фермент в качестве кофактора использует ионы цинка Zn2+, они поддерживают активность.
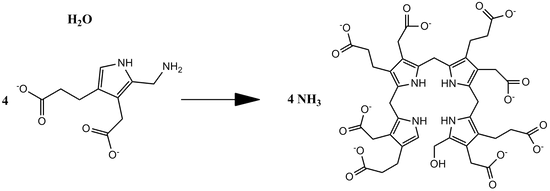
В третьей реакции синтеза гема происходит конденсация четырёх молекул порфобилиногена и одновременно с этим дезаминирование, которые приводят к образованию линейного тетрапиррола — гидроксиметилбилана и аммиака. Фермент, катализирующий данную реакцию — гидроксиметилбилансинтаза или порфобилиноген дезаминаза (КФ 2.5.1.61). Схема реакции:
- 4 порфобилиноген + H2O гидроксиметилбилан + 4 NH3
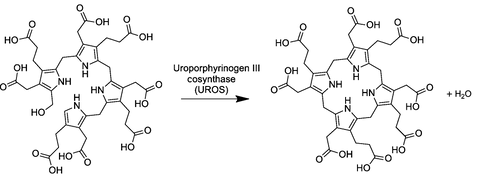
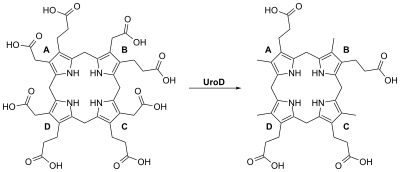
Четвёртая реакция синтеза гема протекает в цитозоле клеток. На этой стадии под действием фермента уропорфириноген III синтазы (КФ 4.2.1.75), линейные молекулы гидроксиметилбилана подвергаются циклизации в уропорфириноген III. При катализе происходит инверсия конечного пиррольного звена (кольцо D) линейной молекулы гидроксиметилбилана, связывая его с первым пиррольным звеном (кольцо А), тем самым образуя крупную макроциклическую структуру, уропорфириноген III[5].
При сниженной активности или дефицита фермента уропорфириноген III синтазы наблюдается образование уропорфириногена I (неферментативно), который обнаруживается в моче и может накапливаться в клетках кожи, где окислятся под действием солнечного света до фототоксичного уропорфирина I. Заболевание, при котором наблюдается дефицит УПГ-III-синтазы называется врождённая эритропоэтическая порфирия или болезнь Гюнтера[6].
В пятой реакции синтеза гема молекулы уропорфириногена III декарбоксилируются с образованием копропорфириногена III. Реакцию катализирует фермент — уропорфириноген III декарбоксилаза (КФ 4.1.1.37). Схема реакции:
- уропорфириноген III копропорфириноген III + 4 CO2.
Реакция протекает в цитозоле, образовавшийся копропорфириноген III далее поступает в матрикс митохондрии, где происходит его дальнейшее преобразование в протопорфириноген IX.
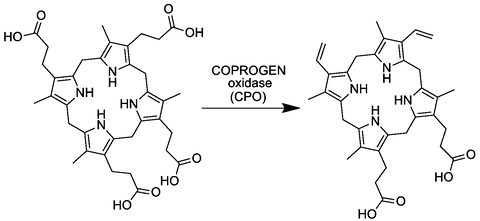
Шестая реакция синтеза гема протекает в матриксе митохондрии. На этой стадии копропорфириноген III поступает из цитозоля в матрикс митохондрии, где происходит его преобразование в протопорфириноген IX, под действием фермента копропорфириноген III оксидазы (КФ 1.3.3.3) Схема реакции:
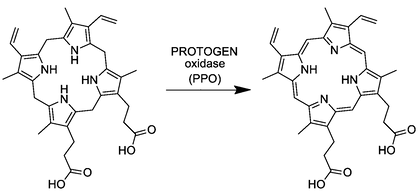
Седьмая реакция синтеза гема, в которой происходит образование молекул протопорфирина IX, путём окисления протопорфориногена IX, под действием фермента протопорфириноген IX оксидазы (КФ 1.3.3.4)[7]. Реакция протекает в митохондриальном матриксе. Схема реакции:
Протопорфирин IX является первым окрашенным тетрапирролом в синтезе гема.
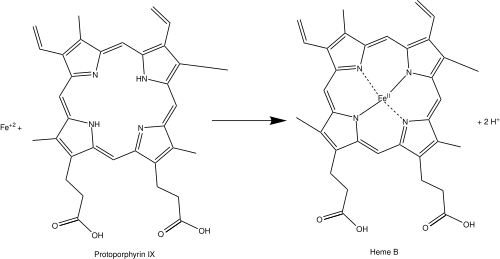
Последняя реакция, которая завершает многостадийный процесс синтеза гема. В данной реакции происходит внедрение ионов железа (металлирование) внутрь плоского макроцикла протопорфирина IX. Катализирует реакцию фермент феррохелатаза (КФ 4.98.1.1). Схема реакции:
- протогем (гем Б) + 2H+ = протопорфирин IX + Fe+2.
Феррохелатаза очень чувствительна к воздействию ионов тяжёлых металлов (Mn2+, Pb2+, Hg2+ и Cd2+), но в особенности к ионам свинца Pb2+, которые препятствуют высвобождению продукта после металлирования[8].