ARNTL
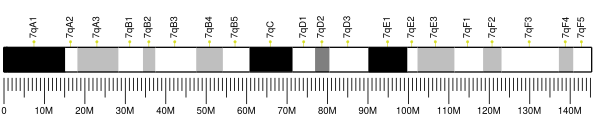
ARNTL (сокр. от англ. Aryl hydrocarbon receptor nuclear translocator-like protein 1) — белок, подобный ядерному транслокатору AHR, кодируется одноимённым геном ARNTL, расположенным на коротком плече (p-плече) 11-ой хромосомы[4]. Также известен как BMAL1, MOP3 и, реже, BHLHE5, BMAL, BMAL1C, JAP3, PASD3 и TIC.
Белок состоит из последовательности 626 аминокислотных остатков и имеет молекулярную массу 68 762 Да[5].
Общие сведения
История
Ген ARNTL был первоначально обнаружён в 1997 году двумя группами исследователей: Джоном Б. Хогеншом и сотруд. в марте[6] и Икедой и Номурой в апреле[7], как часть надсемейства факторов транскрипции домена PAS[6]. Было обнаружено, что белок ARNTL, также известный как MOP3, димеризуется с MOP4, CLOCK и факторами, индуцируемые гипоксией[8]. Названия белкам BMAL1 и ARNTL были даны в последующих статьях. Одна из ранних обнаруженных функций белка ARNTL в циркадной регуляции была связана с гетеродимером CLOCK:BMAL1 (CLOCK:ARNTL), который связывался бы через энхансер E-box для активации транскрипции гена, кодирующего гормон вазопрессин[9]. Однако значение гена в циркадных ритмах не было полностью реализовано до тех пор, не был проведён пока нокаут гена у мышей и не продемонстрировал полную потерю циркадных ритмов в локомоции и других видах поведения[10].
Структура
Белок BMAL1 содержит четыре домена в соответствии с его кристаллографической структурой: домен bHLH, два домена PAS, называемые PAS-A и PAS-B, и транс-активирующий домен. Димеризация белков CLOCK: BMAL1 включает сильные взаимодействия между доменами bHLH, PAS-A и PAS-B как CLOCK, так и BMAL1 и образует асимметричный гетеродимер с тремя различными белковыми интерфейсами. Взаимодействие PAS-A между CLOCK и BMAL1, состоит из α-спирали CLOCK PAS-A и ß-листа BMAL1 PAS-A и α-спирального мотива домена BMAL1 PAS-A и ß-листа CLOCK PAS-A[11]. Области CLOCK и BMAL1 PAS-B располагаются параллельно, что приводит к сокрытию различных гидрофобных остатков аминокислот на ß-листе BMAL1 PAS-B и спиральной поверхности CLOCK PAS-B, таких как остатки Tyr 310 и Phe 423[11]. Ключевые взаимодействия со специфическими аминокислотными остатками, особенно CLOCK His 84 и BMAL1 Leu 125, важны для димеризации этих молекул[12].
Функции
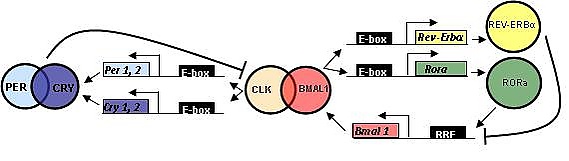
Белок, кодируемый геном Bmal1 у млекопитающих, связывается со вторым белком bHLH-PAS через домен PAS, CLOCK (или его паралог, NPAS2) с образованием гетеродимера в клеточном ядре[13]. Через свой домен BHLH этот гетеродимер связывается с элементами отклика E-box[14] в областях промотора Per (Per1 и Per2) и Cry генов (Cry1 и Cry2)[14]. Это связывание активирует транскрипцию и трансляцию белков PER1, PER2, CRY1 и CRY2.
После того, как белки PER и CRY накапливаются до достаточных концентраций, они взаимодействуют со своими мотивам PAS с образованием большого репрессорного комплекса, который перемещается в ядро, чтобы ингибировать транскрипционную активность гетеродимера CLOCK:BMAL1[15]. Этот процесс приводит к ингибированию транскрипции Per и Cry гены, и вызывает снижение концентрации белка PER и CRY. Эта транскрипция, петля отрицательной обратной связи трансляции (TTFL) модулируется в цитоплазме путём фосфорилирования белков PER казеинкиназой 1ε или δ (CK1 ε или CK1 δ), сигнализируя эти белки для деградации протеасомами 26S[14][16]. SIRT1 также регулирует деградацию белка PER посредством ингибирования транскрипционной активности гетеродимера BMAL1:CLOCK путем циркадного (кругового) деацетилирования[17]. Деградация PER-белков предотвращает образование комплекса больших белков и, таким образом, предотвращает ингибирование транскрипционной активности гетеродимера BMAL1:CLOCK[14]. Белок CRY также сигнализируют о деградации поли-убиквированием белка FBXL3, также предотвращая ингибирование гетеродимера CLOCK:BMAL1. Это позволяет возобновить транскрипцию генов Per и Cry. В петле TTFL ночных мышей наблюдалось, что уровни транскрипции пика гена Bmal1 в CT18 во время средней субъективной ночи имеют антифазный уровень транскрипции Per, Cry и других генов контроля частоты, пик в CT6, в середине-субъективного дня. Этот процесс происходит с длиной периода около 24 часов и поддерживает представление о том, что этот молекулярный механизм ритмичен[18].
В дополнение к циркадной регуляторной TTFL-петле, описанной выше, транскрипция Bmal1 регулируется конкурентным связыванием с сайтом связывания с ретиноидной кислотой, связанным с сайтом-рецептором (RORE) в промоторной области Bmal1. Гетеродимер CLOCK:BMAL1 также связывается с элементами E-box в промоторных областях генов Rev-Erbα и RORα/ß, активируя транскрипцию и трансляцию белков REV-ERB и ROR. Белки REV-ERBα и ROR регулируют экспрессию BMAL1 через вторичный контур обратной связи и конкурируют за связывание с элементами ответа Rev-Erb/ROR в промоторной области Bmal1, в результате чего экспрессию BMAL1 подавляют REV-ERBα и активируют белки ROR. Было показано, что другие ядерные рецепторы тех же семейств (NR1D2 (Rev-erb-β), NR1F2 (ROR-β) и NR1F3 (ROR-γ)) также действуют на транскрипционную активность Bmal1[19][20][21][22].
Несколько посттрансляционных модификаций BMAL1 определяют время циклов обратной связи CLOCK:BMAL1. Фосфорилирование BMAL1 нацеливает его на убиквитинирование и деградацию, а также на деубиквитинирование и стабилизацию. Ацетилирование BMAL1 рекрутирует CRY1 для подавления трансактивации CLOCK:BMAL1[23]. Сумоилирование BMAL1 с помощью небольшого модификатора, связанного с убиквитином 3 (SUMO3), сигнализирует о его убиквитинировании в ядре, что приводит к трансактивации гетеродимера CLOCK:BMAL1[24]. Трансактивация комплекса CLOCK:BMAL1[25] активируется фосфорилированием казеинкиназы 1ε и ингибируется фосфорилированием MAPK[26]. Фосфорилирование CK2α регулирует внутриклеточную локализацию BMAL1[27], а фосфорилирование GSK3B контролирует стабильность BMAL1 и предготавливает его для последующего убиквитинирования[28].
Ген Arntl у крыс расположен в локусах восприимчивости гипертензии 1 хромосомы. Изучение мононуклеотидных полиморфизмов (SNP) в этих локусах обнаружило два полиморфизма, которые происходили в последовательности, кодирующей Arntl, и были связаны с диабетом II типа и гипертонией. При переходе от модели крысы к человеческой модели это исследование предполагает причинную роль вариации гена Arntl в патологии диабета II типа[29]. Недавние данные о фенотипах также предполагают, что этот ген[30] и его партнёр clock[31] играют роль в регуляции гомеостаза и метаболизма глюкозы, и при нарушениях могут привести к гипоинсулинемии или диабету[32]. Что касается других функций, то в другом исследовании показано, как комплекс CLOCK:BMAL1 повышает активность промотора LDLR человека, показывая, что ген Arntl также играет роль в гомеостазе холестерина[33]. Кроме того, было обнаружено, что экспрессия гена Arntl, наряду с генами других генов клеточного ядра, была ниже у пациентов с биполярным расстройством, что указывает на проблему с циркадной функцией у этих пациентов[34]. Arntl, Npas2 и Per2 также были связаны с сезонным аффективным расстройством у людей[35]. Наконец, Arntl был идентифицирован посредством функционального генетического скрининга как предполагаемого регулятора пути онкосупрессора р53, потенциально возможное участие в циркадных ритмах, которые проявляются злокачественными клетками[36].