Трифторуксусная кислота
Трифтору́ксусная кислота́ (трифторэтановая кислота, ТФУК) — органическое соединение, содержащее фтор, фторорганическая карбоновая кислота. Бесцветная дымящаяся жидкость с резким специфическим запахом (отдалённо напоминающим запах уксусной кислоты)[6].
Общие сведения
| Трифторуксусная кислота | |
|---|---|
| Общие | |
| Систематическое наименование |
Трифторэтановая кислота |
| Традиционные названия | Трифторуксусная кислота, ТФУК |
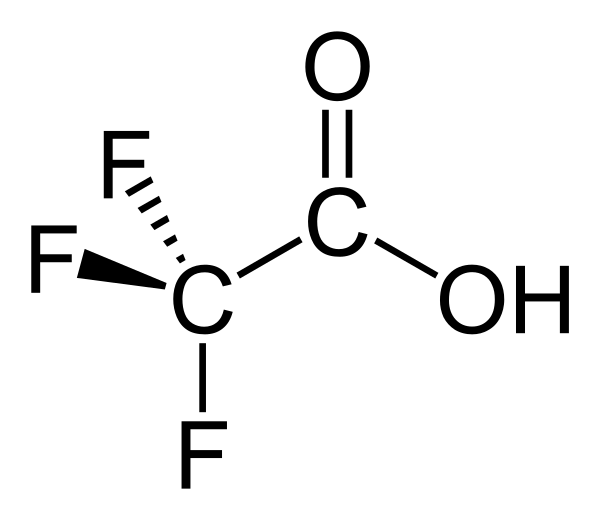
| Хим. формула | CF3COOH |
| Физические свойства | |
| Состояние | бесцветная жидкость |
| Молярная масса | 114,03 г/моль |
| Плотность | 1,531 г/см³ |
| Поверхностное натяжение | 13,53 ± 0,01[1] и 11,42 ± 0,01[1] |
| Динамическая вязкость | 0,808 ± 0,001[2] и 0,571 ± 0,001[2] |
| Термические свойства | |
| Температура | |
| • плавления | -15,36 °C |
| • кипения | 72,4 °C |
| Критическая точка | 218,15 |
| Давление пара | 10 ± 1[3], 15,1 ± 0,1[4] и 100 ± 1[3] |
| Химические свойства | |
| Константа диссоциации кислоты | 0,23 |
| Растворимость | |
| • в воде | смешивается |
| Структура | |
| Дипольный момент | 2,28 ± 0,25[5] |
| Классификация | |
| Рег. номер CAS | 76-05-1 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 6422 |
| UNII | E5R8Z4G708 |
| CompTox Dashboard EPA | DTXSID9041578 |
| Рег. номер EINECS | 200-929-3 |
| SMILES | |
| InChI | |
| RTECS | AJ9625000 |
| ChEBI | 45892 |
| ChemSpider | 10239201 |
| ECHA InfoCard | 100.000.846 |
| Безопасность | |
| NFPA 704 | |
Химические свойства
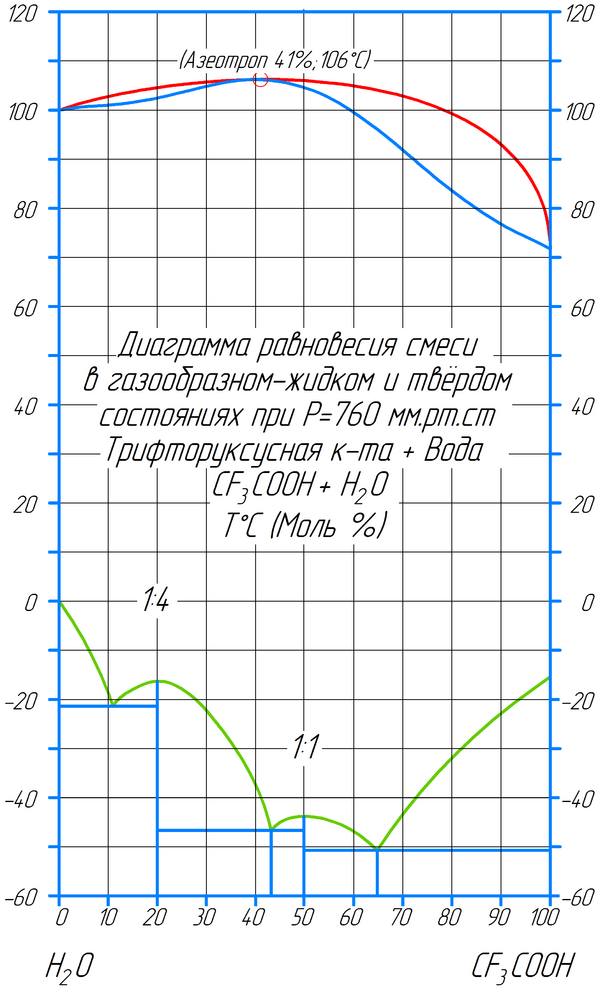
Смешивается во всех отношениях с водой, этанолом, ацетоном, диэтиловым эфиром. С водой образует азеотропную смесь (20,6 масс% воды, 79,4 масс% кислоты) (т. кип. 105,46 0C, )[7].
Типичная сильная карбоновая одноосновная кислота. Разрушает металлы, пробку, резину, бакелит, полиэтилен. Не действует на фторопласт и сухое стекло. Термически стабильна, не разлагается при нагревании до 400 °С[8].
С диалкиловыми эфирами, кетонами, карбоновыми кислотами и другими электронодонорными соединениями даёт прочные комплексы. Легко присоединяется по кратным связям алкенов, циклоалкенов, ацетиленов с образованием трифторацетатов. С галогенами даёт малоустойчивые гипогалогениты CF3COOHal, которые селективно галогенируют различные соединения. Реакция с многоатомными спиртами (например, с триолами) приводит к полициклическим ортоэфирам.
При действии оксида фосфора(V) на трифторуксусную кислоту образуется ангидрид трифторуксусной кислоты ((CF3CO)2O) — сильный ацилирующий агент. Реакция трифторуксусной кислоты со спиртами даёт эфиры, с аминами — амиды, с карбоновыми кислотами — смешанные ангидриды. Последние, а также (CF3CO)2O в присутствии минеральных кислот или сульфокислот используют в качестве промоторов при ацилировании спиртов, фенолов, тиолов
При нагревании серебряной соли трифторуксусной кислоты с избытком I2 образуется трифторметилиодид;
При восстановлении трифторуксусной кислоты и её эфиров LiAlH4 при О °C - трифторацетальдегид CF3CHO, а при избытке восстановителя при 30 °C - 2,2,2-трифторэтанол.
Регенерировать «сухую» ТФУК можно ректификацией с осушителем (Серная кислота, Ангидридом или оксидом фосфора) или вымораживанием.
В жидком виде и в парах вызывает сильные ожоги кожных покровов и слизистых оболочек. ПДК в воздухе рабочей зоны 2 мг/м3.
Получение
Трифторуксусную кислоту на производстве получают электрохимическим фторированием уксусного ангидрида или фторангидрида в безводном HF. В лаборатории чаще используют кислотный гидролиз 1,1,1-трифтор-2,2,2-трихлорэтана или окисление 2,2,2-трифторэтанола[9].
Применение
Трифторуксусную кислоту применяют в качестве сырья в органическом синтезе, катализатора в реакциях этерификации и полимеризации, растворителя для ряда термостойких полимеров. Трифторацетангидрид используют в производстве ацетатного шёлка (США, Великобритания), фармацевтических препаратов, пестицидов, в качестве реагента для защиты функциональных групп в синтезе пептидов[10].
Экология
Трифторуксусная кислота относится к «вечным химикатам», т. к. её прочные углерод-фтористые связи не разрушаются под воздействием естественных процессов. Она поступает в окружающую среду из промышленных выбросов, при распаде хладагентов, пестицидов и лекарственных средств.
В 2025 году трифторуксусная кислота выявлена в осадках по всему миру. Учёные сообщили о повышении её концентрации в озёрах, реках, бутилированной воде и других напитках, зерновых культурах, печени животных, крови людей, в канадских арктических льдах и грунтовых водах Дании. Так, содержание ТФУК в листьях и иголках деревьев в Германии за последние 40 лет выросло в 5–10 раз.
Воздействие ТФУК на здоровье недостаточно изучено. Одни экологи утверждают, что она не накапливаются в организме человека и животных, а другие считают, что рост её концентрации в окружающей среде может нанести необратимый вред[11].
Галерея
Примечания
- ↑ 1 2 CRC Handbook of Chemistry and Physics (англ.) / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6—182. — ISBN 978-1-4822-0868-9
- ↑ 1 2 CRC Handbook of Chemistry and Physics (англ.) / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6—231. — ISBN 978-1-4822-0868-9
- ↑ 1 2 CRC Handbook of Chemistry and Physics (англ.) / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6—95. — ISBN 978-1-4822-0868-9
- ↑ CRC Handbook of Chemistry and Physics (англ.) / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 15—21. — ISBN 978-1-4822-0868-9
- ↑ CRC Handbook of Chemistry and Physics (англ.) / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 9—59. — ISBN 978-1-4822-0868-9
- ↑ CRC Handbook of Chemistry and Physics (англ.) // Taylor & Francis / William M. Haynes. — 2014-06-04. — doi:10.1201/b17118.
- ↑ Никольский Б.П., Григоров О.Н., Позин М.Е. Справочник химика. www.studmed.ru. Дата обращения: 25 июля 2025.
- ↑ Рабинович В. А., Хавин З. Я. Краткий химический справочник. — Л.,: Химия, 1977. — С. 184.
- ↑ Органические реакции / пер. с англ. А. Ф. Платэ, под ред. И. Ф. Луценко. — М.,: Мир, 1965. — С. 134.
- ↑ Günter Siegemund, Werner Schwertfeger, Andrew Feiring, Bruce Smart, Fred Behr, Herward Vogel, Blaine McKusick. Fluorine Compounds, Organic // Ullmann's Encyclopedia of Industrial Chemistry. — 2000-06-15. — doi:10.1002/14356007.a11_349.
- ↑ Растущую концентрацию «вечного химиката» выявили в осадках по всему миру. Мир 24. Дата обращения: 28 июля 2025.
Литература
- «Краткая химическая энциклопедия». — т.5, Т-Я. — М.: Советская энциклопедия, 1967. — С. 276
- «Промышленные фторорганические продукты: Справочник». — Л.: Химия, 1990. — С. 367—371
- «Справочник химика». — Т.3. — М.-Л.: Химия, 1965. — С. 118
- «Химическая энциклопедия». — Т.5. — М.: Советская энциклопедия, 1999. — С. 9
- Альберт А., Сержент Е. «Константы ионизации кислот и оснований». — М.-Л.: Химия, 1964. — С. 118
- Гудлицкий М. «Химия органических соединений фтора». — М.: ГНТИХЛ, 1961. — С. 270
- Некрасов Б. В. «Основы общей химии». — Т.1. — М.: Химия, 1973. — С. 563—564
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник». — Л.: Химия, 1977. — С. 184
- Промышленные фторорганические продукты. Справочник, Л., 1990, с. 367-71. И. И. Крылов.
- Физер Л., Физер M., Реагенты для органического синтеза, пер. с англ., т. 3, M., 1970;
- Исикаве H., Кобаяси Ё., Фтор. Химия и применение, пер. с япон., M., 1982;