Постулаты Бора (ЕГЭ-ОГЭ)
Бо́ровская моде́ль а́тома (также известная как модель Бо́ра или модель Бо́ра — Резерфо́рда) — полуклассическая модель атома, предложенная Нильсом Бором в 1913 году[1].
Бор опирался на пл
анетарную модель атома, предложенную Эрнестом Резерфордом. Однако согласно классической электродинамике электрон, движущийся по орбите, постоянно излучал бы энергию и быстро падал на ядро. Чтобы устранить это противоречие, Бор ввёл допущение, что электроны могут находиться только на определённых стационарных орбитах, где они не излучают. Поглощение или испускание энергии происходит лишь при скачкообразном переходе между такими орбитами. Стационарными считаются только те орбиты, при движении по которым момент количества движения электрона равен целому числу постоянных Планка: .
Применив это допущение совместно с законами классической механики — а именно приравняв силу притяжения электрона со стороны ядра к центробежной силе, действующей на вращающийся электрон — Бор получил выражения для радиуса стационарной орбиты и энергии электрона на ней:
Здесь — масса электрона, — число протонов в ядре, — электрическая постоянная, — заряд электрона.
Именно такое выражение для энергии можно получить, применяя уравнение Шрёдингера в задаче о движении электрона в центральном кулоновском поле.
Радиус первой орбиты в атоме водорода R0=5,2917720859(36)⋅10−11 м[2] получил название боровского радиуса или атомной единицы длины и широко используется в современной физике. Энергия первой орбиты эВ соответствует энергии ионизации атома водорода.
Полуклассическая теория Бора
Основана на двух постулатах Бора:
- В атоме возможны только особые стационарные или квантовые состояния, каждое из которых характеризуется определённым уровнем энергии. В стационарном состоянии атом не излучает электромагнитных волн.
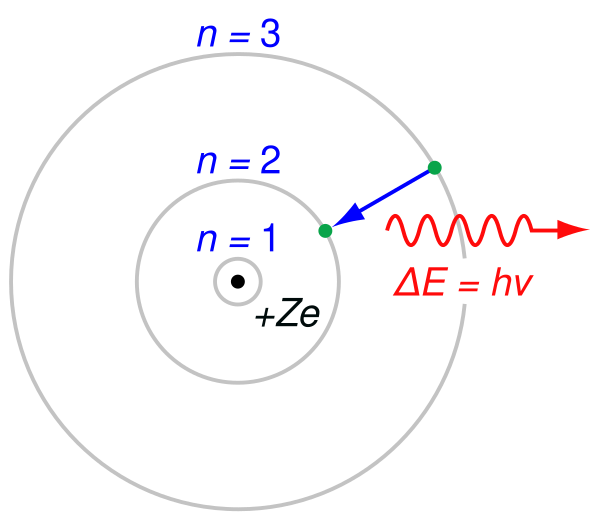
- Излучение и поглощение энергии атомом происходит только при скачкообразном переходе между двумя стационарными состояниями. При этом имеют место два соотношения:
- где — излучённая (поглощённая) энергия, — номера квантовых состояний. В спектроскопии и называются термами.
- Правило квантования момента импульса:
Далее, исходя из классической картины кругового движения электрона вокруг неподвижного ядра по стационарной орбите под действием кулоновской силы, Бором были получены выражения для радиусов стационарных орбит и энергии электрона на этих орбитах:
- м — боровский радиус.
- — энергетическая постоянная Ридберга (численно равна 13,6 эВ).
Достоинства теории Бора
- Объяснила дискретность энергетических состояний водородоподобных атомов.
- Предложила принципиально новый подход к описанию внутриатомных процессов и стала первой полуквантовой теорией атома.
- Эвристическая ценность теории заключается в гипотезе о существовании стационарных состояний и резких переходов между ними, что позднее было распространено на другие микросистемы.
Недостатки теории Бора
- Не смогла объяснить интенсивность спектральных линий.
- Применима только к водородоподобным атомам и не работает для элементов, следующих за ним в таблице Менделеева, без экспериментальных данных (энергии ионизации или других).
- Логически противоречива: не является ни классической, ни квантовой. Система содержит два уравнения — классическое уравнение движения электрона и квантовое условие квантования орбит.
Модель Бора оказалась недостаточно последовательной и общей, поэтому была заменена современной квантовой механикой, основанной на более общих и непротиворечивых постулатах. Сегодня постулаты Бора рассматривают как следствие фундаментальных квантовых законов, однако правила квантования по-прежнему применяются в качестве приближённых соотношений благодаря высокой точности.
Примечания
Категории
| Правообладателем данного материала является АНО «Интернет-энциклопедия «РУВИКИ». Использование данного материала на других сайтах возможно только с согласия АНО «Интернет-энциклопедия «РУВИКИ». |