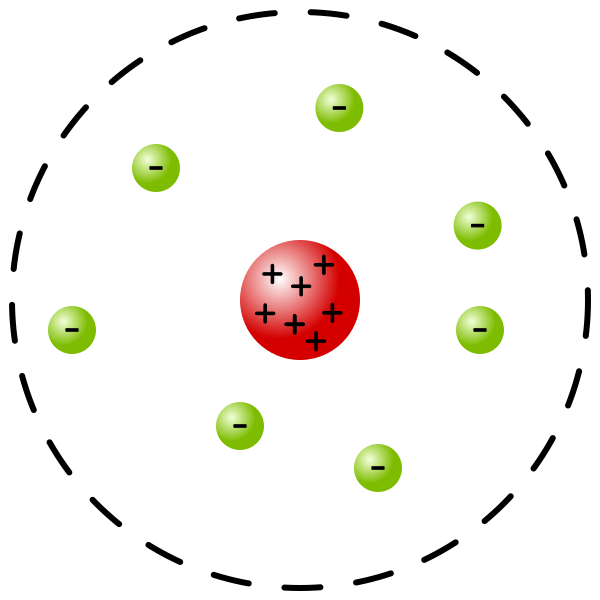
Планетарная модель атома
Планета́рная моде́ль а́тома, или модель атома Резерфо́рда, — исторически важная модель строения атома, предложенная Эрнестом Резерфордом в классической статье[1], опубликованной в 1911 году на основании анализа и статистической обработки результатов экспериментов по рассеиванию альфа-частиц в тонкой золотой фольге, выполненных Гейгером и Марсденом в 1909 году.
В этой модели Резерфорд описывает строение атома так: в центре атома находится очень маленькое, положительно заряженное ядро, в котором сосредоточена почти вся масса атома; вокруг этого ядра вращаются электроны подобно тому, как планеты движутся вокруг Солнца в Солнечной системе.
Планетарная модель атома соответствует современным представлениям о строении атома с некоторыми уточнениями: движение электронов не может быть описано законами классической механики, а имеет квантовомеханическое описание.
Исторически планетарная модель Резерфорда пришла на смену одной из моделей Томсона «пудинга с изюмом», которая предполагает, что отрицательно заряженные электроны размещены на круговых орбитах внутри положительно заряженного атома с распределённым по всему его объёму положительным зарядом, подобно изюминкам в пудинге[2]. На самом деле в своих опытах Резерфорд фактически подтвердил состоятельность другой модели Томсона, предполагающей планетарное строение атома.
Предыстория
К 1904 году японский физик Нагаока Хантаро разработал раннюю, как оказалось впоследствии, ошибочную «планетарную модель» атома («атом типа Сатурна»)[3]. Модель была построена на аналогии с расчётами устойчивости колец Сатурна (кольца уравновешены из-за очень большой массы планеты). Модель Нагаоки была неверна, но два следствия из неё оказались пророческими:
- ядро атома действительно оказалось очень массивным;
- электроны удерживаются на орбите благодаря электростатическим силам (подобно тому, как кольца Сатурна удерживаются гравитационными силами).
Новую модель строения атома Резерфорд предложил в 1911 году на основе анализа экспериментов по рассеиванию альфа-частиц в золотой фольге, проведённых в 1909 году под его руководством[1].
При этом рассеянии неожиданно большое, статистически необъяснимое количество альфа-частиц рассеивалось на большие углы, что свидетельствовало о том, что центр рассеяния имеет небольшие размеры, и в нём сосредоточен значительный электрический заряд и масса всего атома.
Расчёты Резерфорда показали, что рассеивающий центр, заряженный положительно или отрицательно, должен быть по крайней мере в 3000 раз меньше размера атома, который в то время уже был известен и оценивался примерно в 10−10 м. Поскольку в то время электроны уже были известны, а их масса и заряд определены, то рассеивающий центр, который позже назвали ядром, должен был иметь противоположный электронам заряд (положительный). Резерфорд не связал величину заряда с атомным номером. Этот вывод был сделан позже. Резерфорд предположил, что заряд ядра пропорционален атомной массе. Связь электрического заряда ядра с атомным номером химического элемента установил Генри Мозли в экспериментах, выполненных в 1913 году.
Недостатком планетарной модели была невозможность объяснения ею устойчивости атомов. Так как электроны движутся вокруг ядра, испытывая при этом центростремительное ускорение подобно тому, как планеты вследствие действующих на них гравитационных сил Солнца, то они, по законам классической электродинамики, должны излучать электромагнитные волны, теряя при этом кинетическую энергию орбитального движения на излучение, и в результате «упасть» на ядро. Расчёты, выполненные с помощью методов классической электродинамики показывают, что электроны должны «упасть» на ядро за время порядка 10−11 с.
Это противоречие было снято последующим развитием планетарной модели в модели атома Бора, постулирующая другие, отличные от классических законы орбитального движения электронов на основе волн де Бройля. Полностью противоречащие эксперименту выводы классической электродинамики смогло объяснить только развитие квантовой механики.
Примечания
Литература
- Яворский Б. М. Детлаф, А. А. Курс физики. Том III. Волновые процессы, оптика, атомная и ядерная физика. — М. : Высшая школа, 1972.
- Савельев И. В. Курс общей физики. Учебник. Том 3 : Квантовая оптика. Атомная физика. Физика твёрдого тела. Физика атомного ядра и элементарных частиц. — СПб. : Лань, 2019.
- Бор О., Моттельсон Б. Структура атомного ядра. — М. : Мир, 1971.