Деградосома
Деградосо́ма[1] (англ. degradosome) — мультибелковый бактериальный комплекс, который участвует в процессинге рибосомальной РНК и деградации матричной РНК, регулируется некодирующими РНК. Он состоит из РНК-хеликазы B, рибонуклеазы Е (РНКазы Е), полинуклеотидфосфорилазы, а также гликолитического фермента енолазы[2]. Деградосому можно изучать с помощью электронной микроскопии[3].
Пул РНК в клетке постоянно меняется. Например, у Escherichia coli срок жизни мРНК составляет от 2 до 25 минут, у других бактерий он может быть больше. Даже в клетках, находящихся в состоянии покоя, РНК постоянно разрушается, и свободные нуклеотиды, образовавшиеся при этом, в дальнейшем используются в синтезе нуклеиновых кислот. Кругооборот РНК чрезвычайно важен для регуляции экспрессии генов. мРНК бактерий крайне нестабильны по сравнению с мРНК эукариот. Это может быть связано с тем, что бактериям приходится быстрее репрограммировать свой пул мРНК (а следовательно, и белков) в ответ на быстро меняющиеся условия окружающей среды[1].
В клетках всех организмов имеются специальные инструменты для деградации РНК, например, РНКазы, хеликазы, 3'-концевые нуклеотидилтрансферазы, которые добавляют нуклеотидные хвосты к транскриптам, 5'-кэпирующие и декэпирующие ферменты, а также разнообразные РНК-связывающие белки. Часто перечисленные белки собираются в стабильные мультибелковые комплексы, в которых их активность скоординирована. У эукариот таким комплексом является экзосома, а у бактерий — деградосома.
Структура
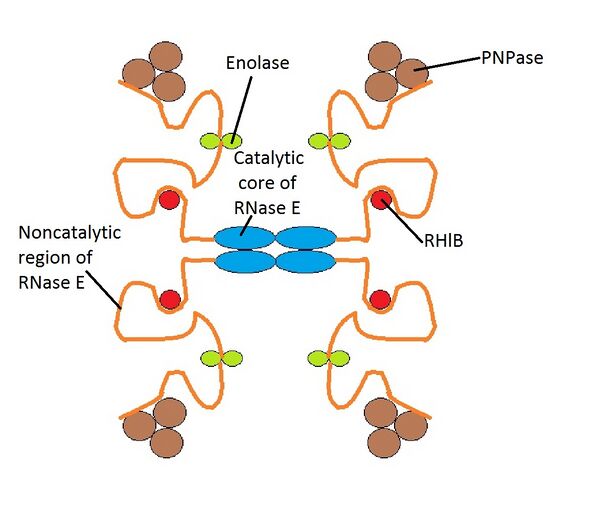
У E. coli масса деградосом составляет от 160 до 400 кДа, а константа седиментации — 8−16 S[1]. Деградосома достаточно крупна, чтобы быть различимой в электронный микроскоп рядом с внутренней мембраной бактерии[4]. Состав мультибелковой деградосомы может варьировать от организма к организму. У E. coli в состав деградосомы входят четыре основных компонента:
- РНКаза Е. Это большая гидролитическая эндорибонуклеаза, в которой можно выделить N-концевую часть, содержащую каталитический домен, и неструктурированную C-концевую часть, функции которой неизвестны, но, по-видимому, она необходима для сборки деградосомы. С-концевая часть РНКазы Е очень гибкая, что обеспечивает возможность взаимодействия для различных компонентов деградосомы. У E. coli РНКаза Е находится в цитоплазматической мембране, и за ней можно наблюдать с помощью флуоресцентного микроскопа. В состав РНКазы Е входят 1061 аминокислотных остатка, а масса этого белка составляет 118 кДа[5].
- Полинуклеотидфосфорилаза (англ. Polynucleotide phosphorylase, PNPase). Это фосфоролитическая экзорибонуклеаза, разрушающая РНК. В состав этого белка входят 421 аминокислотных остатка, а его масса составляет 47 кДа. Она при помощи неорганического фосфата отщепляет от 3'-конца транскрипта по одному нуклеозиддифосфатному остатку[1].
- Енолаза: гликолитический фермент из 432 аминокислотных остатков, массой 46 кДа.
- РНК-хеликаза (RhlB) из 711 аминокислотных остатков, массой 77 кДа. Идентификация этого DEAD-бокс-содержащего белка в деградосоме E. coli была одним из первых свидетельств того, что РНК-хеликазы могут участвовать в деградации мРНК[6]. За счёт энергии АТФ этот фермент расплетает дуплексы в РНК[1].
Возможно, в состав деградосом входит РНКаза III, расщепляющая двухцепочечные участки РНК[1]. Также в состав деградосомы могут входить шапероны GroEL и DnaK[1].
С деградосомой тесно связана полифосфаткиназа (хотя она и не входит в состав деградосомы). Этот фермент образует АТФ для работы хеликазы согласно уравнению (Ф)n + АДФ → (Ф)n−1 + АТФ[7].
Имеются различные варианты деградосом, содержащие разные белки. Дополнительными компонентами деградосомы могут быть PcnB (поли(А)-полимераза) и РНК-хеликазы RhlE и SrmB. В условиях холодового шока в состав деградосомы может входить РНК-хеликаза CsdA. В стационарной фазе в состав деградосомы могут входить такие дополнительные компоненты, как РНКаза R (Rnr) и предполагаемая РНК-хеликаза HrpA. Кроме того, в число белков деградосомы может входить РНК-шаперон Hfq, простатическая кислая фосфатаза (PAP), другие шапероны, а также рибосомные белки[8].
Структура деградосомы E. coli в точности неизвестна, хотя существует модель её работы. Предполагается, что структура деградосомы нестабильна, и каждый её компонент взаимодействует с другими компонентами, находящимися в непосредственной его близости[6].
Функции
Деградосома — это большой мультиферментный комплекс, участвующий в метаболизме РНК и посттранскрипционной регуляции экспрессии генов у разнообразных бактерий, в числе которых Escherichia coli и Pseudoalteromonas haloplanktis. Он задействован в процессинге структурированных предшественников РНК в ходе их созревания[9][10].
Предполагается, что РНК-хеликаза играет вспомогательную роль в разрушении РНК, расплетая вторичные структуры РНК. Иногда вместе с деградосомами выделяется рРНК, подтверждая, что эти комплексы участвуют в деградации рРНК и мРНК. О роли деградосомы информации очень мало. При исследовании деградации транскриптов E. coli было показано, что первыми в ход вступают эндорибонуклеазы, которые надрезают РНК, с тем чтобы экзонуклеазы закончили разрушение получаемых фрагментов. РНК-хеликаза RhIB сама по себе малоактивна, но взаимодействие с РНКазой Е может усиливать её[11]. Роль енолазы в процессе разрушения РНК пока непонятна, но, возможно, она увеличивает специфичность комплекса[12][13]. Известно, однако, что енолаза в составе деградосомы необходима для быстрого разрушения мРНК глюкозного транспортёра в ответ на фосфосахарный стресс у E. coli[14].
Активация
Активация деградосомы происходит под действием некодирующих РНК, соответствующих микроРНК эукариот. Существует два пути для направления РНК на разрушение: связывание с участком инициации трансляции или с кодирующей последовательностью. Для связывания некодирующей РНК с мРНК-мишенью необходим шаперон Hfq. Прикрепившийся комплекс Hfq и некодирующей РНК не даёт рибосоме связаться с транскриптом и активирует нуклеазы (РНКазу Е) для его разрушения. При связывании с кодирующей последовательностью комплекс не даёт рибосоме двигаться дальше, запуская процесс разрушения[9].
Разрушение РНК
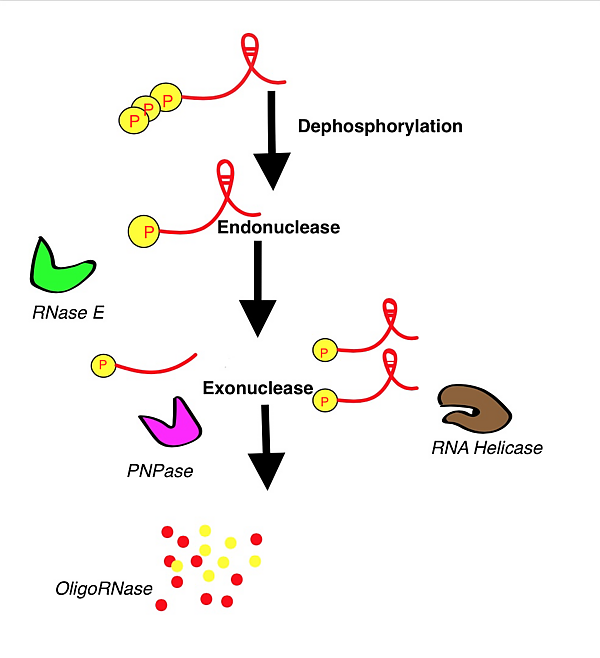
Процесс разрушения РНК очень сложен. В качестве примера рассмотрим наиболее изученное разрушение — мРНК деградосомой Escherichia coli. В разрушении мРНК участвуют как эндо-, так и экзонуклеазы. Фермены РНКаза II и полинуклеотидфосфорилаза (ПНФаза) разрушают мРНК в направлении 3' → 5'. В деградосоме можно выделить 4 компартмента, содержащие несколько РНКаз. С самого начала новосинтезированная мРНК содержит полифосфат. Поэтому первой стадией разрушения мРНК является дефосфорилирование с образованием монофосфата под действием РНК-пирофосфогидролазы. В транскрипте, помимо фосфатного конца (Р-конца), имеется концевая шпилька. Р-конец разрезается эндорибонуклеазой РНКазой Е, а шпилька устраняется РНК-хеликазами. Если в транскрипте имеются дополнительные вторичные структуры, то для упрощения работы экзорибонуклеаз (например, ПНФазы) необходимо действие полимеразы РАР. Наконец, отдельные фрагменты расщепляются олигорибонуклеазами. У других микроорганизмов процесс происходит схожим образом, хотя ферментный состав комплекса может отличаться. Например, у Bacillus subtilis в качестве эндорибонуклеазы вместо РНКазы Е используются РНКазы Y или J, а у архей РНК разрушается экзосомами[9].
Эволюция
Хотя структура деградосомы динамична, её состав вариабелен, а в некоторых лабораторных условиях деградосома и вовсе не нужна, она, тем не менее, сохранилась в ходе эволюции, возможно, из-за того, что она участвует во многих процессах, регулирующих экспрессию генов. Экспериментально было продемонстрировано, что у E. coli наличие экзосомы является селективным преимуществом. Гомологи белков деградосомы E. coli прослеживаются во всех доменах жизни[9]. Стоит, однако, отметить, что у E. coli процесс разрушения РНК не может идти в направлении 5' → 3'. На 5'-конце мРНК E. coli нет кэпа, а экзонуклеазы, работающие в направлении 5' → 3', неизвестны. Похожая ситуация имеет место и у других бактерий, поэтому разрушение транскриптов 5' → 3' может быть уникальной чертой эукариотических клеток[11].
См. также
Примечания
Литература
- Пиневич А. В. Микробиология. Биология прокариотов: в 3 т. — СПб.: Издательство С.-Петербургского университета, 2006. — Т. I. — 352 с. — ISBN 5-288-04057-5.