Гистондеацетилаза 8
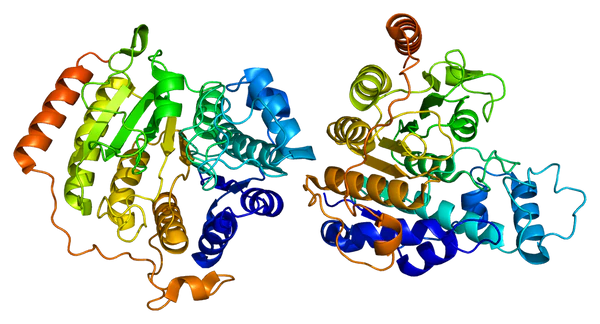
Гистондеацетилаза 8 (англ. Histone deacetylase 8) — фермент, кодируемый у человека геном HDAC8 [5][6][7].
Что важно знать
Функция
Гистоны играют важнейшую роль в регуляции транскрипции, прогрессировании клеточного цикла и процессов развития. Ацетилирование/деацетилирование гистонов изменяет хромосомную структуру и влияет на доступ факторов транскрипции к ДНК. Белок, кодируемый этим геном относится к классу I в семействе гистондезацетилазы/acuc/Apha. Он обладает деятельностью гистондеацетилазы и подавляет транскрипцию, когда связан с промотором[7].
Гистондеацетилаза 8 участвует в морфогенезе черепа[8] и метаболическом контроле над комплексом транскрипции альф/PGC1-alpha[9].
Клиническое значение
HDAC8 был связан с некоторым числом болезненных состояний, в частности, с острым миелоидным лейкозом, а также связан с актиновым цитоскелетом в клетках гладких мышц. миРНК ориентированные на HDAC8 показали противораковые эффекты[10]. Ингибирование индуцированного апоптоза посредством HDAC8 наблюдается при Т-клеточных лимфомах[11]. Кроме того фермент HDAC8 участвует в патогенезе нейробластомы[12]. Таким образом, существует интерес к разработке селективных ингибиторов на базе HDAC8[13][14].
См. также
Примечания
Литература
- Waltregny D., De Leval L., Glénisson W., Ly Tran S., North B.J., Bellahcène A., Weidle U., Verdin E., Castronovo V. Expression of histone deacetylase 8, a class I histone deacetylase, is restricted to cells showing smooth muscle differentiation in normal human tissues. (англ.) // Am J Pathol. : journal. — 2004. — Vol. 165, no. 2. — P. 553—564. — doi:10.1016/S0002-9440(10)63320-2. — PMID 15277229. — PMC 1618574.
- Glénisson W., Waltregny D., Tran S.L., North B.J., Verdin E., Colige A., Castronovo V. Histone deacetylase HDAC8 associates with smooth muscle alpha-actin and is essential for smooth muscle cell contractility. (англ.) // The FASEB Journal : journal. — Federation of American Societies for Experimental Biology, 2005. — June (vol. 19, no. 8). — P. 966—968. — doi:10.1096/fj.04-2303fje. — PMID 15772115.
- Wedel T., Van Eys G.J., Waltregny D., Glénisson W., Castronovo V., Vanderwinden JM. Novel smooth muscle markers reveal abnormalities of the intestinal musculature in severe colorectal motility disorders. (англ.) // Neurogastroenterol Motil. : journal. — 2006. — Vol. 18, no. 7. — P. 526—538. — doi:10.1111/j.1365-2982.2006.00781.x. — PMID 16771768.
- Verdin E., Dequiedt F., Kasler H.G. Class II histone deacetylases: versatile regulators. (англ.) // Trends (journals) : journal. — 2003. — Vol. 19, no. 5. — P. 286—293. — doi:10.1016/S0168-9525(03)00073-8. — PMID 12711221.
- Hu E., Chen Z., Fredrickson T., et al. Cloning and characterization of a novel human class I histone deacetylase that functions as a transcription repressor. (англ.) // J. Biol. Chem. : journal. — 2000. — Vol. 275, no. 20. — P. 15254—15264. — doi:10.1074/jbc.M908988199. — PMID 10748112.
- Buggy J.J., Sideris M.L., Mak P., et al. Cloning and characterization of a novel human histone deacetylase, HDAC8. (англ.) // Biochemical Journal : journal. — 2001. — Vol. 350, no. 1. — P. 199—205. — doi:10.1042/0264-6021:3500199. — PMID 10926844. — PMC 1221242.
- Amann J.M., Nip J., Strom D.K., et al. ETO, a target of t(8;21) in acute leukemia, makes distinct contacts with multiple histone deacetylases and binds mSin3A through its oligomerization domain. (англ.) // Molecular and Cellular Biology : journal. — 2001. — Vol. 21, no. 19. — P. 6470—6483. — doi:10.1128/MCB.21.19.6470-6483.2001. — PMID 11533236. — PMC 99794.
- Strausberg R.L., Feingold E.A., Grouse L.H., et al. Generation and initial analysis of more than 15,000 full-length human and mouse cDNA sequences. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2003. — Vol. 99, no. 26. — P. 16899—16903. — doi:10.1073/pnas.242603899. — PMID 12477932. — PMC 139241.
- Durst K.L., Lutterbach B., Kummalue T., et al. The inv(16) fusion protein associates with corepressors via a smooth muscle myosin heavy-chain domain. (англ.) // Molecular and Cellular Biology : journal. — 2003. — Vol. 23, no. 2. — P. 607—619. — doi:10.1128/MCB.23.2.607-619.2003. — PMID 12509458. — PMC 151524.
- Rodriguez M., Yu X., Chen J., Songyang Z. Phosphopeptide binding specificities of BRCA1 COOH-terminal (BRCT) domains. (англ.) // J. Biol. Chem. : journal. — 2004. — Vol. 278, no. 52. — P. 52914—52918. — doi:10.1074/jbc.C300407200. — PMID 14578343.
- Johnson J.M., Castle J., Garrett-Engele P., et al. Genome-wide survey of human alternative pre-mRNA splicing with exon junction microarrays. (англ.) // Science : journal. — 2004. — Vol. 302, no. 5653. — P. 2141—2144. — doi:10.1126/science.1090100. — PMID 14684825.
- Lee H., Rezai-Zadeh N., Seto E. Negative regulation of histone deacetylase 8 activity by cyclic AMP-dependent protein kinase A. (англ.) // Molecular and Cellular Biology : journal. — 2004. — Vol. 24, no. 2. — P. 765—773. — doi:10.1128/MCB.24.2.765-773.2004. — PMID 14701748. — PMC 343812.
- Vannini A., Volpari C., Filocamo G., et al. Crystal structure of a eukaryotic zinc-dependent histone deacetylase, human HDAC8, complexed with a hydroxamic acid inhibitor. (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2004. — Vol. 101, no. 42. — P. 15064—15069. — doi:10.1073/pnas.0404603101. — PMID 15477595. — PMC 524051.
- Waltregny D., North B., Van Mellaert F., et al. Screening of histone deacetylases (HDAC) expression in human prostate cancer reveals distinct class I HDAC profiles between epithelial and stromal cells. (англ.) // European Journal of Histochemistry : journal. — 2005. — Vol. 48, no. 3. — P. 273—290. — PMID 15590418.
- Waltregny D., Glénisson W., Tran S.L., et al. Histone deacetylase HDAC8 associates with smooth muscle alpha-actin and is essential for smooth muscle cell contractility. (англ.) // The FASEB Journal : journal. — Federation of American Societies for Experimental Biology, 2006. — Vol. 19, no. 8. — P. 966—968. — doi:10.1096/fj.04-2303fje. — PMID 15772115.
- Gantt S.L., Gattis S.G., Fierke C.A. Catalytic activity and inhibition of human histone deacetylase 8 is dependent on the identity of the active site metal ion. (англ.) // Biochemistry : journal. — 2006. — Vol. 45, no. 19. — P. 6170—6178. — doi:10.1021/bi060212u. — PMID 16681389.
- Lee H., Sengupta N., Villagra A., et al. Histone deacetylase 8 safeguards the human ever-shorter telomeres 1B (hEST1B) protein from ubiquitin-mediated degradation. (англ.) // Molecular and Cellular Biology : journal. — 2006. — Vol. 26, no. 14. — P. 5259—5269. — doi:10.1128/MCB.01971-05. — PMID 16809764. — PMC 1592721.
- Vannini A., Volpari C., Gallinari P., et al. Substrate binding to histone deacetylases as shown by the crystal structure of the HDAC8-substrate complex. (англ.) // EMBO Reports : journal. — 2007. — Vol. 8, no. 9. — P. 879—884. — doi:10.1038/sj.embor.7401047. — PMID 17721440. — PMC 1973954.
- Nakagawa M., Oda Y., Eguchi T., et al. Expression profile of class I histone deacetylases in human cancer tissues. (англ.) // Oncology Reports : journal. — 2007. — Vol. 18, no. 4. — P. 769—774. — doi:10.3892/or.18.4.769. — PMID 17786334.