Хлорид нитрозила
Хлорид нитрозила (нитрозилхлорид, хлористый нитрозил, оксид-хлорид азота) — жёлтый газ, токсичен, с удушливым запахом. Обычно наблюдается как продукт процесса разложения царской водки — смеси соляной и азотной кислот. Из оксид-галогенидов азота известны также фторид нитрозила NOF и бромид нитрозила NOBr. В ряду NOF—NOCl—NOBr устойчивость оксогалогенидов уменьшается, а NOI не удалось получить.
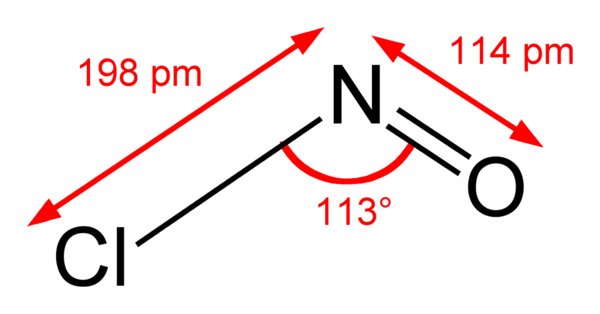
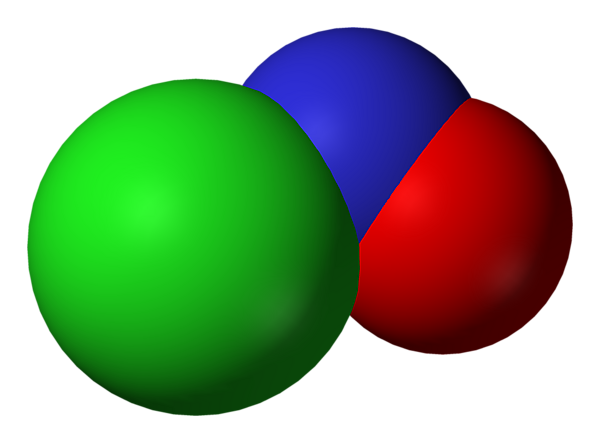
Молекула хлорида нитрозила содержит группу —NO или ион NO+, называемый нитрозилом или нитрозонием. Образование иона NO+ (потенциал ионизации 9,27 эВ) сопровождается упрочением и укорочением связи N=О. Молекула хлорида нитрозила имеет угловую форму с sp²-гибридизацией у атома N. Дипольный момент составляет 1,90 дебай.
Хлорид нитрозила можно рассматривать как хлорангидрид азотистой кислоты.
Общие сведения
| Хлорид нитрозила | |
|---|---|
| Общие | |
| Систематическое наименование |
Хлорид нитрозила |
| Традиционные названия | Хлористый нитрозил |
| Хим. формула | NOCl |
| Физические свойства | |
| Состояние |
жёлто-оранжевый газ красная жидкость |
| Молярная масса | 65,46 г/моль |
| Плотность |
жидкость: 1,417 г/см³ (−12 °C) газ: 2,99 г/л |
| Термические свойства | |
| Температура | |
| • плавления | -61 °C |
| • кипения | -5,4 °C |
| • разложения | 25-100 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | разлагается |
| Классификация | |
| Рег. номер CAS | [2696-92-6] |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 17601 |
| UNII | NHE5I1E5H6 |
| CompTox Dashboard EPA | DTXSID5051945 |
| Рег. номер EINECS | 220-273-1 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E919 |
| RTECS | QZ7883000 |
| Номер ООН | 1069 |
| ChemSpider | 16641 |
| ECHA InfoCard | 100.018.430 |
| Безопасность | |
| NFPA 704 | |
Свойства
- Будучи хлорангидридом азотистой кислоты, хлорид нитрозила реагирует с водой, высвобождая HNO2:
- Реагирует с галогенидами с образованием нитрозил-катиона [NO]+.
- NOCl начинает обратимо разлагаться при температуре 25–100 °C, а выше +100°C полностью разлагается на Cl2 и NO:
- Жидкий хлорид нитрозила способен образовывать комплексные соединения с хлоридами ряда металлов (Pt, Sn, Sb, Ti):
Получение
Хлорид нитрозила можно получать при непосредственном взаимодействии оксида азота(II) с хлором. Он также образуется при нагревании смеси соляной и азотной кислот:
Более удобным способом получения является нагревание нитрозилсерной кислоты с хлоридом натрия:
Дополнительная информация
Хлорид нитрозила зарегистрирован как пищевая добавка с индексом E919.
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3 (Мед-Пол). — 639 с. — ISBN 5-82270-039-8.




![{\displaystyle {\mathsf {2NOCl+SnCl_{4}\rightarrow (NO)_{2}[SnCl_{6}]}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/0ad1808491b940bc1c06b6a4646339855e208682)