Рецептор эритропоэтина
Рецептор эритропоэтина (EpoR) — белок, у людей кодируется геном EpoR[1]. Пептидная цепь EpoR имеет атомную массу 52kDa, атомная масса гликопептида вместе с единственной углеводной цепью - 56-57kDa (по другим данным [1], 66-105kDa). EpoR принадлежит к семейству цитокиновых рецепторов. EpoR присутствует на мембране в виде гомодимеров[2], которые при связывании с лигандом эритропоэтином (Epo) меняют свою конформацию. Эти изменения конформации вызывают аутофосфорилирование киназы Jak2, которая связана с ним изначально, это связано с активностью Jak2[3][4]. Сегодня наиболее аргументированной функцией EpoR является способствование распространению эритроидных предшественников и спасению их от апоптоза[1]. Субъединицы EpoR также способны образовывать гетеродимеры с другими белками-рецепторами — βcR и EPHB4.
Общие сведения
| Рецептор эритропоэтина | |||
|---|---|---|---|
| Доступные структуры | |||
| PDB | Поиск ортологов: PDBe, RCSB | ||
| Идентификаторы | |||
| Символ | EpoR, Epo-R | ||
| Внешние ID | OMIM: 133171 MGI: 95408 HomoloGene: 1731 ChEMBL: 1817 GeneCards: Ген EpoR, Epo-R | ||
| Профиль экспрессии РНК | |||
 | |||
 | |||
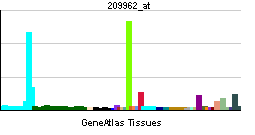 | |||
| Больше информации | |||
| Ортологи | |||
| Вид | Человек | Мышь | |
| Entrez | 2057 | 13857 | |
| Ensembl | ENSG00000187266 | ENSMUSG00000006235 | |
| UniProt | P19235 | P14753 | |
| RefSeq (мРНК) | NM_000121 | NM_010149 | |
| RefSeq (белок) | NP_000112 | NP_034279 | |
| Локус (UCSC) | Chr 19: 0 – 0 Mb |
Chr 9: 0 – 0 Mb |
|
| Поиск в PubMed | Искать | Искать | |
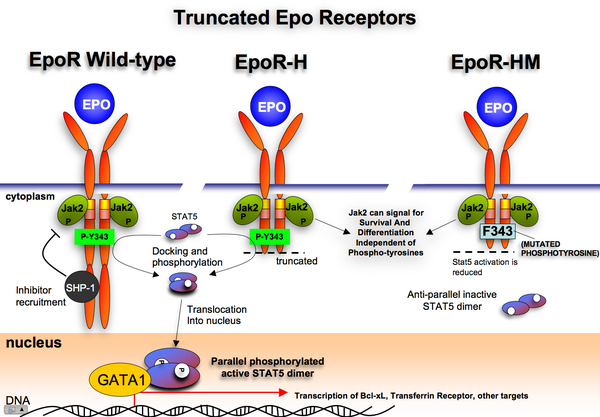
Механизм действия
Цитоплазматические домены EpoR содержат ряд фосфотирозинов, фосфорилированных Jak2 и служащих местами стыковки для различных активаторов внутриклеточного пути.
В дополнение к активации Ras/Akt и ERK/MAP киназы, фосфатидилинозитол 3-киназы/AKT пути и STAT транскрипционных факторов, фосфотирозины также служат в качестве стыковочных участков для фосфатаз, отрицательно воздействующих на сигнализацию EpoR, что предотвращает сверхактивацию.
Главная роль EpoR — стимулировать быстрое распространение клеток-предшественников эритроцитов и спасение этих клеток от гибели.[5]
EpoR вместе с фактором транскрипции GATA-1, вызывает транскрипцию белков, способствующих сохранению Bcl-xL.[6]
Кроме того, EpoR задействован в подавлении экспрессии рецепторов гибели Fas, Trail и TNFa, которые негативно влияют на эритропоэз.[7][8][9]
До сих пор неизвестно, непосредственно ли Epo/EpoR служит причиной распространения и дифференцировки предшественников эритроцитов в естественных условиях, поскольку эффекты были описаны на основе работы in vitro[5].
Есть основания полагать, что дифференцировка эритроидного ряда в основном зависит от присутствия и индукции таких транскрипционных факторов, как GATA-1, FOG-1 и EKLF, а также от супрессии таких миелоидных и лимфоидных факторов, как PU.1.[10] Прямые эффекты сигнализации EpoR — индукция эритроид-специфичных генов, как бета-глобин, в основном плохо поддаются изучению. Известно, что GATA-1 может провоцировать экспрессию EpoR.[11] В свою очередь, сигнальный путь PI3-K/AKT увеличивает активность GATA-1.[12]
Распространение EpoR, вероятнее всего, зависит от типа клеток. Известно, что EpoR может активировать митогенные сигнальные пути и управлять распространением разнообразных неэритроидных и раковых клеток.
Благодаря сигнализации EpoR, CFU-e-предшественники входят в клеточный цикл во время индукции GATA-1 и подавления PU.1.[13] Во время следующих этапов дифференцировки размер клетки уменьшается, а в самом конце ядро выбрасывается наружу. Выживание клеток на этих этапах как раз и зависит от сигнализации EpoR. Также сигнализация EpoR влияет на распространения BFU-e предшественников, которые еще не были достаточно хорошо изучены.
Кроме того, из некоторых данных о макроцитозе при гипоксическом стрессе (когда Epo увеличивается в тысячи раз) следует, что в последующих этапах митоза практически нет, а экспрессия EpoR очень низкая (или отсутствует). Это нужно для того, чтобы как можно скорее обеспечить доступ к запасу эритроцитов. Эти данные доказывают, что ограниченная способность распространяться зависит от Epo, а не от других факторов. EpoR в дифференцировке эритроидного ряда может функционировать в первую очередь как фактор выживания, в то время как его влияние на клеточный цикл в естественных условиях проявляется по прошествии некоторого времени.[14] В других клеточных системах EpoR может обеспечить определенный пролиферативный сигнал. [15]
В данное время роль EpoR в дифференцировке неясна. Экспрессия EpoR может увеличиваться ещё в отделе гемопоэтических стволовых клеток[16]. Неизвестно, какую роль играет сигнализация EpoR в ранней стадии производства эритробластов: разрешающую (то есть индуцирующую только выживание) или инструктирующую (то есть активирующую маркёров для блокировки предшественники на заданной траектории дифференцировки).
Текущие публикации предполагают, что в первую очередь они играют разрешающую роль. Производство BFU-e и CFU-e предшественников было нормальным в эмбрионах грызунов с нокаутированным Epo, равно как и с нокаутированным EpoR[17]. Однако при добавлении Epo или при гипоксическом стрессе число BFU-e и CFU-e крайне сильно возрастает. В любом случае, неясно, какую из двух ролей всё же играет EpoR. Дополнительные вопросы вызывает информация о том, что пути, которые активирует EpoR, общие со многими другими рецепторами. А если заменить EpoR на пролактиновый рецептор, то всё равно идет поддержка дифференцировки и выживания эритроидного ряда, но эти данные, опять же, получены из исследований in vitro[18][19]. В итоге эти данные говорят о том, что, вероятнее всего EpoR участвует в дифференцировке эритроидного ряда не неизвестной инструктирующей функцией, а его ролью в выживании мультипотентных предшественников.
Исследование мутаций на животных
Мыши с усеченным EpoR жизнеспособны[20], что дает возможность предположить, что активность Jak2 достаточна для обеспечения эритропоэза без обязательного фосфотирозинового молекулярного докинга.
Мыши с вариантом рецептора EpoR-HM обладают мутировавшем из тирозина в 343 позиции фенилаланином, что делает молекулярный докинг Stat5 неэффективным. Эти мыши страдают анемией и дают слабый ответ на гипоксический стресс.
Мыши с нокаутированным EpoR имеют дефекты в сердце, мозге и сосудистой системе.
Клиническое значение
Сверхпроизводство эритроцитов повышает шанс развития таких патологий, как тромбоз и апоплексический удар. Дефекты EpoR могут приводить к эритролейкозу и наследственному эритроцитозу. Мутации в Jak2-киназах, связанные с EpoR, также могут привести к истинной полицитемии.[21]
Редко подобное сверхпроизводство эритроцитов просто повышает выносливость без отрицательных эффектов.[22]