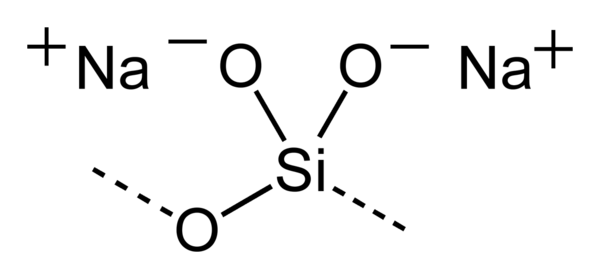
Метасиликат натрия
Метасилика́т на́трия — неорганическое соединение, соль щелочного металла натрия и метакремниевой кислоты с формулой , бесцветные или белые кристаллы, растворяется в холодной воде, образует кристаллогидраты.
Водный раствор известен под названием «жидкое стекло».
Общие сведения
| Метасиликат натрия | |
|---|---|
| Общие | |
| Систематическое наименование |
Метасиликат натрия; силикат натрия |
| Традиционные названия | Кремнекислый натрий |
| Хим. формула | |
| Физические свойства | |
| Состояние | бесцветные или белые кристаллы |
| Молярная масса | 122,06 г/моль |
| Плотность | 2,4; 2,61 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1088; 1089 °C |
| Энтальпия | |
| • образования | −1535 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 18,820; 92,390 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,52 |
| Классификация | |
| Рег. номер CAS | 6834-92-0 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 23266 |
| UNII | 052612U92L |
| CompTox Dashboard EPA | DTXSID7029669 |
| Рег. номер EINECS | 229-912-9 |
| SMILES | |
| InChI | |
| RTECS | VV9275000 |
| ChEBI | 60720 |
| Номер ООН | 3253 |
| ChemSpider | 21758 |
| ECHA InfoCard | 100.027.193 |
| Безопасность | |
| NFPA 704 | |
Нахождение в природе
Входит в состав редких минералов эртиксиита и натросилита [1].
История открытия
Метасиликат натрия был впервые обнаружен фламандским ятрохимиком и врачом Яном Баптиста ван Гельмонтом (1579—1644) в виде жидкого вещества, полученного при плавлении песка с избытком щёлочи. В 1646 году Иоганн Рудольф Глаубер (1604—1670) используя поташ и кремнезём получил вещество, которое он назвал «liquor silicum». И, наконец, в 1818 году немецкий химик и минеролог Иоганн Непомук фон Фукс (1774—1856) воздействуя на кремнёвую кислоту щёлочью получил вещество которое впоследствии стали называть «жидкое стекло»[2].
Получение
Сплавлением диоксида кремния с едким натром или карбонатом натрия:
или:
- .
Разложением ортосиликата натрия:
- .
Безводную соль получают нагреванием кристаллогидрата:
- .
Физические свойства
Метасиликат натрия образует бесцветные или белые кристаллы ромбической сингонии, пространственная группа C cm2, параметры ячейки a = 0,6078 нм, b = 1,053 нм, c = 0,4825 нм, Z = 4.
Хорошо растворим в холодной воде, концентрированные растворы образуют коллоидный раствор «жидкое стекло» гидрозоля переменного состава .
Из водных растворов выделяется кристаллогидрат , который плавится при 47 °С в собственной кристаллизационной воде и начинает разлагаться при температуре выше 100 °С.
В безводном твёрдом веществе метасиликатные анионы фактически является полимером, состоящим из тетраэдров с общими вершинами, а не отдельных ионов [3].
Также известны ряд кристаллогидратов с общей формулой , n = 5, 6, 8, 9 содержащие обособленный гидратированный, приблизительно тетраэдрический анион . Коммерчески доступны пентагидрат силиката натрия или и нонагидрат или [4]. Пентагидрат и нонагидрат имеют свои собственные номера CAS: 10213-79-3 и 13517-24-3 соответственно. Нонагидрат плавится при температуре 48 °C, а пентагидрат — при 72 °C[5].
Химические свойства
Водные растворы имеют щелочную реакцию из-за гидролиза по аниону.
Разлагается в горячей воде с гидролизом:
- .
Разлагается кислотами:
и щелочами:
- .
Реагирует с углекислым газом:
- .
Применение
- Компонент шихты в производстве неорганического стекла.
- Компонент жаростойких красок.
- Добавка в моющие средства и мыло.
- Для пропитки горючих материалов для придания им негорючести.
- В производстве жаростойких кислотоупорных бетонов.
- Наполнитель в облегчённых цементных растворах для цементирования нефтегазовых скважин.
- Водный раствор применяется как клей под названием «жидкое стекло»[6].
- В качестве пищевой добавки (E550), для предотвращающего слипания[7].
- Для сохранения яиц. Когда свежие яйца погружаются в раствор силиката натрия, бактерии, способные разрушить яйцо, удаляются, сохраняя яйцо до девяти месяцев. Перед приготовлением в кипящей воде скорлупы яиц, законсервированных таким образом, необходимо проткнуть скорлупу, чтобы дать выход пару, поскольку скорлупа перестаёт быть пористой[8].
Примечания
Литература
- Химическая энциклопедия / Редколл.: И. Л. Кнунянц и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редколл.: Б. П. Никольский и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.




![{\displaystyle {\ce {SiO2\ +2NaOH->[900-1000~^{\circ }{\text{C}}]Na2SiO3\ +H2O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/8475a5ad1929bf731fe19c08510cea6c17f9e088)
![{\displaystyle {\ce {SiO2\ +Na2CO3->[1150~^{\circ }{\text{C}}]Na2SiO3\ +CO2}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/83bc355d8f580ce9ebe694a5d22167bda511b210)
![{\displaystyle {\ce {Na4SiO4->[1120~^{\circ }{\text{C}}]Na2SiO3\ +Na2O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/839cc1e9ac3ba63b2d79d005b4d6c57936768025)
![{\displaystyle {\ce {Na2SiO3.9H2O->[100-300~^{\circ }{\text{C}}]Na2SiO3\ +9H2O}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/d9c461a434e60921a3c750b7ff7792773ae31e20)










![{\displaystyle {\ce {Na2SiO3\ +(n\ +\ 1)\ H2O->[T]2NaOH\ +(SiO2.nH2O)v}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/71ce19544a76ba3adcad852f0b5dc8a04f15291b)