Замороженный зоопарк
Замороженный зоопарк — это хранилище, где при температуре −196 °C в специальных ёмкостях с жидким азотом хранятся генетические материалы животных, например, образцы ДНК, сперма, яйцеклетки, эмбрионы или живые ткани[1]. Такие материалы могут храниться бесконечно долго и использоваться для искусственного оплодотворения, экстракорпорального оплодотворения, переноса эмбрионов и клонирования. В мире существует несколько криохранилищ, которые используют данную технологию для сохранения биоразнообразия[2].
История и принципы
В 1972 году исследователь из Калифорнийского университета, патологоанатом Куртом Бениршке создал первый замороженный зоопарк в зоопарке Сан-Диего[3][4][5].
«Над „Замороженным зоопарком“ висел плакат с цитатой: „Вы должны собирать вещи по причинам, которых вы пока не понимаете“, — говорит Оливер Райдер, генетик из зоопарка Сан-Диего и один из первых сотрудников Бениршке. — Мы чувствовали, что были хранителями этой растущей коллекции, которая будет иметь такую ценность для будущего, какую мы не могли оценить тогда»[6].
В 1992 году была опубликована работа Грегори Бенфорда, в которой он поддержал идею замороженного зоопарка и предложил создать «Библиотеку жизни»[7][8][2]. Современные зоопарки, например, зоопарк Сан-Диего, и различные исследовательские программы занимаются криоконсервацией генетического материала, чтобы сохранить разнообразие генофонда исчезающих видов или обеспечить возможность реинтродукции таких вымерших видов, как тасманский тигр[9] и мамонт[10].
В 2004 году был основан британский криобанк для животных Frozen Ark. Он имел другую структуру: это была не отдельная коллекция, привязанная к одному учреждению, а распределённая сеть из более чем двух десятков организаций по всему миру. В неё входят зоопарки, музеи и университеты, которые делятся своими знаниями и коллекциями[6].
Сбор материала для создания криоколлекции животных становится проще благодаря большому количеству семенной жидкости у самцов. Получить сперматозоиды можно даже после смерти животного. У самок обычно вырабатывается небольшое количество яиц, но с помощью гормональной терапии можно увеличить их количество до 10-20 ооцитов в зависимости от вида. Некоторые зоопарки предпочитают оплодотворять яйцеклетки и замораживать эмбрионы, поскольку они лучше сохраняются при криоконсервации[11]. Также в некоторых центрах собирают образцы клеток кожи животных, находящихся под угрозой исчезновения или уже вымерших видов. Так, например, исследовательский институт Скриппса успешно разработал метод преобразования клеток кожи в особые клетки, называемые индуцированными плюрипотентными стволовыми клетками (IPS-клетки). Теоретически из этих клеток можно получить сперматозоиды и яйцеклетки[4].
Образцы ДНК необходимы для составления генетического плана видов, которые могут исчезнуть.
«Данная информация может быть использована для целого ряда различных научных исследований, от исследования рака до понимания процессов восстановления, таких как отрастание конечностей, — утверждает Лиза Йон, профессор медицины дикой природы в Ноттингемском университете и научный консультант в Frozen Ark. — Экономя эти ресурсы, мы позволим не только нынешним ученым, но и будущим поколениям ученых делать всевозможные новые открытия»[6].
Недостатки
Замораживание клеток включает в себя более сложный процесс, чем с ДНК. Необходимо предотвратить образование ледяных кристаллов, когда клетки подвергаются воздействию температуры −196 градусов по Цельсию. Для разных типов клеток требуются различные методы заморозки. Например, клетки амфибий сложно заморозить правильно, поэтому они недостаточно представлены в криобанках. Некоторые технологии, которые могли бы оптимизировать использование клеточных линий, всё ещё нуждаются в улучшении[6].
Образцы ДНК из-за экстремально низких температур испытывают различные виды стресса. В частности, сперматозоиды подвергаются воздействию температурного шока, осмотического стресса и окислительного стресса, причём последний является наиболее опасным[12].
Температурный шок возникает из-за повреждения мембраны сперматозоидов в результате их замораживания и последующего размораживания. Осмотический стресс появляется, когда в процессе замораживания внутри ядра образуются кристаллы льда, вызывая дисбаланс осмотического давления внутри клетки.
Окислительный стресс возникает из-за образования избыточного количества активных форм кислорода (ROS), которые являются высокоактивными и разрушительными для всех компонентов клетки[12][13].
В зависимости от типа стресса существуют различные методы борьбы с ним. Так, добавление холестерина в образцы может помочь снизить температурный стресс. Для защиты от осмотического стресса используются специальные белки, которые предотвращают замерзание. Однако наиболее сложным для преодоления является окислительный стресс, вызванный активными молекулами ROS. Тем не менее, существуют способы ограничить повреждения, возникающие при замораживании и оттаивании. Например, добавление определённых белков может повысить шансы на выживание ДНК[12].
Проблемы
После решения вопроса с размножением возникли трудности с перезаселением. Вопрос о том, действительно ли клонирование может помочь восстановить исчезающие виды в дикой природе, остаётся дискуссионным. Некоторые исследователи полагают, что эти усилия и ресурсы можно было бы направить на более действенные меры по охране среды обитания и восстановлению ареала дикой природы, который станет домом не только для одного вида[14].
Потеря среды обитания и конфликты между человеком и дикими животными представляют собой основные опасности для большинства видов, находящихся на грани исчезновения по всему миру.
По словам эколога Дэвида Яховски, если среда обитания будет уничтожена, то попытки клонировать вымерших или находящихся под угрозой исчезновения животных, таких как странствующий голубь, тилацин, лошадь Пржевальского или шерстистый мамонт, не принесут результата[14].
«В ажиотаже вокруг этого нового инструмента мы должны сохранять сильную сосредоточенность на решении проблем, которые приводят к исчезновению или вымиранию большинства видов, — утверждает Дэвид Яховски. — Совершенно ясно, что одно только клонирование не может спасти исчезающие виды. Только когда мы восстановим и обеспечим надлежащую среду обитания и снизим вероятность конфликта между человеком и дикой природой, эти виды могут быть восстановлены»[14].
Применение
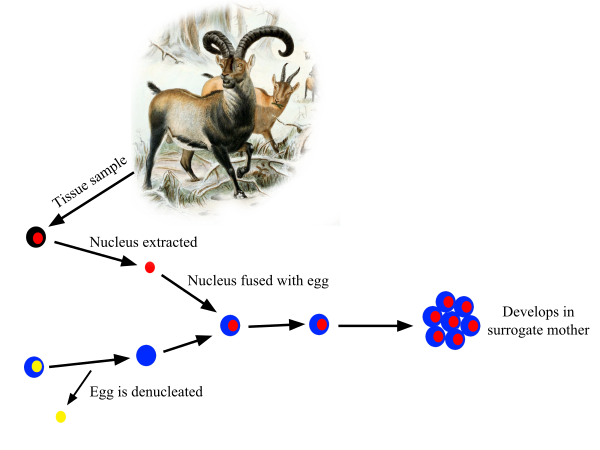
Пиренейский козёл вымер в 2000 году. В 2003 году учёные использовали замороженные клетки последнего представителя данного вида. На первом этапе исследования было получено 439 гибридных яйцеклеток. Для этого в яйцеклетки, из которых предварительно удалили ядра, были пересажены ядра клеток вымершего подвида. После электростимуляции клетки начинали делиться, как если бы они были оплодотворены сперматозоидами. Из всех клеток только 57 были пересажены самкам пиренейского козла, и только семь из них прижились. В результате на свет появился всего один детёныш[15][16] .
Козлёнок прожил всего семь минут после рождения. Причиной смерти стал врождённый дефект лёгких. Возможно, имеющихся клеток недостаточно для создания племенной популяции. Несмотря на неудачу, эксперимент доказал, что клонирование вымерших видов возможно. Опыт открыл перспективы для новых исследований, направленных на сохранение биоразнообразия[17].
Бык-гаур по кличке Ной стал первым клоном из исчезающего вида животных. Для этого эксперимента американские исследователи из института регенеративной медицины использовали криоконсервированные клетки кожи гаура, взятые восемь лет ранее. Учёные извлекли ДНК из этих клеток и внедрили её в яйцеклетку коровы, чтобы создать эмбрион. Корова также послужила суррогатной матерью для развивающегося клона гаура[18]. Гаур прожил всего два дня и умер от дизентерии. Однако данный эксперимент показал, что клонирование может помочь сохранить исчезающие виды животных[19].
Бантенг стал вторым видом животных, находящимся на грани исчезновения, который удалось успешно клонировать[20][21] . Более того, он стал первым клоном, который выжил после младенчества. Исследователи из компании Advanced Cell Technology в Вустере, штат Массачусетс, извлекли ДНК из клеток кожи мёртвого самца бантенга, которые были сохранены в замороженном виде в зоопарке Сан-Диего. Затем они перенесли эту ДНК в яйцеклетки домашних коров бантенга — это называется ядерным переносом соматических клеток.
В результате было создано тридцать эмбрионов, которые были имплантированы домашним коровам бантенг. Два эмбриона появились на свет с помощью кесарева сечения. Первый родился 1 апреля 2003 года, а второй — двумя днями позже. Второй эмбрион страдал от нарушения роста, из-за чего его пришлось умертвить. Первый же выжил и прожил семь лет в зоопарке Сан-Диего, где скончался в апреле 2010 года. Причиной смерти стала травма ноги, после чего его подвергли эвтаназии[22].
В 2020 году на свет появился клон лошади Пржевальского. Для этого был использован генетический материал самца лошади Пржевальского, который родился в 1975 году в Великобритании и с 1978 по 1998 год жил в США. Его ДНК, сохранённая в криоконсервированном состоянии, хранилась в биобанке зоопарка Сан-Диего в течение 40 лет[23].
Исследование родословной отобранного самца показала, что его геном содержит гораздо больше разнообразных генетических комбинаций, чем у любой тогда живущей лошади.
Именно поэтому учёные решили использовать его клетки для создания клона: в случае успеха клоны данной особи позволили бы заметно обогатить генетическое разнообразие стада[24].
В 2020 году специалисты создали яйцеклетку, содержащую генетический материал отобранного самца, и пересадили её суррогатной матери — кобыле домашней лошади. В результате клонирования родился жеребёнок, которого назвали в честь доктора Курта Бениршке. По мнению учёных, животное, которое родилось с помощью замороженной ДНК, может помочь восстановить популяцию исчезающего вида. Прежде в дикой природе лошадь Пржевальского встречалась только в 1969 году[23].
Клонирование было осуществлено методом переноса ядер соматических клеток (SCNT), при котором жизнеспособный эмбрион создаётся путём пересадки ядра соматической клетки, содержащей ДНК, в незрелую яйцеклетку — ооцит, у которой было удалено собственное ядро. Таким образом, был получен эмбрион, генетически идентичный донору соматической клетки[25]. Поскольку ооцит был взят у домашней лошади, это был пример межвидового переноса ядер соматических клеток[26].
В 1979 году считалось, что черноногий хорёк вымер, но спустя более 40 лет учёные смогли воссоздать этот вид, используя генетический материал последних выживших особей. Антония, мать двух детёнышей, была клонирована от черноногого хорька, который умер в 1988 году в зоопарке Сан-Диего. В том же году в США стартовала программа по разведению этих животных в неволе. Специалисты отобрали всего 18 особей в дикой природе из небольшой инбредной, то есть состоявшей из близкородственных особей, популяции, обнаруженной в 1981 году в Вайоминге[27].
В 2021 году исследователи успешно клонировали несколько особей черноногих хорьков, используя клетки, которые были сохранены в специальных хранилищах[28]. Клонирование удалось провести при помощи замороженных генов животного, которое умерло более 30 лет назад. В результате эксперимента родились два хорька, но выжил только один из них. Клонированную особь вымирающего вида назвали Элизабет Энн. Суррогатной матерью для клонированного детёныша стала самка домашнего хорька, в помёте которой также родились два маленьких хорька[29].
В 2024 году популяция черноногого хорька насчитывала 350 особей[14].
Россия
В начале 2010-х годов в Институте цитологии и генетики СО РАН, Новосибирск, был создан криобанк. В нём не только хранятся генетические ресурсы лабораторных животных, но и проводятся исследования, направленные на разработку методов сохранения диких и исчезающих видов животных с помощью современных технологий репродуктивной биологии[30][31].
Как утверждают в институте, возможности криотехнологий велики, а при их стремительном развитии почти фантастические: с их помощью успешно борются с бесплодием, создают банк редких животных и элитных сельскохозяйственных пород.
Затем большинство проектов в этой сфере сосредоточено на сохранении растений.
В 2017 году в Центре превосходства в области биотехнологий Московского государственного университета имени М. В. Ломоносова было открыто криохранилище для культур клеток и меристем растений в рамках проекта «Ноев ковчег». Криобанк рассчитан на 50 000 образцов, которые хранятся в парах жидкого азота при температуре −180° C. Среди образцов есть меристемы ценных сельскохозяйственных видов и культуры клеток, способные синтезировать ценные биологически активные вещества растительного происхождения для биотехнологического применения[32].
В 2024 году специалисты Института биологических проблем криолитозоны Сибирского отделения РАН представили проект первого российского криохранилища, которое представляет собой банк семян с миллионом образцов дикоросов, сельскохозяйственных, древесных и редких видов растений, который разместят в толще многолетнемёрзлых пород Якутии[33].