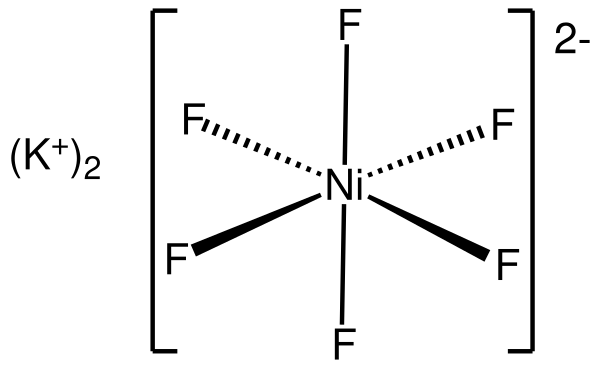
Гексафтороникелат(IV) калия
Гексафтороникелат(IV) калия — неорганическое соединение с химической формулой K2NiF6.
Что важно знать
| Гексафтороникелат(IV) калия | |
|---|---|
| Общие | |
| Систематическое наименование |
Гексафтороникелат(IV) калия |
| Хим. формула | K2NiF6 |
| Физические свойства | |
| Молярная масса | 250,88 г/моль |
| Плотность | 3,03 г/см³ |
| Классификация | |
| Рег. номер CAS | 17218-47-2 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 71431096 |
| CompTox Dashboard EPA | DTXSID20849392 |
| Рег. номер EINECS | 625-130-0 |
| SMILES | |
| InChI | |
| ChemSpider | 21241633 |
| ECHA InfoCard | 100.153.655 |
Получение
Гексафтороникелат(IV) калия получают реакцией хлорида никеля(II), фтора и фторида калия при 275 °C:
Химические свойства
Бурно реагирует с водой, выделяя кислород. Растворяется в безводной плавиковой кислоте с образованием светло-красного раствора. Гексафтороникелат(IV) калия разлагается при 350 °C с образованием гексафтороникелата(III) калия, фторида никеля(II) и фтора:[1][2]
Гексафтороникелат калия — сильный окислитель. Он может превращать фторид хлора(V) и фторид брома(V) в ClF6+ и BrF6+, соответственно:[3]
- (X = Cl или Br , −60 °C , aHF = безводная плавиковая кислота).
Гексафтороникелат калия разлагается при высоких температурах с выделением газообразного фтора, как и фторид тербия(IV), выделяющий фтор в основном одноатомный, а не типичный двухатомный.[4]
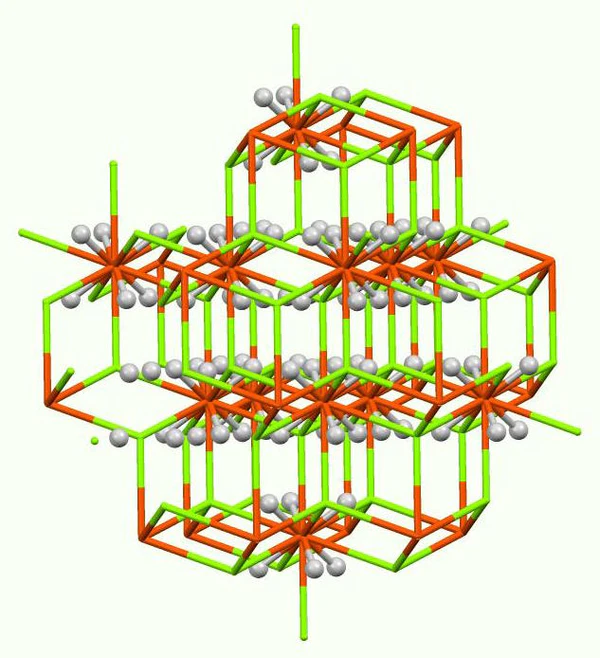
Принимает структуру K2PtCl6 и Mg2FeH6.[5]




![{\displaystyle {\ce {3K_{2}NiF_{6}->[^{\circ }t]2K_{3}NiF_{6}\ +NiF_{2}\ +F_{2}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/d6d2b5b5367900601db8c528ebd794d0833fee4e)
![{\displaystyle {\ce {K_2NiF_6 + 5 AsF_5 + XF_5 ->[aHF] XF_6AsF_6 + Ni(AsF_6)_2 + 2KAsF_6}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/3e17897ab9dc76f29da358e536d9f00ba00abe59)