Фторид хлора(V)
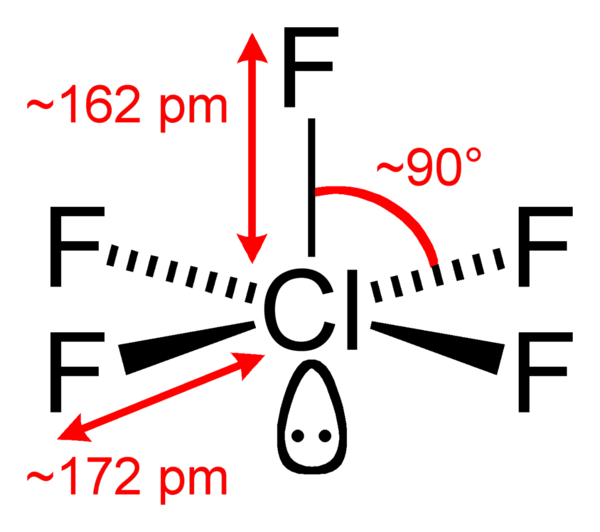
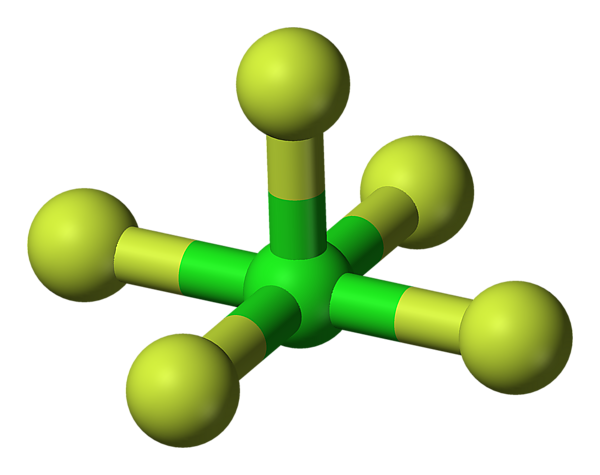
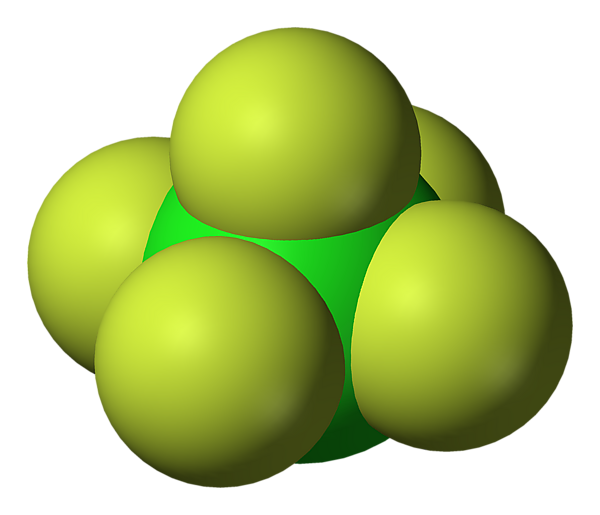
Фтори́д хло́ра(V) (пентафтори́д хло́ра, пятифто́ристый хлор) — ClF5, соединение хлора с фтором, представляющее собой при комнатной температуре бесцветный ядовитый тяжёлый газ с сильным раздражающим запахом. Конденсируется при охлаждении до −13 °C (или при увеличении давления) в бесцветную жидкость. Впервые синтезирован в 1963 году.
Что важно знать
| Фторид хлора(V) | |
|---|---|
| Общие | |
| Систематическое наименование |
Пентафторид хлора |
| Хим. формула | ClF5 |
| Физические свойства | |
| Состояние | бесцветный газ |
| Молярная масса | 130,445 г/моль |
| Плотность | 0,0045 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | −103 °C |
| • кипения | −13,1 °C |
| Энтальпия | |
| • образования | −238,49 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | гидролиз |
| Классификация | |
| Рег. номер CAS | 13637-63-3 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 61654 |
| UNII | O4RJ1HW01H |
| CompTox Dashboard EPA | DTXSID90894056 |
| Рег. номер EINECS | 237-123-6 |
| SMILES | |
| InChI | |
| RTECS | FO2975000 |
| ChemSpider | 55559 |
| ECHA InfoCard | 100.033.734 |
Физические свойства
Температура плавления −103 °C, кипения −13,1 °C. В газовой фазе бесцветен, конденсируется в мутно-белую жидкость и в белые кристаллы. Давление паров в диапазоне от −80 до +25 °C зависит от абсолютной температуры как lg Pмм рт.ст. = 7,2683 − 1137,16/T. Плотность в жидкой фазе при −23 °C равна 1,922 г/см3, в диапазоне от −80 до −23 °C изменяется как 2,696 г/см3 − 3,08⋅10−3 T (K)[1].
Химические свойства
Сильный окислитель и очень сильный фторирующий агент. Реагирует с водой, взаимодействует со всеми элементами, кроме фтора, кислорода, азота и инертных газов[1]:
- С диоксидом кремния при комнатной температуре переходит во фторид кремния(IV)[2]:
- Под действием ультрафиолетового излучения вступает во взаимодействие с PtF6, при этом образуется смесь ClF6PtF6 и ClF4PtF6[3]:
Получение
- Реакция трифторида хлора с газообразным фтором при высоких температуре и давлении:
- Синтез из элементов при 350 °C и давлении 250 атм (фотохимическая активация позволяет снизить давление синтеза до 1 атм).
- Фторирование соединений вида Me[ClF4] (Me = K, Rb, Cs).
- Электролиз раствора ClF3 в HF.
Применение
Применяется как фторирующий агент, но используется редко, так как не имеет преимуществ перед трифторидом хлора. В США было предложено использовать его как компонент ракетного топлива, высококипящий окислитель, однако по данным на 1981 года работы по этой теме находились на стадии стендовых и лабораторных испытаний[4].
Токсичность
Очень токсичен, ядовитый (удушающий) газ.
Примечания
Литература
- Николаев Н. С., Суховерхов В. Ф., Шишков В. Д., Аленчикова И. Ф. Химия галоидных соединений фтора. М.: Наука, 1968.
- Лидин Р. А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.






![{\displaystyle {\mathsf {2PtF_{6}+2ClF_{5}\rightarrow ClF_{6}[PtF_{6}]+ClF_{4}[PtF_{6}]}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/68e89972a20489d8be15642ff17f09d6f6286a08)