Барбитуровая кислота
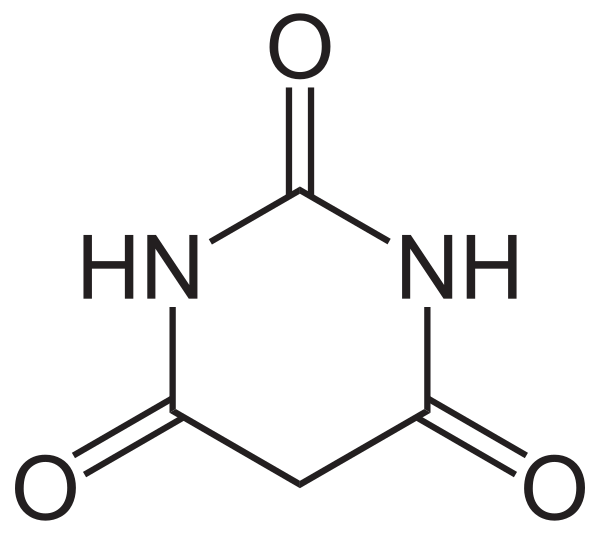
Барбитуровая кислота — 2,4,6-тригидроксипиримидин (2,4,6-пиримидинтрион, N,N-малонилмочевина). Соединение, относящееся к классу уреидов. Представляет собой бесцветные кристаллы с tпл 245 °C (протекает с разложением), растворимые в горячей воде. Плохо растворяется в холодной воде и этаноле, хорошо — в горячей воде, в простых эфирах. Производные барбитуровой кислоты, содержащие алкильные или арильные заместители, а также их соли, называются барбитуратами[1].
Общие сведения
| Барбитуровая кислота | |
|---|---|
| Общие | |
| Хим. формула | C4H4N2O3 |
| Физические свойства | |
| Молярная масса | 128,09 г/моль |
| Классификация | |
| Рег. номер CAS | 67-52-7 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 6211 |
| UNII | WQ92Y2793G |
| CompTox Dashboard EPA | DTXSID8020129 |
| Рег. номер EINECS | 200-658-0 |
| SMILES | |
| InChI | |
| ChEBI | 16294 |
| ChemSpider | 5976 |
| ECHA InfoCard | 100.000.598 |
| Безопасность | |
| NFPA 704 | |
Синтез и свойства
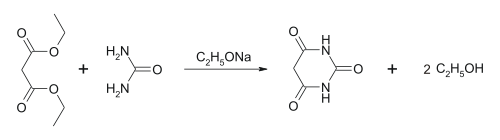
Барбитуровая кислота впервые была синтезирована Адольфом Байером в 1864 г. конденсацией мочевины с малоновой кислотой[2]. Современной модификацией синтеза Байера является использование диэтилового эфира малоновой кислоты в присутствии этилата натрия[3]:
Этот же метод применяется для синтеза 5-замещённых барбитуратов из C-замещённых эфиров малоновой кислоты.
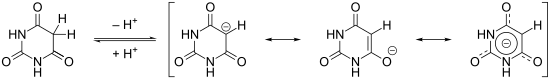
Для барбитуровой кислоты (и 5-монозамещённых барбитуратов) возможны две таутомерных формы: неароматическая пиримидин-2,4,6(1H,3H,5H)-трион и ароматическая 2,4,6-тригидроксипиримидин, в растворах равновесие смещено в сторону преобладания неароматической формы. Вместе с тем, депротонирование барбитуровой кислоты ведёт к образованию резонансно стабилизированного ароматического аниона, что и обуславливает её кислотные свойства:
Дальнейшее депротонирование с сохранением ароматической структуры энергетически невыгодно, поэтому барбитуровая кислота титруется как одноосновная кислота.
Благодаря резонансной стабилизации аниона метиленовая группа барбитуровой кислоты проявляет CH-кислотные свойства: барбитуровая кислота конденсируется с ароматическими альдегидами с образованием 5-арилиденбарбитуровых кислот, нитрозируется с образованием нитрозопроизводного, перегруппировывающегося в 5-оксим (виолуровую кислоту).
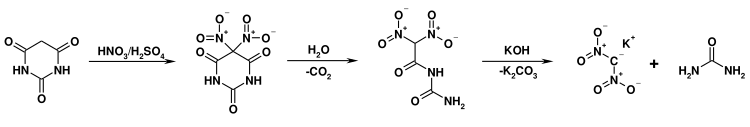
Барбитуровая кислота нитруется дымящей азотной кислотой с образованием 5-нитробарбитуровой (дилитуровой) кислоты, нитрование нитрующей смесью ведёт к образованию 5,5-динитробарбитуровой кислоты, которая может быть далее гидролизована до динитрометана[4]:
Алкилирование барбитуровой кислоты идёт преимущественно по атомам азота (так, при взаимодействии с диметилсульфатом образуется 1,3-диметилбарбитуровая кислота), однако в случае стерических затруднений наряду с N-алкилированием происходит и O-алкилирование, исключением является диазометан, который с барбитуровой кислотой образует 6-метокси-1-метилурацил[5].
При действии оксихлорида фосфора на барбитуровую кислоту происходит замещение хлором кислорода с образованием 2,4,6-трихлорпиримидина.
Применение
Барбитуровую кислоту применяют для получения рибофлавина, пиримидина, виолуровой и мочевой кислоты. Некоторые производные кислоты (в основном 5,5-дизамещённые, к примеру 5,5-диэтилбарбитуровая кислота, 5-фенил5-этилбарбитуровая кислота) являются снотворными средствами.
Барбитуровая кислота применяется в качестве одного из компонентов при фотоколориметрическом определении цианидов по Кенигу.
См. также
Примечания