Адиабата (ЕГЭ-ОГЭ)
Изопроце́сс — это процесс, протекающий при постоянной массе идеального газа и постоянном значении одного из параметров состояния системы.
Если масса идеального газа фиксирована, то его состояние определяется тремя макроскопическими параметрами: давлением, объёмом и температурой. Эти параметры связаны друг с другом уравнением состояния (уравнением Менделеева—Клапейрона, уравнением состояния идеального газа).
Адиаба́тный (адиабати́ческий) проце́сс — термодинамический процесс, при котором система не обменивается теплотой с окружающим пространством.
Адиабатный процесс возможен при хорошей теплоизоляции системы. Примерами таких процессов являются быстрое сжатие или расширение газа. Если термодинамический процесс в общем случае представляет собой три процесса — теплообмен, совершение системой (или над системой) работы и изменение её внутренней энергии[1], то адиабатический процесс в силу отсутствия теплообмена () системы со средой сводится только к последним двум процессам[2]. Поэтому первое начало термодинамики в этом случае приобретает вид[3]:
где — изменение внутренней энергии тела, — работа, совершаемая системой.
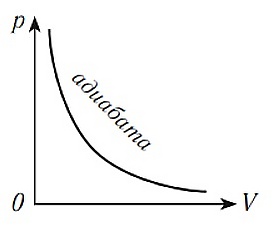
Зависимость давления от объёма газа при адиабатном процессе на графике изображается кривой, называемой адиабата. При адиабатном сжатии давление газа с уменьшением объёма растёт быстрее из-за повышения температуры.
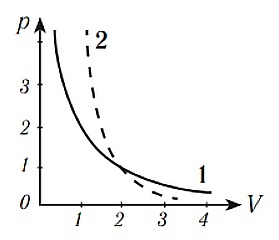
Различие в изображении адиабаты и изотермы дает рисунок, на котором адиабата обозначена цифрой 2, а изотерма — цифрой 1.
Примером адиабатного процесса в природе является образование облаков.
Комментарии
1. Более подробные сведения об изопроцессах выходят за рамки школьного курса физики.
Примечания
Литература
- Акопян А. А. Общая термодинамика. — М.—Л.: Госэнергоиздат, 1955. — 696 с.
- В. И. Крутов, Исаев С. И., Кожинов И. А. и др. Техническая термодинамика / Под. ред. В. И. Крутова. — 3-е изд., перераб. и доп. — М.: Высшая школа, 1991. — 384 с. — ISBN 5-06-002045-2.
- [www.libgen.io/book/index.php?md5=F0DD1E2241DFA869DADAFFD4614905AC Термодинамика. Основные понятия. Терминология. Буквенные обозначения величин] / Отв. ред. И. И. Новиков. — АН СССР. Комитет научно-технической терминологии. Сборник определений. Вып. 103. — М.: Наука, 1984. — 40 с. (недоступная ссылка)
- Кириллин В. А., Сычёв В. В., Шейндлин А. Е. Техническая термодинамика: учебник для вузов. — М.: Издательство МЭИ, 2008. — 496 с. Архивная копия от 24 ноября 2011 на Wayback Machine
- Крестовников А. Н., Вигдорович В. Н. Химическая термодинамика. — 2-е изд., испр. и доп. — М.: Металлургия, 1973. — 256 с.
- Кудрявцев П. С. История физики. — М.: Гос. учебно-педагог. изд-во, 1956. — Т. 1. От античной физики до Менделеева. — 564 с. — 25 000 экз.
- Ландау Л. Д., Лифшиц Е. М. Статистическая физика. Часть 1. — Издание 5-е. — М.: Физматлит, 2005. — 616 с. — («Теоретическая физика», том V). — ISBN 5-9221-0054-8.
- Савельев И. В. Курс общей физики:Молекулярная физика и термодинамика. — М.: Астрель, 2001. — Т. 3. — 208 с. — 7000 экз. — ISBN 5-17-004585-9.
- Сивухин Д. В. Общий курс физики. — М.: Наука, 1975. — Т. II. Термодинамика и молекулярная физика. — 519 с.
- J. Dalton. 2 // Memoirs of the Literary and Philosophical Society of Manchester. — 1802. — Т. 5. — 701 с.
- Alejandro Romanelli. Alternative thermodynamic cycle for the Stirling machine. — Montevideo, Uruguay: Instituto de Física, Facultad de Ingeniería, 2017.